
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ионная полимеризация
Если в радикальной полимеризации активным центром является радикал, то в ионной – ионы. Полимеризация, при которой ее активный центр – заряд иона – передается последовательно по макромолекулярной цепи при ее росте, называется ионной полимеризацией.
Ионная полимеризация, как и радикальная, – цепной процесс. Однако растущая макромолекула при ионной полимеризации в отличие от радикальной представляет собой (в процессе роста) не свободный радикал, а ион – катион или анион. В зависимости от этого различают катионную (карбониевую) и анионную (карбанионную) полимеризации.
Ионная полимеризация протекает в присутствии катализаторов, способствующих образованию ионов. Но, в противоположность инициаторам, они не входят в состав полимера, то есть не расходуются в процессе полимеризации; поэтому ионная полимеризация называется также каталитической.
Особенностью ионной полимеризации является ее очень высокая скорость при низких температурах (от –50 до –70 °С). Эта скорость зависит от полярности среды, в которой протекает полимеризация.
По ионному механизму могут полимеризоваться соединения с кратными связями: >С=С<, >С=О, −С≡N и гетероциклические соединения с неустойчивым циклом, например
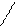
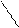 СН2 −СН2 (этиленоксид)
СН2 −СН2 (этиленоксид)
О
8.1.2.1. Катионная (карбониевая) полимеризация
Этот тип полимеризации протекает через образование катионов. В этом случае используют катализаторы, обладающие электроноакцепторными свойствами. Присоединяя молекулу мономера, они образуют катион – ионкарбония. Катализаторами катионной полимеризации могут быть протонные кислоты HClO4, H2 SO4, HCl и катализаторы Фриделя – Крафтса (AlCl3, ВF3, TiCl4, FeCl3, SiCl4 и др.). Катионную полимеризацию можно ускорить с помощью добавок – сокатализаторов НВ: вода, кислоты и другие вещества, являющиеся донорами протонов. Сокатализаторы существенно влияют на активность катализаторов, которые способны взаимодействовать с ними.
По катионному механизму получаются, например, производные этилена с электронодонорными заместителями, карбонильные гетероциклические соединения, а также нитрилы (изобутилен, триоксан, тетрагидрофуран). Катионная полимеризация протекает через три основные стадии.
1. Инициирование. На этой стадии происходит взаимодействие катализатора (АlСl3) и сокатализатора (НВ) с образованием комплексного соединения, которое проявляет свойства сильной кислоты:
AlCl3 + HB ® [AlCl3 B]– H+ эта кислота, отдавая протон молекуле мономера, превращает его в карбониевый ион, уравновешенный комплексным противоионом (ионная пара):
[AlCl3 B]– H+ + CH2 =CHR ® CH3 −C+ HR + AlCl3 B– (s,p-сопряжение).
Большое значение имеет характер заместителя в мономере. Электронодонорные заместители создают избыток электронной плотности на противоположном конце молекулы мономера и этим способствуют присоединению протона (или положительно заряженного иона). Таким образом, в катионной полимеризации особую активность могут проявлять такие мономеры, как пропилен, бутилен, изобутилен, диены.
2. Рост цепи. В процессе роста цепи поляризованные молекулы мономера присоединяются к растущему иону, «внедряясь» между макрокарбкатионом (со стороны его заряженной части) и противоионом (AlCl3 B–):
n CH2 =CHR
 CH3 −C+ HR + CH2 =CHR ® CH3 −CHR−CH2 −С+ НR
CH3 −C+ HR + CH2 =CHR ® CH3 −CHR−CH2 −С+ НR
AlCl3 B– ® CH3 −CHR−[−CH2 −CHR] n −CH2 −C+ HR
AlCl3 B–
3. Обрыв цепи. Рост цепи прекращается в результате отщепления (регенерации) от растущего иона комплексной кислоты или катализатора:
CH3 −CHR−[−CH2 −CHR−] n −CH2 −CHR+ ®
AlСl3 B–

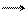 CH3 −CHR−[−CH2 −CHR−] n −CH2 −CHRВ + AlCl3
CH3 −CHR−[−CH2 −CHR−] n −CH2 −CHRВ + AlCl3

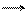 CH3 −CHR−[−CH2 −CHR−] n −CH=CHR + НВ + AlCl3
CH3 −CHR−[−CH2 −CHR−] n −CH=CHR + НВ + AlCl3
В результате обрыва цепи катализатор снова выделяется в свободном виде.
Суммарная скорость катионной полимеризации прямо пропорциональна концентрации катализатора, а средняя степень полимеризации от концентрации катализатора не зависит, но прямо пропорциональна концентрации мономера:
V = k [K], P = k [M],
где [K] – концентрация катализатора,
[M] – концентрация мономера.
8.1.2.2. Анионная (карбанионная) полимеризация
Эта полимеризация протекает через стадию образования карбаниона. Катализаторами здесь служат электронодонорные вещества – основания, щелочные металлы, металлорганические соединения (бутилнатрий, трифенилметилнатрий, Al(C2 H5)3 и его комплексы и др.), гидриды металлов (LiH, NaH), амид калия KNН2. К анионной полимеризации более склонны акрилаты (СН2 =СН−СООR), стирол, диены. В качестве активного центра у них выступает карбанион.
Приведем механизм анионной полимеризации в присутствии катализатора (KNH2) в среде жидкого аммиака при низких температурах.
Инициирование:
_ _ _

 KNH2 K+ + NH2 NH2 + CH2 =CHR ® NH2 −CH2 −CHR K+
KNH2 K+ + NH2 NH2 + CH2 =CHR ® NH2 −CH2 −CHR K+
В присутствии металлорганических соединений (R–Na) образование активного центра происходит внедрением мономера по поляризованной связи металл – углерод:
CH2 =CHR _
 R–Na ® R– + Na+ R−CH2 −CHR Na+
R–Na ® R– + Na+ R−CH2 −CHR Na+
Например, анионная полимеризация бутадиена-1,3 в присутствии катализатора С4 Н9 Li начинается с нуклеофильной атаки диена алкиланионом С4 Н9 –:
C4 H9 Li
 n CH2 =CH−CH=CH2 _
n CH2 =CH−CH=CH2 _
® C4 H9 –(−CH2 −CH=CH−CH2–) n –1 −CH2 −CH=CH−CH2 Li+
Электроноакцепторные заместители (R) в молекуле мономера способствуют присоединению аниона. Оттягивая электронную плотность, они создают дефицит электронов на конце молекулы, к которому присоединяется
отрицательно заряженная группа (NH2 –, R–). В реакции анионной полимеризации могут активно участвовать метилметакрилат, акрилонитрил, метакрилонитрил и другие.
Рост цепи:
_ CH2 =CHR _ n CH2 −CHR

 H2 N−CH2 −CHR H2 N−CH2 −CHR−CH2 −CHR
H2 N−CH2 −CHR H2 N−CH2 −CHR−CH2 −CHR
K+ _ K+
® H2 N–[−CH2 −CHR–] n +1 −CH2 −CHR
K+
В процессе этой реакции, как и при катионной полимеризации, мономер занимает место между макрокарбкатионом и противоионом.
Обрыв цепи. Реакция передачи цепи на растворитель или мономер может вызвать прекращение роста макромолекулярной цепи:
_
H2 N–[−CH2 −CHR–] n +1 −CH2 −CHR K+ + HNH2 ®
® H2 N–[−CH2 −CHR–] n +1 −CH2 −CH2 R + KNH2
Установлено, что скорость анионной полимеризации пропорциональна квадрату концентрации мономера и корню квадратному из концентрации катализатора:
V = k [M2 ] 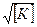 , где [M] – концентрация мономера;
, где [M] – концентрация мономера;
[K] – концентрация катализатора.
Активность карбаниона значительно снижается c увеличением стерического влияния (например, напряжения) в отдельных участках макромолекулы.
В качестве катализатора анионной полимеризации часто выступают щелочные металлы. Они способствуют окислительно-восстановительным реакциям, протекающим между этими металлами и мономерами. Образующиеся металлорганические соединения катализируют дальнейший рост макромолекулярной цепи:
 2Na + CH2 =CH−CH=CH2 ® Na+ CН2 – −CH=CH−CH2 – Na+ CH 2 = CH −C H = CH 2
2Na + CH2 =CH−CH=CH2 ® Na+ CН2 – −CH=CH−CH2 – Na+ CH 2 = CH −C H = CH 2
_
 ® Na+ CH2 – −CH=CH−CH2 −CH2 −CH=CH−CH2 Na+ CH 2 =CH-CH=CH 2
® Na+ CH2 – −CH=CH−CH2 −CH2 −CH=CH−CH2 Na+ CH 2 =CH-CH=CH 2
Полимеризация в этом случае протекает на поверхности металла (натрия). Мономер (бутадиен), адсорбируясь на металле, поляризуется и реагирует с карбанионом. Однако образующийся натрийбутадиеновый (и натрийизопреновый) каучук нестереорегулярен.
Впервые синтез каучука из бутадиена методом анионной полимеризации с применением металлического натрия в промышленных масштабах был осуществлен в нашей стране.
Мономеры, вступающие в анионную полимеризацию, по реакционной активности можно расположить в ряд:
акрилонитрил > метакрилонитрил > метилметакрилат > стирол > бутадиен.
Сейчас методом анионной полимеризации осуществляется промышленное производство полиамидов, полимеров формальдегида, этиленоксида, силоксанов, каучуков.
|
|
Дата добавления: 2014-12-08; Просмотров: 7206; Нарушение авторских прав?; Мы поможем в написании вашей работы!