
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Полиамидных ВМС
|
|
|
|
Получение мономеров для синтеза
Энант (полиамид-7).
Исходное вещество для получения энанта – w-аминоэнантовая кислота, которую получают из этилена и ССl4 в результате реакции теломеризации (оборванной полимеризации):
инициатор
 n CH2 =CH2 + CCl4 Cl(CH2)6 CCl3 (30 %)
n CH2 =CH2 + CCl4 Cl(CH2)6 CCl3 (30 %)
1,1,1,7-тетрахлоралкан
H2 SO4
 Сl(CH2)6 CCl3 Cl(CH2)6 COOH
Сl(CH2)6 CCl3 Cl(CH2)6 COOH
хлорэнантовая кислота
NH3 водн.
 Сl(CH2)6 COOH H2 N(CH2)6 COOH
Сl(CH2)6 COOH H2 N(CH2)6 COOH
w-аминоэнантовая кислота
Капрон (полиамид-6, найлон-6).
Исходное сырье – лактам e-аминокапроновой кислоты – капролактам, который можно получить из фенола, бензола и циклогексана. Наиболее распространено использование в этих целях фенола.



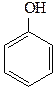 Ni
Ni 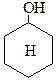 Сплав Ni c Fe
Сплав Ni c Fe  H2 N-OH
H2 N-OH
фенол циклогексанол циклогексанон


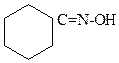 H2 SO4
H2 SO4 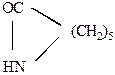
оксим циклогексанона капролактам
Найлон-6,6 (анид, полиамид-6,6)
Исходное сырье – адипиновая кислота и гексаметилендиамин, которые получают по схеме:
1. 
фенол циклогексанол циклогексанон
НООС−(СН2)–СООН ® NºC–(CH2)4 −CºN ® NH2 –(CH2)6 –NH2
адипиновая кислота динитрил адипиновой гексаметилендиамин
кислоты

 2. Н2 С=СН−СН=СН2 Cl2 Cl−СН2 −CH=CH−CH2 −Cl 2Na СN
2. Н2 С=СН−СН=СН2 Cl2 Cl−СН2 −CH=CH−CH2 −Cl 2Na СN
бутадиен
 NC−CH2 −CH=CH−CH2 −CN 2H2 H2 N−(−CH2 −)6 −NH2
NC−CH2 −CH=CH−CH2 −CN 2H2 H2 N−(−CH2 −)6 −NH2
8.5.2. Основные закономерности и отличительные особенности
реакции поликонденсации
По характеру функциональных групп, взаимодействующих между собой при поликонденсации, молекулы делят на:
1. Мономеры с взаимодействующими однородными функциональными группами. Реакция поликонденсации может осуществляться между молекулами одного и того же мономера:
n HO−CH2 −CH2 −OH ® (−CH2 −CH2 O−) n + (n – 1)H2 O
полигликоли
2. Мономеры, содержащие в молекуле взаимодействующие разнородные функциональные группы:
n H2 N−R−COOH ® (−NH−R−CO–) n + (n – 1)H2 O
|
|
|
полиамиды
3. Мономеры с невзаимодействующими однородными функциональными группами. Реакция поликонденсации протекает лишь при взаимодействии мономеров, имеющих функциональные группы одного типа:
n H2 N–R–NH2 + n HOOC–R¢−COOH ®
® (−NH−R−NH−CO−R¢−CO−) n + (2 n – 1)H2 O
4. Мономеры с невзаимодействующими разнородными функциональными группами, например H2 N–R–OH (аминоспирт). Такие мономеры для синтеза полимеров применяются редко.
Если в поликонденсации участвуют однотипные молекулы мономеров, то такой процесс называется гомополиконденсацией:
n HO−(CH2) m −COOH ® H−(−O−(CH2) m −CO−) n −OH + (n + 1)H2 O
оксикислоты
В случае разнотипных мономеров имеет место гетерополиконденсация:
n HOROH + n HOOCRCOOH ® H−(−OROOCR¢CO−) n −OH + (2 n – 1)H2 O
Структура макромолекулярной цепи полимеров определяется функциональностью мономеров. В случае бифункциональных мономеров при поликонденсации образуются линейные полимеры (линейная поликонденсация) (см. примеры выше). Если в поликонденсацию вступают мономеры с функциональностью равной трем, четырем и более, то образуются разветвленные или пространственные полимеры (пространственная поликонденсация). Чем больше функциональных групп содержит мономер, тем больше образующийся полимер похож на жесткую пространственную сетку с высокой степенью поперечного сшивания. Примером такой структуры может служить полимер, полученный из глицерина и фталевой кислоты.
Для процесса поликонденсации имеет значение не только природа и число функциональных групп в молекуле мономера, но и расстояние между ними. Действительно, при взаимодействии функциональных групп, отделенных друг от друга тремя или четырьмя атомами углерода, может образоваться (на первой стадии) вместо линейной макромолекулы циклическое соединение (пяти- или шестичленный цикл), устойчивое согласно теории напряжения Байера. Например, из g-гидроксимасляной кислоты в результате внутримолекулярной конденсации вместо полимера образуется циклический бутиролактон:
|
|
|
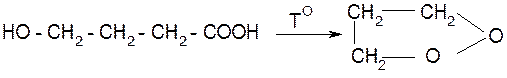
g-гидроксимасляная кислота бутиролактон
Циклическая структура может возникнуть и в результате межмолекулярной конденсации:
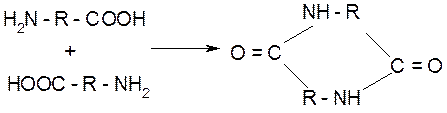
аминокислота дикетопиперазин
Циклизация затрудняется с увеличением расстояния между функциональными группами, в результате чего образуются малоустойчивые циклы. Таким образом, способность бифункциональных мономеров к циклизации зависит от напряженности образующегося цикла, что, в свою очередь, определяется расстоянием между функциональными группами.
Кроме того, на процесс поликонденсации и на реакционную способность мономеров влияет также расположение функциональных групп. Например, внутримолекулярная циклизация становится невозможной, если две функциональные группы находятся в п -положении бензольного кольца. Но циклизация происходит, если эти группы находятся в о -положении. Так, если в о -положении присутствуют нереакционноспособный заместитель или мешающие друг другу в пространстве функциональные группы, то это сказывается и на процессе поликонденсации.
Например, близость аминогрупп в о -фенилендиамине способствуют образованию циклических продуктов, что приводит иногда к полному прекращению линейной поликонденсации.
Таким образом, циклизация затрудняет, а чаще и вообще препятствует процессу поликонденсации в целом. Поэтому при введении в эту реакцию мономеров необходимо учитывать их способность к побочным реакциям, в частности к циклизации.
Поликонденсация также протекает через три основные стадии.
1. Образование активных центров (функциональных групп). Как правило, при поликонденсации исходные мономеры уже содержат активные функциональные группы. Но бывает, что эти группы создаются непосредственно в процессе поликонденсации. Например, при синтезе фенолформальдегидных полимеров активные центры (метильные группы) образуются при взаимодействии фенола с формальдегидом:

фенолоспирт
Эти группы затем вступают в реакцию поликонденсации между собой.
2. Рост цепи. В процессе роста цепи происходит выделение низкомолекулярных веществ. Это приводит к тому, что состав элементарных звеньев полимера не соответствует составу исходного мономера. В этом заключается одно из основных отличий реакции поликонденсации от реакции полимеризации.
|
|
|
Особенностью стадии роста цепи при поликонденсации является то, что ее можно представить как сумму однотипных реакций, происходящих между молекулами мономера, димера, тримера и т. д.
3. Прекращение роста и обрыв цепи. Вторая характерная особенность реакции поликонденсации – ее обратимый характер. При достижении состояния равновесия скорость образования полимера на каждой стадии взаимодействия мономеров равна скорости его разрушения (деструкции). Для получения полимеров с большой молекулярной массой необходимо нарушать это равновесие, удаляя выделяющийся в процессе поликонденсации низкомолекулярный продукт. Для этого или повышают температуру среды, или понижают давление. Первое необходимо для понижения вязкости реакционной среды, которая возрастает по мере течения реакции поликонденсации, а к снижению давления в реакторе прибегают, чтобы высокая температура не разрушала полимер. Таким образом, молекулярная масса полимера и скорость поликонденсации зависит от положения равновесия. Оно, в свою очередь, определяется концентрацией мономера, температурой, катализатором и т. д.
Повышение концентрации мономера ускоряет достижение равновесия и, следовательно, ускоряет поликонденсацию и получение полимера с максимальной молекулярной массой.
Повышение температуры реакции также ускоряет поликонденсацию. Что касается достижения равновесия, то это зависит от теплового эффекта реакции. Если реакция эндотермическая, то с повышением температуры молекулярная масса уменьшается. Так как тепловые эффекты реакций поликонденсации обычно невелики, то и температура реакции мало влияет на молекулярную массу полимера.
Катализаторы повышают скорость реакции и ускоряют достижение равновесия в системе. Если реакция доводится до равновесия, то катализаторы на молекулярную массу полимера не влияют.
|
|
|
Процесс поликонденсации может прекратиться по многим причинам: вследствие установившегося равновесия в системе, изменения структуры и нарушения эквивалентности функциональных групп, увеличения вязкости реакционной среды и связанного с этим уменьшения подвижности макромолекул. Продукты поликонденсации представляют собой сложную смесь. В ее состав могут входить фракции полимергомологов, низкомолекулярные соединения, некоторое количество не вступивших в поликонденсацию мономеров и даже побочных продуктов.
|
|
|
|
|
Дата добавления: 2014-12-08; Просмотров: 975; Нарушение авторских прав?; Мы поможем в написании вашей работы!