
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Осмотическое давление растворов
|
|
|
|
Все растворы обладают способностью к диффузии. Диффузией называется стремление вещества равномерно распределиться по всему предоставленному ему объёму.
Если разделить раствор и растворитель полунепроницаемой перегородкой, через которую проходят молекулы растворителя, но не проходят молекулы растворённого вещества, то в этом случае возможна только диффузия растворителя в раствор.
Процесс односторонней диффузии растворителя в раствор через полунепроницаемую перегородку называется осмосом.
Осмотическим давлением называется сила на единицу площади (Н/м2), заставляющая растворитель переходить через полунепроницаемую перегородку в раствор, находящийся при том же внешнем давлении, что и растворитель. Осмотическое давление разбавленных растворов подчиняется законам идеального газа.
Закон Вант-Гоффа:
Осмотическое давление разбавленных идеальных растворов численно равно тому давлению, которое оказывало бы растворённое вещество, если бы при данной температуре оно в виде идеального газа занимало тот же объём.
π = СRT, (71)
где C – молярная концентрация раствора, моль/л; R – универсальная газовая постоянная 8,314 Дж/(моль∙К); T – абсолютная температура, К.
В растворах электролитов благодаря электролитической диссоциации и увеличения числа частиц экспериментальное значение осмотического давления всегда выше, чем теоретически вычисленное по уравнению (71). Степень отклонения наблюдаемого осмотического давления (πэксп) от вычисленной величины (πвыч) выражается изотоническим коэффициентом
i = 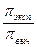 .
.
При вычислении осмотического давления растворов электролитов в уравнение (71) вводится поправочный (изотонический) коэффициент i > 1, учитывающий увеличение числа частиц в растворе вследствие электролитической диссоциации молекул:
|
|
|
π = i СRT. (72)
Для растворов неэлектролитов изотонический коэффициент равен 1. Изотонический коэффициент i зависит от природы электролита и степени диссоциации его молекул. В общем случае при распаде электролита с образованием k – ионов
i = 1+ (k – 1)α. (73)
Если при распаде молекулы образуется два иона k = 2, то формула (73) примет более простой вид:
i = 1+ α. (74)
Пользуясь выражениями (71- 74), можно рассчитать осотическое давление, концентрацию, молекулярные веса растворённых веществ, а также степень диссоциации электролитов в растворах.
Пример 10. Вычислить осмотическое давление 2%-ного раствора глюкозы при 0ºС. Плотность раствора принять равной единице.
Решение. Осмотическое давление вычисляем по формуле (71). Концентрация раствора выражается в моль/дм3, R = 8,314 Дж/(моль∙К), молекулярная масса глюкозы С6Н12О6 равна 180 г/моль.
В 100 г 2%-ного раствора содержится 2 г глюкозы. Поскольку плотность данного раствора равна 1, то в 1дм3 содержится 20 г глюкозы, а это соответствует молярной концентрации С =  , в результате получаем:
, в результате получаем:
π = 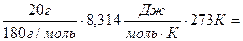 252,2 кПа
252,2 кПа
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 2148; Нарушение авторских прав?; Мы поможем в написании вашей работы!