
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Количество и молярная масса вещества
|
|
|
|
В химических экспериментах и технологических процессах имеют дело не с отдельными атомами и молекулами, а с той или иной массой (или объемом) вещества, в которой содержится огромное число атомов и молекул. Для проведения расчетов с такими массами введено понятие о количестве вещества. Количество вещества обозначается символом n (читается: эн) Единицей количества вещества является моль.
Один моль – это такое количество вещества, в котором содержится столько молекул, атомов, ионов или других структурных единиц, сколько содержится атомов в 12 г изотопа углерода 12С.
Число структурных единиц, составляющих один моль вещества, известно: 6,02∙1023. Это число называется постоянной Авогадро (или числом Авогадро) и является одной из фундаментальных постоянных величин в химии и физике. Поэтому
Один моль – это такое количество вещества, в котором содержится 6,02∙1023 молекул, атомов или других структурных единиц.
Примечание. число Авогадро – это число 6,02∙1023, а постоянная Авогадро – это то же число с указанием единицы измерения: 6,02∙1023 моль–1. Точное значение постоянной Авогадро, установленное несколькими независимыми способами, приведено в справочнике.
Масса одного моля вещества называется молярной массой; её обозначение (символ) – М, единица измерения – г/моль. Для веществ с атомной структурой (благородные газы, металлы) молярная масса равна относительной атомной массе, выраженной в граммах, например: M(Fe) = 55,85 г/моль» 56 г/моль. Для веществ с молекулярной структурой молярная масса равна относительной молекулярной массе, выраженной в граммах, например: M(H2SO4)» 98 г/моль. Для веществ с ионной структурой молярная масса рассчитывается для формульной единицы вещества, например: M(CaCO3)» 100 г/моль.
|
|
|
Примечание. Понятие моль распространяется на любые формульные и структурные единицы: n(Fe) – количество атомов железа, n(H2O) – количество молекул воды, n(NaCl) – количество формульных единиц хлорида натрия, n(Na+) – количество катионов натрия и т.д.
Количество вещества (n), масса (m) и молярная масса (M) связанны между собой:
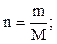 m = n·M;
m = n·M; 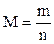
Пример 3. Какое количество воды содержится в 0,9 л этого вещества?
Решение. Плотность воды равна единице (1 кг/л), следовательно, масса 0,9 л воды равна 0,9 кг или 900 г. Молярная масса Н2О 18 г/моль. Искомая величина равна 900:18, т.е. 50 моль.
Пример 4. Вычислить массу 25 моль гидроксида калия.
Решение. Молярная масса КОН равна 56 г/моль, поэтому масса 25 моль этого вещества составляют 25∙56 = 1400 г или 1,4 кг.
Пример 5. Массе 5,39 г соответствует 0,05 моль неизвестного металла. Какой это металл?
Решение. Вычисляем молярную массу неизвестного металла, она равна 5,39: 0,05, т.е. 107,8 г/моль. Следовательно неизвестный металл (находим его по атомной массе в периодической системе) – серебро.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 881; Нарушение авторских прав?; Мы поможем в написании вашей работы!