
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Порядок и беспорядок в природе, детерминированный хаос. 1 страница
|
|
|
|
Можно привести пример перехода от порядка, упорядоченности к хаосу, если нагревать кристаллы поваренной соли, то амплитуда колебаний атомов увеличивается, связь между атомами уменьшается, упорядоченная структура кристалла разрушается и исчезает, а атомы начинают хаотически двигаться. Приведенный пример иллюстрирует процессы, связанные с действием одного из фундаментальных законов природы, имеющего универсальный характер, а именно: со вторым началом (законом) термодинамики.
Суть этого закона заключается в том, что во всех тепловых процессах, связанных с выделением тепла в результате трения, прохождения электрического тока и, как следствие, с выделением тепла при горении, экзотермических химических реакциях и т.д., тепло в естественных условиях всегда переходит от более горячего тела к более холодному, но не наоборот.
Имеется несколько формулировок данного закона. Одна из формулировок, принадлежащая создателю классической термодинамики Э. Клаузиусу, гласит: невозможен процесс, при котором теплота переходила бы самопроизвольно от тел более холодных к телам более теплым.
Другая формулировка связана с понятием энтропии – одной из термодинамических функций, определяющих направление протекания тепловых процессов. В процессах теплопередачи изменение энтропии (ΔS) определяется как ΔS = ΔQ / T, где ΔQ – количество переданного тепла, а Т – абсолютная температура.
Поскольку тепло всегда передается от теплого тела к холодному, то изменение количества тепла ΔQ – величина положительная, а следовательно, и изменение энтропии ΔS есть величина положительная, т.е. энтропия в таких процессах возрастает.
Этот закон носит всеобщий характер и формулируется следующим образом: в замкнутых системах (без притока энергии извне) процессы протекают таким образом, что энтропия системы возрастает.
|
|
|
Таким образом, второе начало термодинамики устанавливает наличие в природе фундаментальной асимметрии, т.е. однонаправленности всех самопроизвольно протекающих процессов.
И хотя количество энергии в замкнутых системах сохраняется, распределение энергии меняется необратимым образом – происходит деградация форм энергии с постепенным переходом всех форм энергии в тепловую. Иными словами, в замкнутых системах самопроизвольно осуществляется необратимый процесс перехода от более упорядоченных структур к менее упорядоченным, или к хаосу.
А поскольку в таких процессах энтропия систем возрастает, то ее принято характеризовать как меру хаоса. Таким образом, из второго закона термодинамики вытекает, что в природе самопроизвольно возможно только одно направление процессов – от порядка к беспорядку, хаосу.
Однако такой вывод противоречит многим фактам. Известны процессы развития от неупорядоченности, хаоса к порядку, перехода от структур, имеющих более низкую организацию, к структурам с более высокой организацией. Примером может служить эволюционное развитие живых организмов от примитивных форм к высокоорганизованным. Долгое время противоречие между вторым законом термодинамики и эволюционной теорией поступательного развития живой природы Дарвина не находило разрешения. Однако сейчас объяснение такому противоречию найдено.
Дело в том, что второй закон термодинамики рассматривает процессы только в замкнутых системах, в то время как живые системы являются открытыми, т.е. обмениваются энергией и веществом с внешней средой. В открытых системах энтропия может, как возрастать, так и уменьшаться, тогда как в целом для открытых систем в совокупности с внешней средой обитания второй закон термодинамики справедлив. Таким образом, в открытой системе энтропия может уменьшаться за счет увеличения энтропии во внешней среде.
|
|
|
В результате при определенных неравновесных условиях в системе за счет внутренних перестроек могут возникнуть упорядоченные структуры. Эту особенность системы называют самоорганизацией, а сами структуры, возникающие в диссипативных (рассеивающих энергию) системах при неравновесных необратимых процессах, – диссипативными (по терминологии И. Пригожина). Под действием флуктуации возникают коллективные формы движения и новые структуры более высокой организации.
Структурные уровни организации материи. В настоящее время принято единую Природу для удобства делить на три структурных уровня – микро-, макро- и мегамир. Естественными, хотя отчасти и субъективными, признаками деления являются размеры и массы исследуемых объектов.
Микромир – мир предельно малых, непосредственно не наблюдаемых микросистем с характерным размером от 10–8 см и менее (атомы, атомные ядра, элементарные частицы).
Макромир – мир макротел, начиная от макромолекул (размеры от 10–6 см и выше) до объектов, размерность которых соотносима с масштабами непосредственного человеческого опыта – миллиметры, сантиметры, километры, вплоть до размеров Земли (длина экватора Земли равна ~ 109 см).
Мегамир – мир объектов космического масштаба от 109 см до 1028 см. Этот диапазон включает размеры Земли, Солнечной системы, Галактики, Метагалактики.
Хотя микро–, макро– и мегамир тесно взаимосвязаны и составляют единое целое, тем не менее на каждом из этих структурных уровней действуют свои специфические законы: в микромире – законы квантовой физики, в макромире – законы классического естествознания, прежде всего классической физики: механики, термодинамики, электродинамики. Законы мегамира основаны в первую очередь на общей теории относительности.
Микромир. Атомная физика. Научные основы атомно-молекулярного учения были заложены гораздо позднее в работах русского ученого М.В. Ломоносова, французских химиков Л. Лавуазье и Ж. Пруста, английского химика Дж. Дальтона, итальянского физика А. Авогадро и других исследователей.
|
|
|
Периодический закон Д.И. Менделеева показал существование закономерной связи между всеми химическими элементами. Считалось, что при всех химических превращениях разрушаются и создаются только молекулы, атомы же остаются неизменными и не могут дробиться на части. И, наконец, в конце XIX в. были сделаны открытия, показавшие сложность строения атома и возможность превращения одних атомов в другие.
Г.Р. Кирхгоф и Р.В. Бунзен обнаружили, что каждому химическому элементу соответствует характерный, присущий только ему набор спектральных линий в спектрах испускания и поглощения.
Изучение свойств катодных лучей привело к заключению, что они состоят из мельчайших частиц, несущих отрицательный заряд. Эти частицы получили название электронов.
В 1896 г., изучая люминесценцию различных веществ, А.А. Беккерельслучайно обнаружил, что соли урана, излучают без предварительного их освещения. Это излучение было названо радиоактивным излучением, позднее было установлено, что оно состоит из тяжелых положительно заряженных α -частиц, легких отрицательных β-частиц (электронов) и электрически нейтрального γ-излучения. Открытие электрона можно считать началом рождения атомной физики, обусловившим попытки построения моделей атома. Первые модели атома на основе представлений классической механики и электродинамики появились в 1904 г.: автором одной из них стал японский физик Хантаро Нагаока, другая принадлежала английскому физику Дж. Томсону – автору открытия электрона.
Дж. Томсон предпринял попытку теоретически объяснить периодическую систему элементов Д. И. Менделеева. Э. Резерфорд в 1912 г. и открыл атомное ядро, масса которого примерно в 8000 раз больше массы электрона, а положительный заряд равен по модулю удвоенному заряду электрона, ядро имеет диаметр порядка 10–12–10–13 см, размер атома примерно 10–8 см, т.е. в 10 – 100 тысяч раз превышает размеры ядра. Если принять заряд электрона за единицу, то заряд ядра оказался в точности равен номеру данного химического элемента в периодической системе элементов Д.И. Менделеева.
|
|
|
Из опытов Резерфорда непосредственно вытекала планетарная модель атома с положительно заряженным атомным ядром. Электроны должны двигаться вокруг ядра под действием электрических кулоновских сил подобно планетам вокруг Солнца. В атоме водорода вокруг ядра обращается всего лишь один электрон. Ядро было названо Резерфордом протоном и стало рассматриваться как элементарная частица. Размер атома определяется радиусом орбиты движения его электронов.
Вскоре выяснилось, что модель атома Резерфорда противоречит законам электродинамики, из которых следует, что движение электронов по круговым орбитам происходит с ускорением, а ускоренно движущийся заряд, согласно законам электродинамики Максвелла, должен излучать электромагнитные волны (ω – частотой, равной частоте его обращения вокруг ядра). Излучение сопровождается потерей энергии. Теряя энергию, электроны должны приближаться к ядру и упасть на него, но этого не происходит, атомы устойчивы, могут существовать неограниченно долго, не излучая электромагнитные волны. Выход нашел датский ученый Н.Бор, сделав вывод о том, что законы классической механики и электродинамики вообще не применимы в микромире и, в частности, в атоме. Чтобы сохранить наглядную планетарную модель атома Резерфорда, он сформулировал два постулата (постулаты Бора), идущие вразрез и с классической механикой, и с классической электродинамикой. Эти постулаты заложили основы принципиально новых теорий микромира – квантовой механики и квантовой электродинамики (квантовой теории электромагнитного поля). Обосновывая свои постулаты, Бор опирался на идею существования квантов электромагнитного поля, выдвинутую в 1900 г. М. Планком и развитую затем А. Эйнштейном (для объяснения фотоэффекта).
Постулаты Бора: электрон может двигаться вокруг ядра не по любым орбитам, а только по та называемым устойчивым, или квантовым, орбитам, на которых атом не излучает электромагнитных волн. Переход электрона с удаленной орбиты на более близкую орбиту сопровождается потерей энергии электрона и излучением атомом кванта.
Простейшим из атомов является атом водорода: вокруг ядра вращается только один электрон. Исходя из постулатов Бор рассчитал радиусы возможных орбит для этого электрона и нашел, что они относятся, как квадраты натуральных чисел: 1:2: 3:...: п, где п главное квантовое число. Радиус ближайшей к ядру первой орбиты в атоме водорода равняется 0,53 ангстрема.
Развивая волновые идеи частиц микромира, Э. Шрёдингер создал математическую волновую модель атома в виде знаменитого сейчас волнового дифференциального уравнения Шрёдингера:
Анализ волнового уравнения Шрёдингера показал, что с его помощью можно определить все возможные дискретные энергии Еп в атоме. Кроме того, было выяснено, что волновая функция не позволяет абсолютно точно определить положение электронов в атомах, можно говорить лишь о вероятности нахождения электронов в том или ином месте атома, которая характеризуется квадратом амплитуды волны.
В настоящее время на основе квантовой механики, а также квантовой электродинамики – квантовой теории электромагнитного поля, разработанной в 1927 г. П.А. Дираком, удалось объяснить многие особенности поведения многоэлектронных атомно-молекулярных систем. В частности, удалось разрешить важнейший вопрос о структуре атомов различных элементов и установить зависимость свойств элементов от строения электронных оболочек им атомов.
Число электронов, вращающихся вокруг ядра атома, соответствует порядковому номеру элемента в периодической системе Д.И. Менделеева. Электроны расположены послойно. Каждому слою принадлежит определенное заполняющее или как бы насыщающее его число электронов. Электроны одного и того же слоя характеризуются близкими значениями энергии, т.е. находятся примерно на одинаковом энергетическом уровне. Вся оболочка атома распадается на несколько энергетических уровней (n). Электроны каждого последующего слоя находятся на более высоком энергетическом уровне, чем электроны предыдущего слоя. Максимальное число электронов (N), могущих находиться на данном энергетическом уровне (n), определяется по формуле N = 2n2, т.е. на первом уровне (n=1) может находиться два электрона, на втором (п = 2) – восемь электронов, на третьем (n= 3) – восемнадцать.
Атомы, лишившиеся одного или нескольких электронов, становятся заряженными положительно, атомы, присоединившие электроны, − отрицательно. Такие заряженные частицы называются ионами.
Состояние каждого электрона в атоме характеризуется четырьмя квантовыми числами – n, l, т, s:
1) n – главное квантовое число, характеризует энергию электрона на соответствующей орбите (n);
2) l – орбитальное квантовое число, характеризует форму орбиты (электронного облака) и может изменяться в атоме от 0 до n = 1;
3) т – магнитное квантовое число, характеризует ориентацию орбит(электронных облаков) в пространстве и может принимать значения от +1 до –1;
4) s – спиновое квантовое число, характеризует вращение электрона вокруг собственной оси и может принимать только два значения: s = ±1/2.
Согласно одному из важнейших принципов квантовой механики – принципу Паули, в атоме не может быть электронов, у которых все четыре квантовых числа одинаковы. В рамках квантовой механики получили полное объяснение, как структура атомов, так и изменение свойств химических элементов в периодической системе Д.И. Менделеева.
Свое место в ряду элементарных частиц занял фотон – частица электромагнитного поля, не имеющая массы покоя. Синтез квантовой механики и специальной теории относительности привел к предсказанию существования античастиц. Оказалось, что у каждой частицы должен быть как бы свой «двойник» – другая частица с той же массой, но противоположным электрическим или каким-либо другим зарядом. Английский физик П.А. Дирак – основатель релятивистской к пантовой теории поля – предсказал существование позитрона и возможность превращения фотона в пару электрон-позитрон и обратно. Позитрон – античастица электрона – экспериментально был открыт и 1934 г. К.Д. Андерсономв космических лучах.
Ядерная физика. По современным представлениям, атомные ядра элементов состоят из протонов и нейтронов. Первые указания на то, что и состав ядер входят протоны (ядра атомов водорода) были получены Резерфордом в 1919 г. в результате его нового (после открытия строения атома) сенсационного открытия – расщепления атомного ядра под действием α-частиц и получения новых химических элементов в результате первой искусственной ядерной реакции.
Схема реакции Резерфорда может быть представлена следующим образом: α–частица попадает в атомное ядро азота  N и поглощается им. Образующееся при этом промежуточное ядро изотопа фтора
N и поглощается им. Образующееся при этом промежуточное ядро изотопа фтора  F оказывается неустойчивым: оно выбрасывает из себя один протон, превращаясь в ядро изотопа кислорода
F оказывается неустойчивым: оно выбрасывает из себя один протон, превращаясь в ядро изотопа кислорода 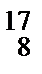 О.
О.
В 1932 г. Д.Д. Иваненко опубликовал заметку, в которой высказал предположение, что наряду с протоном структурным элементом ядра также является нейтрон. В 1933 г. он обосновал протон-нейтронную модель ядра и сформулировал основной тезис, заключающийся в том, что в ядре имеются только тяжелые частицы – протоны и нейтроны. При этом обе частицы могут превращаться друг в друга. В дальнейшем протон и нейтрон стали рассматривать как два состояния одной частицы – нуклона.
А в том же 1933 г. Дж. Чедвик экспериментально доказал существование нейтронов в атомных ядрах. Он облучал α–частицами бериллиевую пластинку и исследовал реакцию превращения бериллия (Be) в углерод (С) с испусканием нейтрона n.
Нейтроны, вылетающие из бериллия, направлялись в камеру Вильсона, наполненную азотом (N), и при попадании нейтрона в и протон атома азота образовывалось ядро бора (В) и α–частицы.
Сам нейтрон не дает трека в камере Вильсона, но по трекам ядра бора и α–частицы можно рассчитать, что данная реакция вызвана нейтральной частицей массой в одну атомную единицу массы, т.е. нейтроном. Отметим, что свободный нейтрон существует недолго, он радиоактивен, период его полураспада составляет около 8 мин, после чего он превращается в протон, испуская β–частицу (электрон) и нейтрино. После открытия нейтрона протон-нейтронная модель строения атомных ядер Д.Д. Иваненко стала общепризнанной.
Все ядерные реакции сопровождаются испусканием тех или иных элементарных частиц. Продукты ядерных реакций оказываются радиоактивными, их называют искусственно радиоактивными изотопами. Явление искусственной радиоактивности было открыто в 1934 г. известными французскими физиками Фредериком и Ирен Жолио-Кюри.
Как и естественно радиоактивные вещества, искусственно полученные радиоактивные изотопы испускают известные α, β, и γ–излучения. Но кроме перечисленных излучений Фредерик и Ирен Жолио-Кюри открыли новый вид радиоактивности – испускание положительных электронов-позитронов.
Ниже приведены основные сведения о свойствах и строении ядер.
1. Ядром называется центральная часть атома, в которой сосредоточена практически вся масса атома и его положительный электрический заряд. Все атомные ядра состоят из протонов и нейтронов, которые считаются двумя зарядовыми состояниями одной частицы – нуклона.
Протон имеет положительный электрический заряд, равный по абсолютной величине заряду электрона е =1,6 –19 Кл и массу покоя тр ~ 1,6726 • 10 –27кг. Нейтрон не имеет электрического заряда, его масса немного больше массы протона – тп = 1,6749 • 10 –27 кг.
Массу ядер элементарных частиц обычно выражают в атомных единицах массы (а.е.м.). За атомную единицу массы принята 1/12массы изотопа углерода 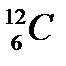 : 1 а.е.м. = 1,66 • 10 –27 кг. Следовательно, тр = 1,00728 а.е.м., а тп = 1,00866 а.е.м.
: 1 а.е.м. = 1,66 • 10 –27 кг. Следовательно, тр = 1,00728 а.е.м., а тп = 1,00866 а.е.м.
2. Зарядом ядра называется величина Ze, где е –величина заряда протона; Z – порядковый номер химического элемента в периодической системе Менделеева, равный числу протонов в ядре.
В настоящее время известны ядра с порядковым номером Z = 1 до Z = 114. Для легких ядер отношение числа нейтронов (N) к числу протонов (Z) близко или равно единице. Для ядер химических элементов, расположенных в конце периодической системы, отношение N/Z = 1,6.
3. Общее число нуклонов в ядре А = N + Z называется массовым числом. Нуклонам (протону и нейтрону) приписывается массовое число, равное единице. Ядра с одинаковыми Z, но различными А называются изотопами. Ядра, которые при одинаковом А имеют различные Z, называются изобарами. Ядра химических элементов принято обозначать символом .X, А, Z где X – символ химического элемента; А – массовое число; Z – атомный номер.
4. Размер ядра характеризуется радиусом ядра, имеющим условный смысл ввиду размытости границ ядра. Эмпирическая формула для радиуса ядра R = R А, где R= (1,3/1,7)10 –15 м, может быть истолкована как пропорциональность объема ядра числу нуклонов в нем.
5. Ядерные частицы имеют собственные магнитные моменты, которыми определяется магнитный момент ядра (Ртт) в целом. Единицей измерения магнитных моментов ядер служит ядерный магнетон μ яд = eh/2тр, где е – абсолютная величина заряда электрона; h – постоянная Планка; тр – масса протона. Ядерный магнетон μ яд в 1836,5 раза меньше магнитного момента электрона в атоме, откуда следует, что магнитные свойства атомов определяются магнитными свойствами его электронов.
6. Распределение электрического заряда протонов по ядру в общем случае несимметрично. Мерой отклонения этого распределения сферически симметричного является квадрупольный электрический момент ядра Q.
Нуклоны, составляющие ядро, связаны между собой особыми силами притяжения – ядерными силами. Устойчивость атомных ядер большинства элементов свидетельствует о том, что ядерные силы исключительно велики: они должны превышать значительные кулоновские силы отталкивания, действующие между протонами, расположенными на расстояниях порядка 10–13 см (порядок размеров ядра). Ядерные силы – силы особого рода, связанные с существованием внутри ядра особого вида материи – ядерного поля.
В настоящие время принята мезонная теория ядерных сил, согласно которой нуклоны взаимодействуют друг с другом путем обмена особыми элементарными частицами – π –мезонами – квантами ядерного поля.
Наличие обменных частиц в ядре – мезонов – вначале было предсказано теоретически японским ученым Хидоки Юкавой в 1936 г., а затем открыто в космических лучах в 1947 г.
Общая характеристика ядерных сил сводится к следующему.
1. Ядерные силы являются короткодействующими силами. Они проявляются лишь на весьма малых расстояниях между нуклонами ядра порядка 10 –15 м. Длина (1,5 ÷2,2) –10 –15 м называется радиусом действия ядерных сил.
2. Ядерные силы обнаруживают зарядовую независимость: притяжение между двумя нуклонами одинаково независимо от зарядового состояния нуклонов – протонного или нуклонного.
3. Ядерные силы обладают свойством насыщения, которое проявляется в том, что нуклон в ядре взаимодействует лишь с ограниченным числом ближайших к нему соседних нуклонов.
Энергия, необходимая для разобщения нуклонов, составляющих ядро, называется энергией связи ядра. Величину энергии связи можно определить на основе закона сохранения энергии и закона пропорциональности массы и энергии в соответствии с формулой Эйнштейна Е = тс2.
Согласно закону сохранения энергии, энергия нуклонов, связанных в ядре, должна быть меньше энергии разобщенных нуклонов на величину энергии связи ε0. С другой стороны, согласно закону пропорциональности массы и энергии, изменение энергии системы ΔW должно сопровождаться пропорциональным изменением массы системы на Δm, т.е. ΔW = Δmc2, где с – скорость света в вакууме.
Так как в данном случае ΔW есть энергия связи ядра, то масса атомного ядра должна быть меньше суммы масс нуклонов, составляющих ядро, на величину Δm, которая называется дефектом массы ядра. Из соотношения ΔW = Δmc2 можно рассчитать энергию связи ядра, если известен дефект массы этого ядра Δm.
Общая формула для расчета энергии связи любого ядра (в джоулях) будет иметь вид: ΔW = c2{[Z-mp+{A-Z)mn]- тя}, где Z– атомный номер; А — массовое число.
Энергия связи ядра, приходящаяся на один нуклон, называется удельной энергией связи ( ε ). Следовательно, ε = ΔW / А (удельная энергия связи) характеризует устойчивость атомных ядер. Чем больше s, тем устойчивее ядро. На рис. 1 представлены результаты расчетов удельных энергий связи для разных атомов (в зависимости от массовых чисел А).
Из графика на рис. 1 следует, что удельная энергия связи максимальна (8,65 МэВ) у ядер с массовыми числами порядка 100. У тяжелых и легких ядер она несколько меньше (например, 7,5 МэВ у урана и 7 МэВ у гелия), у атомного ядра водорода 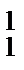 H удельная энергия связи равна нулю, что вполне понятно, потому что в этом ядре нечего разобщать: оно состоит только из одного нуклона (протона).
H удельная энергия связи равна нулю, что вполне понятно, потому что в этом ядре нечего разобщать: оно состоит только из одного нуклона (протона).
Всякая ядерная реакция сопровождается выделением или поглощением энергии. При делении тяжелых ядер с массовыми числами А порядка 100 (и более) ядерная энергия выделяется.
| εуд, МэВ |
 Н Н
|
 Не Не
|
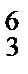 Li Li
|
 B B
|
 Не Не
|
 Kr Kr
|
 Pt Pt
|
 U U
|
| а.е.м. |
Рис. 1. Зависимость удельных энергий связи от массовых чисел
Выделение ядерной энергии происходит и при ядерных реакционного типа – при объединении (синтезе) нескольких легких ядер в одно ядро. Таким образом, выделение ядерной энергии происходит как при реакциях деления тяжелых ядер, так и при реакциях синтеза легких ядер. Количество ядерной энергии Δ ε, выделяемое каждым прореагировавшим ядром, равно разности между энергией связи ε продукта реакции и энергией связи исходного ядерного материала.
Соотношение ∆E∆t > ħ/2 означает, что преобразование энергии с точностью ∆Е должно занять интервал времени равный, по меньшей мере, ∆t~ ħ/∆E. Это соотношение ответственно за естественную ширину спектральных линий атомов и ионов. Время жизни возбужденного состояния атомов имеет порядок t ~10-8÷10-9с. Следовательно, неопределенность энергии таких состояний составляет ∆E~ ħ/t, чему соответствует естественная ширина спектральных линий. Если неопределенность энергии ∆Е ~ ħ/∆t соответствует энергии некоторой частицы (mс2, hv), to эта частица, возникнув из «ничего», может находиться в виртуальном состоянии время ∆t без нарушения закона сохранения энергии. В современной квантовой теории поля взаимодействие частиц и их взаимные превращения рассматриваются как рождение или поглощение каждой реальной частицей виртуальных частиц. Любая частица непрерывно испускает или поглощает виртуальные частицы разных типов.Так, например, электромагнитное взаимодействие – результат обмена виртуальными фотонами, гравитационное – гравитонами. Поле ядерных сил обусловлено виртуальными π – мезонами. Слабое взаимодействие создают векторные бозоны (открытые в 1983 году в ЦЕРНе, Швейцария-Франция). А переносчиком сильного взаимодействия являются глюоны (от английского слова, означающего «клей»).
Получение экспериментальной информации об одних физических величинах, описывающих микрочастицу, неизбежно связано с потерей информации о других величинах, дополнительных к первым. Это утверждение, впервые сформулированное датским физиком Н. Бором, называется принципом дополнительности. Бор объяснял принцип дополнительности влиянием измерительного прибора, который всегда является макроскопическим прибором, на состояние микрообъекта. Однако с позиций современной квантовой теории, состояния, в которых взаимно дополнительные величины имели бы одновременно точно определенные значения, принципиально невозможны. Принцип дополнительности отражает объективные свойства квантовых систем, не связанные с существованием наблюдателя, а роль измерительного прибора заключается в «приготовлении» некоторого состояния системы. Любая новая теория, претендующая на более глубокое описание физической реальности и на более широкую область применения, чем старая, должна включать предыдущую как предельный случай. Так релятивистская механика (специальная теория относительности) в пределе малых скоростей переходит в ньютоновскую. В квантовой механике принцип соответствия требует совпадения ее физических следствий в предельном случае с результатами классической теории. В принципе соответствия проявляется тот факт, что квантовые эффекты существенны лишь при рассмотрении микрообъектов, когда величины размерности действия сравнимы с постоянной Планка. С формальной точки зрения принцип соответствия означает, что в пределе ħ → 0 квантовомеханическое описание физических объектов должно быть эквивалентно классическому. Значение принципа соответствия выходит за рамки квантовой механики – он войдет составной частью в любую новую теоретическую схему. В современной физике термин «элементарные частицы» обычно употребляется не в своем точном значении, а менее строго – для наименования большой группы мельчайших частиц материи, которые не являются атомами или атомными ядрами (исключение составляет протон). Наиболее важное свойство всех элементарных частиц – способность рождаться и уничтожаться (испускаться и поглощаться) при взаимодействии с другими частицами. Сейчас общее число известных науке элементарных частиц (вместе с античастицами) приближается к 400. Некоторые из них стабильны и существуют в природе в свободном или слабосвязанном состоянии. Это – электроны, протоны, нейтроны, фотоны и различного сорта нейтрино.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 486; Нарушение авторских прав?; Мы поможем в написании вашей работы!