
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Бор – типичный неметалл
|
|
|
|
Общая и неорганическая химия
ЛЕКЦИИ
Лекция 13. Бор и подгруппа алюминия (Al, Ga, In, Tl).
| Свойства простых веществ[[1],[2]] | |||||
| B | Al | Ga | In | Tl | |
| Температура плавления, 0С | |||||
| Температура кипения, 0С | |||||
| Радиус атома, пм (10-12 м) | |||||
| Радиус иона Э3+, пм |
Элементарный бор существует в кристаллической и аморфной формах. Кристаллический бор – полупроводник; с повышением температуры его электропроводность возрастает, в отличие от металлов.
Бор образует с водородом ряд летучих соединений – боранов, при комнатной температуре диборан B2H6 и тетраборан B4H10 газообразны, более тяжелые – жидкости, самовоспламеняющиеся на воздухе.
У боранов очень высокая теплота сгорания (у B2H6 выделяется 2025 кДж/моль, а у С2H6 – всего лишь 1425 кДж/моль). Поэтому все они и их производные испытаны в качестве ракетных топлив. Основные препятствия для такого применения – самовоспламеняемость и очень высокая токсичность.
Уникальная особенность строения боранов – многоцентровые связи. Водород в них формально двухвалентный, а бор в пента- и декаборане – пятивалентный, хотя у него, как элемента второго периода, есть только 4 орбитали (1s и 3p).
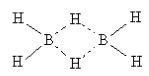
Структурная формула диборана
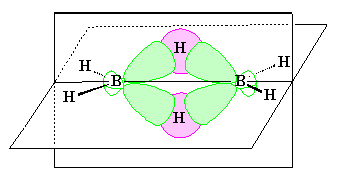
Схема распределения электронов по орбиталям в трехцентровых связях диборана [[3]]
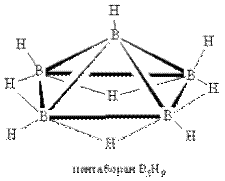
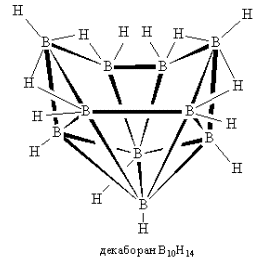
Структурные формулы из статьи М.М.Левицкого и Д.А.Леменовского
Соединения бора с азотом (1:1) оказываются аналогами углерода. Вещество состава BN (нитрид бора) существует в двух модификациях: “белый графит” и “боразон” или “эльбор”, по твердости равный алмазу. Совершенно одинаковы и соответствующие кристаллические решетки веществ, только у нитрида бора каждые два атома углерода заменены парой атомов азота и бора.
|
|
|
Боразон сохраняет свою твердость при температуре до 20000С, алмаз на воздухе сгорает при 8000С.
Особенно интересными оказались свойства соединения B3N3H6 (температура плавления -560, кипения +550С). Вещество, названное боразолом, – электронный и химический аналог бензола.
3 B2H6 + 6 NH3 ® 2 B3N3H6 + 12 H2
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 692; Нарушение авторских прав?; Мы поможем в написании вашей работы!