
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Введение. Классификация наук. Место химии в ряду естественных наук
|
|
|
|
УЧЕБНАЯ ПРОГРАММА
Классификация наук. Место химии в ряду естественных наук. Предмет химии и объекты изучения. Химическая наука - основа новых отраслей промышленности.
РАЗДЕЛ 1. Атомно-молекулярное учение
Основы атомно-молекулярного учения (атомы, молекулы, ионы). Химические элементы. Вещества. Аллотропия. Законы количественных отношений при химических превращениях. Валентность химических элементов.
Классификация сложных веществ. Оксиды, основания, кислоты, соли, их химические свойства и способы получения.
РАЗДЕЛ 2. Периодический закон Д.И. Менделеева
Систематика химических элементов: исторический аспект. Структура периодической системы Д.И. Менделеева, ее роль в открытии новых элементов.
Строение периодической системы Д.И. Менделеева: периоды, группы элементов. Развитие периодического закона в связи со строением атома: радиоактивность, ядерная модель атома Резерфорда и ее противоречия, атомные спектры.
Квантовая теория света и строение атома по Бору. Электронное облако. Квантование движения электрона в атоме. Принцип Паули. 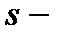 ,
, 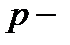 ,
, 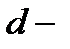 ,
, 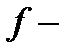 орбитали и максимальное число электронов на них.
орбитали и максимальное число электронов на них.
Распределение электронов в атомах по орбиталям. Электронная конфигурация атома и периодическая система элементов. Размеры атомов и ионов. Энергия ионизации и сродство к электрону. Строение атомного ядра, естественная и искусственная радиоактивность. Ядерные реакции.
РАЗДЕЛ 3. Химическая связь и строение молекул
Энергетический аспект образования химических связей. Ковалентная связь. Электроотрицательность атомов. Полярные и неполярные молекулы, их геометрия и свойства.
Способы образования ковалентной связи, ее насыщяемость и направленность. Гибридизация атомных орбиталей. Типы и геометрия ковалентных молекул.
|
|
|
Ионная связь, ее ненаправленность и ненасыщаемость. Поляризуемость и поляризующая способность ионов в ионных соединениях, эффективные заряды ионов. Водородная и металлическая связь. Валентность и степень окисления элементов в свете строения вещества.
РАЗДЕЛ 4. Агрегатное состояние вещества и методы исследования его строения
Агрегатные состояниявещества: газы и плазма, кристаллическое и аморфное состоянии твердых тел, жидкости. Методы исследования строения веществ.
РАЗДЕЛ 5. Основные закономерности протекания химических реакций
Гомогенные и гетерогенные химические реакции. Скорость химической реакции, ее зависимость от концентрации реагентов, их природы и температуры. Энергия активации химической реакции. Катализ.
Необратимые и обратимые реакции. Константа химического равновесия. Способы смещения химического равновесия. Принцип Ле Шателье.
Факторы, определяющие направленность химических реакций. Термодинамика химических превращений: внутренняя энергия, энтальпия, энтропия и энергия Гиббса.
РАЗДЕЛ 6. Вода. Растворы
Вода. Аномальные свойства воды. Растворы и способы выражения их состава. Насыщенные и пересыщенные растворы. Растворимость веществ в воде.
РАЗДЕЛ 7. Растворы электролитов
Электролиты и неэлектролиты. Теория электролитической диссоциации. Механизмы диссоциации электролитов. Степень электролитической диссоциации. Сила электролитов. Константа диссоциации электролитов.
Свойства электролитов с точки зрения теории электролитической диссоциации. Ионно-молекулярные уравнения химических реакций. Диссоциация воды. Водородный показатель.
РАЗДЕЛ 8. Окислительно-восстановительные реакции и основы электрохимии
Степени окисления элементов. Окислительно-восстановительные реакции. Составление уравнений окислительно-восстановительных реакций. Важнейшие восстановители и окислители.
|
|
|
Химический источник электрической энергии. Гальванический элемент Якоби - Даниэля. ЭДС гальванического элемента. Электродные потенциалы. Ряд напряжений металлов.
Электролиз. Катодные и анодные процессы. Законы электролиза. Электролиз в промышленности.
Студентам заочного факультета в I семестре изучения химии необходимо выполнить контрольную работу № 1 по общей химии.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 480; Нарушение авторских прав?; Мы поможем в написании вашей работы!