
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
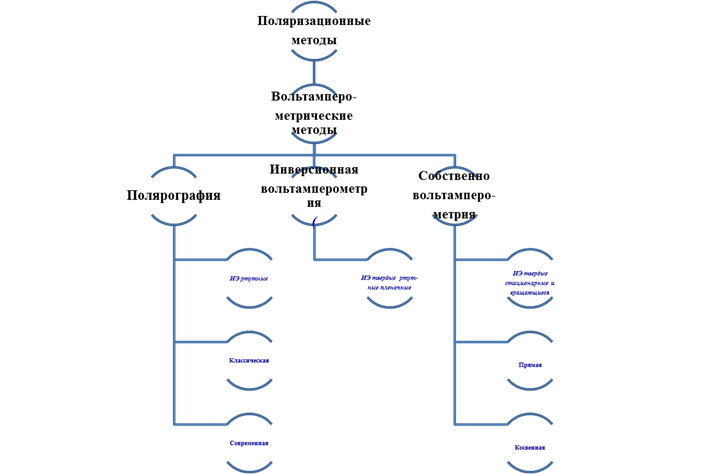
Вольтамперометрические методы
• Основаны на расшифровке поляризационных кривых (вольтамперограмм), полученных в электролитической ячейке с поляризующимся индикаторным электродом и неполяризующимся электродом сравнения.
• Вольтамперограмма дает качественную и количественную информацию о веществах, восстанавливающихся или окисляющихся на индикаторном микроэлектроде.
Для регистрации вольтамперограмм применяют двух- и трехэлектродные ячейки.
Особенность ячейки – большое различие площадей поверхности электродов.
Индикаторный микроэлектрод имеет площадь поверхности значительно меньше, чем электрод сравнения, поэтому плотность тока на нем во много раз больше. Из-за этого налагаемое извне напряжение заметно влияет на микроэлектрод и он поляризуется.
Третий электрод – вспомогательный, он служит токоотводом от индикаторного электрода, обеспечивая постоянство потенциала электрода сравнения
 |

Классическая полярография
Достоинства:
• Из-за постоянной скорости вытекания капель величина их поверхности хорошо воспроизводится.
• Периодическое обновление Hg позволяет постоянно иметь чистую поверхность электрода.
• Катод – маленькая капля Hg – плотность тока велика, это обуславливает получение хорошей полярограммы.
• Область поляризации электрода широка: (-1,2) – (-1,5) В для кислых растворов; (-2,0) – (-2,2) В для нейтральных и щелочных растворов. Это позволяет анализировать многие вещества.
• Протоны на Hg капле восстанавливаются с большим перенапряжением, поэтому можно полярографировать катионы металлов, стоящие в ряду напряжений до Н, вплоть до щелочных Ме.
Недостатки:
• Громоздкость и хрупкость конструкции.
• Капилляр может засориться.
• Hg токсична.
Внешнее напряжение, налагаемое на полярографическую ячейку, расходуется на изменение потенциала катода (Hg), потенциала анода (электрод сравнения) и преодоления сопротивления раствора (омическое падение напряжения, IR):
Е = (Еа – Ек) + IR.
То есть на поляризацию индикаторного электрода расходуется только часть налагаемого напряжения. Но при условии, что S поверхности анода во много раз больше, чем катода, поляризацией анода можно пренебречь, т.к. из-за малой плотности тока его потенциал остается практически постоянным (Еа = 0):
Е = (– Ек) + IR.
Если сопротивление раствора уменьшить, то и слагаемым IR можно пренебречь. Для снижения сопротивления в анализируемый раствор вводят избыток индифферентного электролита (или просто фона). В качестве фона пригодны различные соли щелочных и щелочноземельных Ме, растворы кислот, щелочей, буферные смеси (IR = 0). При этих условиях напряжение, подаваемое на ячейку, численно равно потенциалу индикаторного микроэлектрода:
Е = (– Ек).
Последнее позволяет при получении полярографической кривой откладывать по оси абсцисс величину подаваемого на электроды напряжения.
Нормальный вид этой кривой часто нарушается появлением острых или пологих горбов (максимумов первого или второго рода), которые могут быть обусловлены разными причинами.
Перед регистрацией полярограммы необходимо удалить из раствора растворенный кислород (растворимость 10-4 м/л), который восстанавливается на Hg электроде и мешает определению большинства веществ.
Способы удаления кислорода:
• Пропуская ток какого-либо электрохимически инертного газа (азот, гелий, аргон). Ячейка должна быть герметичной. Время удаления кислорода 15-20 минут.
• Добавление избытка сульфита натрия в виде твердой соли или насыщенного раствора. Что при этом происходит? Время удаления кислорода 5-10 минут.

· Наличие остаточного тока (АБ) обусловлено двумя причинами:
· Могут восстанавливаться легковосстанавливающиеся примеси (чаще всего это плохо удаленный кислород).
· Образование двойного электрического слоя (молекулярного конденсатора). Такой конденсатор формируется и заряжается на каждой вытекающей капле, поэтому даже в отсутствие электроактивных веществ через ячейку протекает ток – его называют конденсационным или емкостным током (IC).
· Потенциал в точке (Б) – потенциал выделения. Он отвечает началу электрохимической реакции восстановления ионов Меn+ на индикаторном электроде с образованием амальгамы:
· Меn+ + n•е + Hg0 = Ме(Hg).
· С этого момента электрод деполяризуется, т.е. рост потенциала электрода отстает от роста налагаемого внешнего напряжения.
· Вещество (катион), участвующее в электрохимической реакции и вызывающее деполяризацию электрода, называют деполяризатором. Он может быть доставлен к поверхности микроэлектрода как в результате диффузии, так и другими способами (миграция, конвекция):
Миграция ионов к катоду обусловлена действием его электрического поля.
В результате механической или тепловой конвекции раствор перемешивается, способствуя подводу деполяризатора к поверхности электрода.
Но если раствор не перемешивать, не встряхивать, поддерживать t0 – const, то можно считать, что основным способом подвода деполяризатора к поверхности электрода будет диффузия. Почему? Объяснения далее.
Участок (БВ) – здесь идет рост тока (I), достигающий в определенный момент (в точке В) максимальной постоянной величины, называемой предельным током. Потенциал в точке максимального наклона (Е½) называется потенциалом полуволны.
Участок (ВГ) – здесь сила тока (I) практически не зависит от потенциала электрода.
В этот момент электрод обладает энергией, достаточной для восстановления всех находящихся вблизи поверхности катионов деполяризатора.
При этом возникает приэлектродный слой, где концентрация деполяризатора падает практически до 0 за счет высокой скорости переноса электронов с электрода и быстрого восстановления катионов.
В результате обеднения приэлектродного слоя по сравнению с объемом раствора, где концентрация катионов равна исходной, возникает градиент концентраций, вызывающий диффузию катионов в обедненный приэлектродный слой.
Диффундирующие к поверхности электрода катионы восстанавливаются, но т.к. разность концентраций между электродным слоем и массой раствора практически не меняется из-за протекания ничтожно малых токов, предельный ток на участке (ВГ) остается постоянным.
Он остается постоянным до потенциала, когда на электроде начнется новая электрохимическая реакция с участием другого катиона-деполяризатора.
Тогда будет наблюдаться новый подъем силы тока.
Ток, обусловленный электрохимической реакцией называют фарадеевским (IF), подчеркивая его связь с процессом электролиза.
Предельный ток складывается из фарадеевского, миграционного и конвекционного токов. Поэтому, чтобы получить простую функциональную зависимость силы тока от концентрации деполяризатора, нужно устранить миграционную и конвекционную составляющие и создать условия при которых предельный ток обуславливался только диффузией деполяризатора. Сделать это не сложно:
Наличие избытка ионов фонового электролита (уменьшение миграционного тока).
Если при регистрации полярограммы раствор не перемешивать, не встряхивать, поддерживать t0 – const (исчезнут механическая и тепловая конвекции).
|
|
Дата добавления: 2014-11-29; Просмотров: 777; Нарушение авторских прав?; Мы поможем в написании вашей работы!