
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение количества белка турбидиметрическим методом с сульфосалициловой кислотой
|
|
|
|
Измерение напряжения электронными вольтметрами прямого преобразования.
Для той же формы несинусоидального периодического сигнала (форму сигнала см. в индивидуальном задании № 4) найти все его параметры по показаниям электронного вольтметра. Показания вольтметра задать самостоятельно. Задачу решить для всех вольтметров вида В3 и вольтметра вида В4 с открытым и закрытым входами.
Рекомендуемая литература
1. Новицкий П.В., Зограф И.А. Оценка погрешностей результатов измерений. – Л.: Энергоатомиздат. Ленингр. отд – ние, 1985. – 248с.
2. Селиванов М.Н., Фридман А.Э., Кудряшова Ж.Ф. Качество измерений: Метрологическая справочная книгаю – Л.: Лениздат, 1987. – 295с.
3. Рабинович С.Г. Погрешности измерений. – Л.: Энергия. 1978, - 262с.
4. Эрастов В.Е. Метрология, стандартизация и сертификация: Учеб. пособие. – Томск: Изд – во Томск. гос. Ун – та систем упр. И радиоэлектроники, 2005. – 266с.
Принцип. Сульфосалициловая кислота вызывает денатурацию белка с появлением мутности, интенсивность которой пропорциональна количеству белка.
Реактивы.
1. 3% раствор сульфосалициловой кислоты (ССК).
2. 0,9% раствор хлорида натрия.
3. Стандартный 1% раствор альбумина.
Специальное оборудование: фотоэлектроколориметр (ФЭК).
Ход исследования. В 2 пробирки (опыт и контроль) наливают по 1,25мл профильтрованной мочи. В опытную пробирку добавляют 3,75мл 3% раствора ССК, а в контрольную – 3,75 мл 0,9% раствора хлорида натрия и перемешивают содержимое пробирок. Через 5 минут измеряют оптическую плотность опытной пробы на ФЭКе при длине волны 590-650нм (светофильтр оранжевый или красный), в кювете на 5мм, против контрольной пробы.
Концентрацию белка определяют по калибровочному графику. Для построения калибровочного графика из стандартного 1% раствора альбумина готовят разведения в соответствии с таблицей 6. Из каждого полученного разведения берут 1,25мл и обрабатывают как опытные образцы.
|
|
|
Прямолинейная зависимость при построении калибровочного графика сохраняется до 1г/л. При более высокой концентрации белка мочу следует развести и учитывать разведение при расчетах.
Таблица 6
Приготовление разведений для построения калибровочного графика
| №№ | 1% раствор альбумина, мл | 0,9% раствор NaCl, мл | Концентрация белка, г/л |
| 0,05 | 9,95 | 0,05 | |
| 0,1 | 9,9 | 0,1 | |
| 0,2 | 9,8 | 0,2 | |
| 0,5 | 9,5 | 0,5 | |
| 1,0 | 9,0 | 1,0 |
Определение концентрации белка в моче с пирогаллоловым красным
Принцип. При взаимодействии белка с красителем пирогаллоловым красным образуется окрашенный комплекс, интенсивность поглощения которого на длине волны 600нм увеличивается с ростом концентрации белка в пробе.
Реактивы поставляются в наборе: раствор пирогаллолового красного и молибдата натрия в сукцинатном буфере, калибровочные растворы белка 1г/л и 0,2г/л.
Специальное оборудование: фотоэлектроколориметр или специальный фотометр МИКРОЛАБ-600 для определения концентрации белка.
Ход исследования. Приготовить пробы смешением компонентов в количестве, указанном в таблице 7.
Таблица 7
Приготовление проб
| Компоненты | Холостая проба | Калибровочная проба 1г/л | Опытная проба |
| Образец | - | - | 20мкл |
| Калибровочный раствор 1,0 г/л | - | 20мкл | - |
| Вода дистиллированная | 20мкл | - | - |
| Реагент | 1мл | 1мл | 1мл |
После смешения компонентов пробы инкубируют 15 минут при комнатной температуре. Окраска стабильна в течение 30 минут после завершения инкубирования. Измеряют оптическую плотность опытных проб и калибровочной пробы в кюветах на 1см при длине волны 600нм против холостой пробы.
Расчет ведут по формуле:
|
|
|
С = 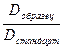 , где С – концентрация белка в пробе,
, где С – концентрация белка в пробе,
Dобразец – оптическая плотность опытной пробы,
Dстандарт – оптическая плотность калибровочной пробы.
Если результат определения более 1,9г/л, следует развести исследуемый образец в 2 или более раза дистиллированной водой, повторить тест и результат умножить на степень разведения. Если концентрация белка менее 0,07г/л и требуется уточнение результата, повторить анализ с калибровочной пробой 0,2г/л при соотношении образец/реагент=1:10.
1.2.2.2. ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ В МОЧЕ
В моче здоровых людей глюкозы практически нет, так как вся она, перешедшая с фильтратом в первичную мочу, реабсорбируется затем в почечных канальцах. Появление глюкозы в моче называется глюкозурия. Как правило, глюкозурия является следствием гипергликемии (увеличения содержания глюкозы в крови) выше 7-9 ммоль/л. Эта концентрация соответствует почечному порогудля глюкозы.
Почечный порог – это определенное содержание вещества в крови, выше которого данное вещество полностью не реабсорбируется, и часть его выделяется с мочой. Вещества, которые в нормальной моче не содержатся, а появляются в ней только после увеличения в крови выше определенного уровня, называются пороговыми.К пороговым веществам относятся глюкоза, аминокислоты, билирубин, ионы калия, фосфора. Появление пороговых веществ в моче всегда свидетельствует о патологии.
Глюкозурии делятся на инсулярные и экстраинсулярные. Инсулярные глюкозурии развиваются при недостатке в организме инсулина – гормона поджелудочной железы, который вырабатывается β-клетками островков Ларгенганса и является единственным в организме гипогликемическим гормоном, то есть гормоном, снижающим уровень глюкозы в крови. При недостатке инсулина содержание глюкозы в крови увеличивается выше почечного порога, что приводит к глюкозурии. Инсулярная глюкозурия характерна для сахарного диабета.
Экстраинсулярные глюкозурии не связаны с выработкой инсулина, а зависят от других факторов. Они могут быть физиологические (временные, у здоровых людей) и патологические (при заболеваниях). Физиологические глюкозурии появляются при чрезмерном употреблении сахара или меда – алиментарные [от лат. alimentum пища], стрессовых ситуациях (нейрогенные), приеме некоторых лекарственных препаратов (лекарственные).
|
|
|
Патологические экстраинсулярные глюкозурии могут иметь разное происхождение: гормональное, центральное, почечное. Гормональные глюкозурии, не связанные с инсулином, возникают при гиперфункции (усиленной работе) желез внутренней секреции, вырабатывающих гормоны с гипергликемическим действием:
- гипофиза (адренокортикотропный гормон – АКТГ);
- щитовидной железы (тироксин);
- надпочечников (адреналин, глюкокортикоиды).
Глюкозурии центрального происхождения выявляются при травмах и опухолях головного мозга, отравлении угарным газом, воспалительных заболеваниях мозга и мозговых оболочек (менингитах, энцефалитах), а также при кровоизлиянии в мозг.
Почечные глюкозурии обусловлены снижением почечного порога для глюкозы, то есть уменьшением способности почечных канальцев реабсорбировать глюкозу. При этом глюкоза выделяется с мочой даже при нормальном содержании ее в крови. Глюкозурии почечной природы встречаются при почечном диабете и хронических заболеваниях почек.
У больных со сморщенными почками глюкозурия может отсутствовать, несмотря на значительную гипергликемию, что зависит от уменьшения фильтрации глюкозы через склерозированные клубочки.
Таблица 8
Причины и виды глюкозурий
| Инсулярные глюкозурии | Экстраинсулярные глюкозурии | |
| Физиологические | Патологические | |
| Сахарный диабет | Алиментарные Нейрогенные Лекарственные | Гормональные Центрального происхождения Почечные |
Методы определения глюкозы в моче. Определение глюкозы является обязательным компонентом общего анализа мочи. Вначале проводят качественное определение глюкозы одним из методов:
- унифицированной пробой Гайнеса;
- с помощью тест-полосок типа «Глюкотест».
Если глюкоза в моче обнаружена, то проводят ее количественное определение унифицированными методами:
- на поляриметре. Метод основан на способности раствора глюкозы вращать поляризованный луч света вправо. В настоящее время используется редко, так как трудоемок и дает неточные результаты, если не достигнута полная прозрачность мочи;
|
|
|
- по цветной реакции с ортотолуидином;
- ферментативным глюкозооксидазным методом, который является наиболее точным и специфичным.
Количество глюкозы в моче выражается в ммоль/л. 1ммоль/л = 55,51% глюкозы.
Качественное определение глюкозы в моче пробой Гайнеса
Принцип. Метод основан на способности глюкозы восстанавливать в щелочной среде при нагревании гидрат окиси меди (синего цвета) в гидрат закиси меди (желтого цвета) и закись меди (красного цвета).
Реактивы. Реактив Гайнеса:
1) 13,3г кристаллического сульфата меди растворяют в 400мл дист. воды;
2) 50г едкого натра растворяют в 400мл дист. воды;
3) 15г глицерина растворяют в 200мл дист. воды;
4) смешивают растворы 1 и 2 и тотчас приливают раствор 3.
Получается раствор синего цвета, стойкий при хранении.
Ход исследования. К 3-4 мл реактива Гайнеса добавляют 8-12 капель мочи, содержимое пробирки перемешивают. Ставят в кипящую водяную баню на 1 минуту. При наличии глюкозы в моче содержимое пробирки приобретает оранжевый, красный или бурый цвет. Если глюкозы в моче нет, то синий цвет реактива не меняется.
Проба Гайнеса не является специфической для глюкозы. Кроме глюкозы, эту пробу дают и другие вещества, обладающие восстанавливающими свойствами (мочевая кислота, креатинин, индикан, желчные пигменты и др.).
Определение глюкозы в моче с помощью индикаторных тест-полосок типа «Глюкотест»
Принцип. Метод основан на специфическом окислении глюкозы ферментом глюкозооксидазой. Образовавшаяся при этом перекись водорода разлагается пероксидазой с выделением атомарного кислорода, который окисляет краситель с изменением его цвета.
Ход исследования. Полоску погружают в мочу, чтобы смочилась индикаторная зона. Сразу же помещают полоску на пластмассовую пластинку. Через 2 минуты читают результат, сравнивая цвет индикаторной зоны с прилагаемой шкалой.
Моча для исследования на глюкозу должна быть свежесобранной, так как при хранении глюкоза быстро разлагается микроорганизмами.
1.2.2.3. ОПРЕДЕЛЕНИЕ КЕТОНОВЫХ ТЕЛ В МОЧЕ
Кетонурия (ацетонурия) - это выделение с мочой кетоновых (ацетоновых) тел. К ацетоновым телам относятся ацетон, ацетоуксусная кислота и β-оксимасляная кислота. В моче здоровых людей они содержатся в следовых количествах и обычными качественными пробами не выявляются.
Кетоновые тела появляются в моче при сахарном диабете, голодании. При этом моча приобретает резко кислую реакцию и запах ацетона (прелых фруктов). Иногда кетонурия бывает у детей при погрешностях в питании. Это так называемая «ацетонемическая рвота», не имеющая большого диагностического значения.
Методы обнаружения кетоновых тел в моче. Определение кетоновых тел не входит в общий анализ мочи, относится к дополнительным методам химического исследования. Проводится по специальному назначению врача, а также в тех порциях мочи, в которых была обнаружена глюкоза. Кетоновые тела в моче определяют качественно или полуколичественно. Точное определение количества кетоновых тел в моче не проводится, так как они выделяются из организма не только с мочой, но и с пóтом, и с выдыхаемым воздухом.
Для определения кетоновых тел используются унифицированные методы:
- проба Ланге с нитропруссидом натрия;
- экспресс-методы (реактивные полоски, таблетки, порошок), основанные на том же принципе, что и проба Ланге.
|
|
|
|
|
Дата добавления: 2014-11-29; Просмотров: 2868; Нарушение авторских прав?; Мы поможем в написании вашей работы!