
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Аcidum boricum
|
|
|
|
Кислота борна
Сполуки бору
Цинку сульфат.
Кислота борна.
Загальна характеристика групи.
3. Натрію тетраборат.
4. Магнію сульфат.
5. Кальцію хлорид.
До Ш групи періодичної системи належать п’ять елементів: бор, алюміній, галій, індій і талій. Елементи Ш групи характеризуються наявністю на зовнішній електронній оболонці 3 електронів. З ростом атомної маси зростають металічні властивості елементів. У бору переважають неметалічні властивості; гідроксиди алюмінію, галію і талію амфотерні. З ростом атомної ваги зростає також і токсичність сполук елементів Ш групи, і тому препарати талію належать до отрут.
Сполуки галію і індію не знайшли жодного застосування в лікарській справі.
Бор розповсюджений у природі елемент. Він входить до складу багатьох мінералів у вигляді кисневих сполук.
Найважливішими мінералами бору є бура
Na2B4O7. H2O (тинкаль), борокальцит CaB4O7.4H2O.
Мінерали алюмінію широко розповсюджені у природі.
З них найважливішими є біла глина 2SiO2. AL2O3. 2H2O, кріоліт Na3ALF6. Вихідною сировиною для виготовлення лікарських засобів є тільки біла глина.
Солі алюмінию легко гідролізуються в водних розчинах з утворенням колоїдного гідроксиду. В зв’язку з цим вони мають обволікаючу, адсорбуючу та в’яжучу дію.
H3BO3 M.M. 61,83
Борну кислоту отримують із бури, обробляючи її гарячий розчин мінеральною кислотою:
Na2B4O7 + H2SO4 + 5H2O = Na2 SO4 + 4H3BO3
Властивості:
Борна кислота – безбарвні блискучі лусочки або дрібний кристалічний порошок, розчинний в 25 ч. води холодної, в 3,5 ч. води гарячої, в 25 ч. спирту та 5 ч. гліцерину. Водні розчини мають слабокислу реакцію, але солі борної кислоти невідомі. При нейтралізації кислоти утворюються тетраборати (солі кислоти H2B4O7) або метаборати (солі кислоти HBO2). При додаванні до розчину борної кислоти гліцерину або маніту (згідно ДФУ) появляється сильнокисла реакція в результаті утворення одноосновної гліцероборної кислоти:
|
|
|
CH2OH-CHOH-CH2OH + H3BO3 = CH2OH- B(CHO-CH2O)OH + 2 H2O
Ідентичність:
1. Характерною реакцією на борну кислоту є горіння її спиртових розчинів зеленим полум’ям. При цьому утворюється борноетиловий ефір:
H3BO3 + 3C2H5OH = B(OC2H5)3 + 3H2O
H3BO3 + 3CH3OH = B(OCH3)3 + 3H2O (згідно ДФУ)
Реакція проходить найкраще при наявності концентрованої сірчаної кислоти, яка зміщує реакцію вправо.
2. Куркумовий папірець, змочений розчином борної кислоти та декількома краплями хлороводневої кислоти, забарвлюється при висушуванні в рожевий або червоно-бурий колір, що переходить від розчину аміаку в зелено-чорний.
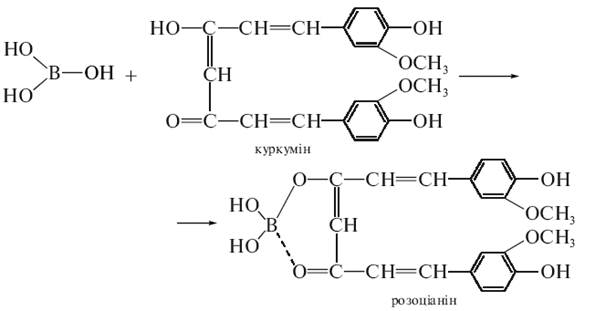
Кількісне визначення:
Метод нейтралізації, алкаліметрія, титрований розчин 0,1М гідроксиду натрію, в присутності гліцерину або маніту, індикатор фенолфталеїн, титрування проводять до появи рожевого забарвлення:

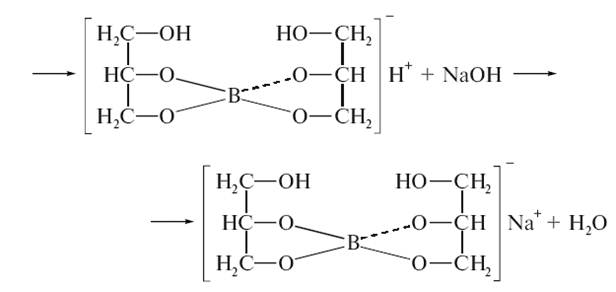
Борна кислота використовується як антисептичний засіб, у вигляді 2-3% водних розчинів для полоскання горла, в мазях та присипках. 1-2% розчини застосовуються в очній практиці.
Натрію тетраборат. Бура.
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 599; Нарушение авторских прав?; Мы поможем в написании вашей работы!