
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общее число степеней свободы
|
|
|
|
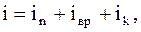 (2.8)
(2.8)
где  - число степеней свободы поступательного движения;
- число степеней свободы поступательного движения;
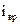 - число степеней свободы вращательного движения;
- число степеней свободы вращательного движения;
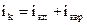 - число степеней свободы колебательного движения;
- число степеней свободы колебательного движения;
iкп - число степеней свободы колебаний точки при поступательном движении;
iквр - число степеней свободы колебаний точки при вращательном движении.
Молекулы газа имеют число степеней свободы:
а) одноатомная - i = 3 (три степени свободы поступательного движения);
б) двухатомная при упругой связи между атомами - i = 6;
в) двухатомная при жёсткой связи между атомами - i = 5;
г) трёхатомная молекула при жёсткой связи между атомами - i = 6.
Теорема о равномерном распределении энергии по степеням свободы: на любую степень свободы приходится в среднем одинаковая энергия, равная 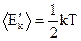 , а молекула, обладающая i степенями свободы, обладает энергией
, а молекула, обладающая i степенями свободы, обладает энергией
 (2.9)
(2.9)
где i = iп + iвр + iк.
Внутренняя энергия произвольной массы газа m складывается из энергии отдельных молекул:
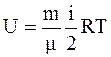 , (2.10)
, (2.10)
где m - молярная масса газа.
Теплоемкость - физическая величина, численно равная количеству теплоты, которое необходимо сообщить веществу для нагревания его на один градус.
Удельная теплоёмкость "c" - физическая величина, численно равная количеству теплоты, которое необходимо сообщить единице массы вещества для нагревания её на один градус.
Молярная теплоёмкость "C" - физическая величина, численно равная количеству теплоты, которое необходимо сообщить одному молю вещества, чтобы увеличить его температуру на один градус:
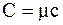 . (2.11)
. (2.11)
Удельная теплоёмкость при постоянном объеме"cv" - физическая величина, численно равная количеству теплоты, которое необходимо сообщить единице массы вещества для нагревания её на один градус в условиях постоянного объема:
|
|
|
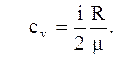 (2.12)
(2.12)
Удельная теплоёмкость при постоянном давлении "cp" - физическая величина, численно равная количеству теплоты, которое необходимо сообщить единице массы вещества для нагревания её на один градус в условиях постоянного давления:
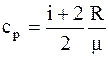 . (2.13)
. (2.13)
Молярная теплоёмкость при постоянном объеме "Cv" - физическая величина, численно равная количеству теплоты, которое необходимо сообщить одному молю вещества, чтобы увеличить его температуру на один градус в условиях постоянного объема:
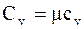 .
. 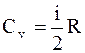 . (2.14)
. (2.14)
Молярная теплоёмкость при постоянном давлении "Cp" - физическая величина, численно равная количеству теплоты, которое необходимо сообщить одному молю вещества, чтобы увеличить его температуру на один градус в условиях постоянного давления:
 ,
, 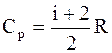 . (2.15)
. (2.15)
Отношение молярных и удельных теплоемкостей g:
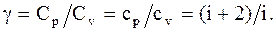 (2.16)
(2.16)
Средняя квадратичная скорость молекул ( для газа массой "m", находящегося в состоянии равновесия, при T = const) остаётся постоянной:
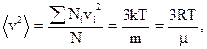 или
или  , (2.17)
, (2.17)
где Ni - число молекул, обладающих скоростью vi;
N - число всех молекул.
Наиболее вероятная скорость - скорость движения молекул, которая характеризует положение максимума функции распределения Максвелла:
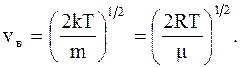 (2.18)
(2.18)
|
|
|
|
|
Дата добавления: 2014-12-07; Просмотров: 433; Нарушение авторских прав?; Мы поможем в написании вашей работы!