
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Опыт 1. Определение кислотного числа
|
|
|
|
Кислотное число — количество калия гидроксида в миллиграммах, необходимое для нейтрализации свободных кислот, содержащихся в 1 г масла. Оно показывает количество свободных кислот в исследуемом жире. По величине кислотного числа судят о доброкачественности жира. Свежий жир свободных кислот почти не содержит.
Методика
Около 10 г (точная навеска) жирного масла растворяют в 50 мл равных объемов спирта и эфира, предварительно нейтрализованного по фенолфталеину раствором калия гидроксида 0,1 моль/л. Прибавляют 3-5 капель фенолфталеина и титруют при постоянном помешивании раствором калия гидроксида 0,1 моль/л до появления розового окрашивания, не исчезающего в течение 15 с.
1 мл раствора калия гидроксида 0,1 моль/л соответствует 5,61 мг калия гидроксида.
Кислотное числоIA вычисляют по формуле:
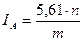 , где
, где
п — количество раствора калия гидроксида 0,1 моль/л, израсходованное на титрование, мл; т — масса навески жира, г.
Если объем раствора калия гидроксида 0,1 моль/л, пошедший на титрование, менее 2 мл, то соответствующим образом увеличивают массу навески испытуемого вещества.
Опыт 3. Определение числа омыления
Число омыления — количество калия гидроксида в миллиграммах, необходимое для нейтрализации свободных кислот и омыления сложныхэфиров, содержащихся в 1 г исследуемого жира.
Методика
Точную навеску жира (в соответствии с предложенной таблицей) смешивают в колбе вместимостью 200—250мл с 25 мл спиртового раствора калия гидроксида 0,5 моль/л.
К колбе присоединяют обратный холодильник и погружают ее в кипящую водяную баню на 30 мин, поддерживая легкое кипение. Конец омыления определяют по образованию совершенно прозрачного и однородного раствора, не изменяющегося при разведении водой. Параллельно в тех же условиях ставят контрольный опыт: в другой колбе нагревают 25 мл спиртового раствора калия гидроксида 0,5 моль/л без добавления жира.
|
|
|
К растворам сразу же после прекращения нагревания прибавляют 25 мл свежепрокипяченной горячей воды, прибавляют 5 капель раствора фенолфталеина и титруют раствором кислоты хлористоводородной 0,5 моль/л до обесцвечивания.
1 мл раствора калия гидроксида 0,5 моль/л содержит 28,05 мг калия гидроксида.
Число омыления IS вычисляют по формуле:
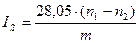 , где
, где
n1 — количество раствора кислоты хлористоводородной 0,5 моль/л, израсходованное на титрование контрольного опыта, мл; п2 — количество раствора кислоты хлористоводородной 0,5 моль/л, израсходованное на титрование испытуемого образца, мл; т — масса навески жира, г.
| Предполагаемое значение числа омыления | Масса навески Вещества (г) | ||
| 3-10 | 12-15 | ||
| 10-40 | 8-12 | ||
| 40-60 | 5-8 | ||
| 60-100 | 3-5 | ||
| 100-200 | 2,5-3 | ||
| 200-300 | 1-2 | ||
| 300-400 | 0,5-1 |
Эфирное число — количество калия гидроксида, в миллиграммах, необходимое для омыления эфиров, содержащихся в 1 г исследуемого вещества. Эфирное число IEвычисляют по формуле:
IE = IS – IA, где
IS — число омыления; IS –кислотное число.
Опыт 4. Определение йодного числа
Йодное число — количество галогена в пересчете на йод, в граммах, которое присоединяется по месту двойных связей ненасыщенных жирных кислот в 100 г испытуемого вещества в описанных условиях. Йодное число показывает содержание ненасыщенных жирных кислот в 100 г жира
Методика 1
Навеску вещества (в соответствии с предложенной таблицей) помещают в сухую колбу с притертой пробкой вместимостью 250 мл, растворяют в 15 мл хлороформа, если нет других указаний в частной статье. К полученному раствору медленно прибавляют 25 мл раствора йода бромида.
Колбу закрывают пробкой и выдерживают в темном месте при частом перемешивании в течение 30 мин, если нет других указаний в частной статье. Прибавляют 10 мл раствора 100 г/л калия йодида, 100 мл воды и титруют раствором натрия тиосульфата 0,1 моль/л при интенсивном перемешивании до светло-желтой окраски, затем прибавляют 5 мл раствора крахмала и титруют раствором натрия тиосульфата 0,1 моль/л по каплям до обесцвечивания.
|
|
|
Параллельно проводят контрольный опыт. Йодное число Ii вычисляют по формуле:
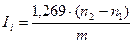 ,где
,где
n2 — количество раствора натрия тиосульфата 0,1 моль/л, израсходованное на титрование в испытуемом растворе, мл; n1 — количество раствора натрия тиосульфата 0,1 моль/л, израсходованное на титрование в контрольном опыте, мл;
т — масса навески вещества, г.
| Предполагаемое значение | Масса навески вещества, г |
| менее 20 | 1,0 |
| 20-60 | 0,5-0,25 |
| 60-100 | 0,25—0,15 |
| более 100 | 0,15—0,10 |
Опыт 4. Определение перикисного числа
Перекисное число — количество миллиэквивалентов активного кислорода, соответствующее количеству перекисей, содержащихся в 1000 г испытуемого вещества.
Если нет указаний в частной статье, используют метод А (ГФУ).
Метод А
Около 5,0 г (точная навеска) вещества помещают в коническую колбу с притертой стеклянной пробкой вместимостью 250 мл, прибавляют 30 мл смеси хлороформ— кислота уксусная ледяная (2:3). Колбу встряхивают до растворения вещества, прибавляют 0,5 мл насыщенного раствора калия йодида, перемешивают в течение 1 мин и прибавляют 30 мл воды. Полученный раствор титруют раствором натрия тиосульфата 0,01 моль/л, медленно добавляя титрант при непрерывном перемешивании почти до полного исчезновения желтой окраски. Затем прибавляют 5 мл раствора крахмала и продолжают титровать, интенсивно перемешивая до обесцвечивания раствора.
Параллельно проводят контрольный опыт.
Объем раствора натрия тиосульфата 0,01 моль/л, израсходованный на титрование в контрольном опыте, не должен превышать 0,1 мл.
Перекисное число I Р рассчитывают по формуле:
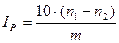 ,где
,где
n1 — объем раствора натрия тиосульфата 0,1 моль/л, израсходованный на титрование исследуемого вещества, мл; n2 — объем раствора натрия тиосульфата 0,1 моль/л, израсходованный на титрование в контрольном опыте, мл; т — масса навески вещества, г.
|
|
|
Задание 12. Определение количество неомыляемых веществ
Определите количество неомыляемых веществ в образце исследуемого масла. Произведите расчет и запишите результаты в лабораторный журнал.
Термин «неомыляемые вещества» применяется к веществам, нелетучим при температуре от 100 до 105 °С, которые экстрагируются органическим растворителем из испытуемого образца после его омыления. Содержание неомыляемых веществ вычисляется в % (мас. д.).
NB! Следует использовать стеклянную посуду со шлифами без смазки.
Методика
Навеску испытуемого вещества, указанную в частной статье, помещают в колбу вместимостью 250 мл, снабженную обратным холодильником. Прибавляют 50 мл раствора калия гидроксида спиртового 2 моль/л и нагревают на водяной бане в течение 1 ч, периодически перемешивая круговыми движениями. Затем охлаждают до температуры ниже 25 °С и содержимое колбы с помощью 100 мл воды переносят в делительную воронку. Полученный раствор осторожно встряхивают с тремя порциями эфира, свободного от пероксидов, по 100 мл каждая. Все эфирные извлечения собирают в другую делительную воронку, в которую предварительно помещают 40 мл воды, осторожно встряхивают в течение нескольких минут и оставляют до полного разделения слоев, после чего отбрасывают водный слой. Эфирный слой промывают двумя порциями воды, по 40 мл каждая. Затем тщательно отмывают поочередно 40 мл раствора 30 г/л калия гидроксида и 40 мл воды, повторяя данную процедуру 3 раза. Затем эфирный слой отмывают водой порциями по 40 мл до отсутствия щелочной реакции в водном слое по фенолфталеину. Эфирный слой количественно переносят в доведенную до постоянной массы колбу при помощи эфира, свободного от пероксидов.
Эфир отгоняют и к остатку прибавляют 6 мл ацетона. Растворитель тщательно удаляют в потоке воздуха. Остаток в колбе высушивают при температуре от 100 до 105 °С до постоянной массы, охлаждают в эксикаторе и взвешивают.
Содержание неомыляемых веществ, %, вычисляют по формуле:
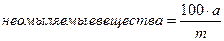 ,где
,где
а — масса остатка, г; т — масса навески вещества, г.
|
|
|
Остаток растворяют в 20 мл спирта, предварительно нейтрализованного по фенолфталеину, и титруют спиртовым раствором натрия гидроксида 0,1 моль/л. Если израсходованный объем раствора натрия гидроксида спиртового 0,1 моль/л превышает 0,2 мл, разделение двух слоев было неполным; при этом взвешенный остаток не может рассматриваться как «неомыляемые вещества». В данном случае испытание следует повторить.
Задание 13. Проведение элаидиновой пробы
Элаидиновая проба – реакция на невысыхающие масла. Олеиновая кислота под действием HNO2 переходит в стереоизомет – элаидиновую кислоту, которая при комнатной температуре имеет твердую конситенцию.
Вышеперечисленные показатели являются важнейшими показателями качества жирных масел и нормативные документы требуют проведения анализа по всем вышеперечисленным параметрам.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Дайте Определение понятию жиры, приведите общую формулу и классификацию жиров и жирных масел.
2. Охарактеризуйте кислоты, входящие в состав жиров и жирных масел.
3. Перечислите способы получения жиров и жирных масел.
4. Перечислите особенности получения касторового и миндального масел.
5. Перечислите установления подлинности жиров. Приведите примеры физических и химических методов.
6. Охарактеризуйте метод количественного определения жиров в растительных объектах.
7. Перечислите физико-химические свойства жиров и жирных масел.
8. Охарактеризуйте физические и химические показатели жирных масел, их аналитическое значение и методики определения.
9. Какие вещества относятся к сопутствующим веществам жирных масел (неомыляемому остатку жира)?
10. Перечислите невысыхающие, полувысыхающие и высыхающие жирные масла.
11. С помощью, какой реакции определяют невысыхающие жирные масла?
12. Охарактеризуйте химический состав касторового масла и льняного масел и укажите их применение.
13. Приведите пример твердого растительного жира, особенности его химической структуры и пути использования в медицинской практике.
14. Охарактеризуйте витамин F, его биологическую активность и применение.
15. Приведите примеры жиров животного происхождения, которые используются в медицинской практике.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 1817; Нарушение авторских прав?; Мы поможем в написании вашей работы!