
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Задачи для самостоятельного решения
|
|
|
|
1. При 25°С электродный потенциал серебра, погруженного в раствор b (AgNO3/ H2O) = 0,2 моль/кг равен 0,747 В. Средний коэффициент активности Ag+γ = 0.657. вычислите стандартный электродный потенциал серебряного электрода и полученную величину сравните с табличной1.
2. Потенциал никелевого электрода в растворе сульфата никеля при 25°С равен – 0,275 В. Вычислите активность ионов никеля в растворе.
3. Напишите уравнения реакций, протекающих на электродах и в элементе, и вычислите э.д.с. его при 25°С, если b (Cd (NO3)2 / H2O) = 0,2 моль/кг.
Cd | Cd (NO3)2 || KClнасыщ., Hg2Cl2 | Hg
Средний коэффициент активности иона Cd2+ равен 0,4671.
4. Напишите уравнение реакций, идущих на электродах и в элементе, и вычислите его э. д. с. при 25°С, если b (AgNO3/H2O) = 0,01 моль/кг.
Hg | Hg2Cl2, KClнасыщ. | AgNO3 | Ag
По ионной силе раствора найдите в справочной таблице коэффициент активности Ag+1.
5. Вычислите э. д. с. элемента при 25°С:
Mn | MnCl2 (а 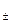 = 0,0005) || AgNO3 (а
= 0,0005) || AgNO3 (а 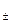 = 0,005) | Ag.
= 0,005) | Ag.
Напишите уравнения реакций, протекающих на электродах и в элементе.
6. По величинам стандартных электродных потенциалов установите, могут ли самопроизвольно при 25°С в водном растворе протекать следующие реакции:
а) FeCl2 + Sn → SnCl2 + Fe;
б) Cu (NO3)2 + 2Ag → 2AgNO3 + Cu;
в) 2FeCl3 + SnCl2 → 2FeCl2 + SnCl4;
г) KMnO4 + 2KCl → K2MnO4 + Cl2(водн)
Если данная реакция неосуществима, запишите уравнение самопроизвольного протекающей реакции. Составьте элементы, в которых протекают эти реакции. Вычислите константы равновесия самопроизвольно протекающих реакциях.
7. Вычислите значение диффузионного потенциала при 25°С, возникающего на границе соприкосновения двух растворов хлорида лития, моляльность которых 0,01 и 0,001 моль/кг. Средние коэффициенты активности ионов в общих растворов считать равными единице. Подвижности ионов Li+ и Cl- равны соответственно 38,7 и 76,3 См ∙ см2/моль. Определите, какой из растворов зарядится положительно.
|
|
|
8. Вычислите э. д. с. элемента (при 25°С):
Cd | CdSO4 (а 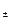 = 0,05) || CdSO4 (а
= 0,05) || CdSO4 (а 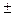 = 0,5) | Cd.
= 0,5) | Cd.
Напишите уравнение электродных реакций и суммарное уравнение. За счет какого процесса возникает электродвижущая сила в элементе?
9. Вычислите э. д. с. элемента (при 25°С):
Ag / AgNO3 (а 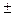 = 0,01) | AgNO3 (а
= 0,01) | AgNO3 (а 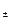 = 0,1) | Ag,
= 0,1) | Ag,
1) пренебрегая диффузионным потенциалом и
2) учитывая диффузионный потенциал.
Подвижность ионов Ag+ и NO 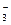 равны соответственно 61,9 и 71,4 См ∙ см2/моль.
равны соответственно 61,9 и 71,4 См ∙ см2/моль.
10. Вычислите э. д. с. элемента (при 25°С):
Zn | ZnSO4 (а+ = 0,001) | ZnSO4 (а 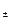 = 0,01) | Zn,
= 0,01) | Zn,
учитывая диффузионный потенциал. Подвижность ионов 1/2 Zn2+ и ½ SO 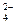 равны соответственно 53,5 и 79,8 См ∙ см2/моль.
равны соответственно 53,5 и 79,8 См ∙ см2/моль.
11. При 25°С э. д. с. элемента
Ag | CH3COOAg || AgNO3 | Ag
равна 0,013 В. Моляльность раствора AgNO3 0,1 моль/кг, а средний коэффициент активности ионов Ag+ в этом растворе равен 0,734. Вычислите активность ионов Ag+ в растворе ацетата серебра.
12. Э. д. с. элемента
Ag | AgBr, KBr (а 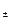 = 0,085)||AgNO3 (а+ = 0,072)| Ag
= 0,085)||AgNO3 (а+ = 0,072)| Ag
при 25°С равна 0,602 В. Вычислите произведение растворимости и растворимость AgBr.
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 901; Нарушение авторских прав?; Мы поможем в написании вашей работы!