
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Кельвина
|
|
|
|
Термодинамическая вероятность W состояния тела или системы
— это число способов, которыми может быть реализовано данное конкретное термодинамическое состояние (макросостояние). Иначе говоря, это число всевозможных микрораспределений частиц по координатам и скоростям (микросостояний), которыми может быть осуществлено данное макросостояние.
Формула Больцмана: S = k∙lnW
где k — постоянная Больцмана.
Энтропия системы определяется логарифмом числа микросостояний, с помощью которых может быть реализовано данное макросостояние.
Энтропия является мерой неупорядоченности системы, — чем больше число микросостояний, реализующих данное макросостояние, тем больше энтропия.
17. Принцип возрастания энтропии.
все процессы в замкнутой системе ведут к увеличению её энтропии. В замкнутой системе идут в направлении от менее вероятных состояний к более вероятным, до тех пор, пока вероятность состояния не станет максимальной.
В состоянии равновесия — наиболее вероятного состояния системы — число микросостояний максимально, при этом максимальна и энтропия.
18. Второе начало термодинамики
Любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает (закон возрастания энтропии).
Первое начало термодинамики выражает закон сохранения и превращения энергии применительно к термодинамическим процессам.
Второе начало термодинамики определяет направление протекания термодинамических процессов, указывая, какие процессы в природе возможны, а какие — нет.
Существуют ещё двеформулировки второго начала термодинамики, эквивалентных закону возрастания энтропии:
1) по Кельвину: невозможен круговой процесс, единственным
результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
|
|
|
2) по Клаузиусу: невозможен круговой процесс, единственным
результатом которого является передача теплоты от менее нагретого тела к телу более нагретому.
19. Третье начало термодинамики.
Третье начало термодинамики — теорема Нернста-Планка — постулирует поведение термодинамических систем при нуле Кельвина (абсолютном нуле):
Теплоемкости Cv и Ср при Т = 0К равны нулю, поскольку:
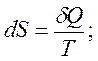

 ;
; 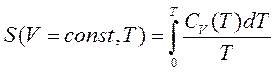
_______________________
Далее – тепловые машины и холодильники
20. Тепловые двигатели и холодильные машины
Тепловой двигатель — это периодически действующий двигатель, совершающий работу за счет полученной извне теплоты.
Термостатом называется термодинамическая система, которая может обмениваться теплотой с телами практически без изменения собственной температуры.
Рабочее тело — это тело, совершающее круговой процесс и обменивающееся энергией с другими телами.
Принцип работы теплового двигателя: от термостата с более высокой температурой Τ1, называемого нагревателем, за цикл отнимается количество теплоты Q1, а термостату с более низкой температурой Т2, называемому холодильником, за цикл передается количество теплоты Q2. При этом совершается работа А = Q1 - Q2.

Термический КПД двигателя:
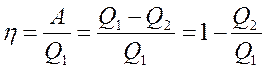
Чтобы КПД был равен 1, необходимо, чтобы Q2 = 0, а это запрещено вторым началом термодинамики.
Процесс, обратный происходящему в тепловом двигателе, используется в холодильной машине: от термостата с более низкой температурой Т2 за цикл отнимается количество теплоты Q2 и отдается термостату с более высокой температурой Т1>Т1. При этом Q = Ql - Q2 = А или Ql = Q2 + А
Количество теплоты Q1, отданное системой термостату T1, больше количества теплоты Q2, полученного от термостата Т2 на величину работы, совершенной над системой.
|
|
|
Эффективность холодильной машины характеризует холодильный коэффициент η' — отношение отнятой от термостата с более низкой температурой количества теплоты Q2 к работе А, которая затрачивается на приведение холодильной машины в действие:
21. Теорема Карно
Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей Τ1 и холодильников Т2, наибольшим КПД обладают обратимые машины.
При этом КПД обратимых машин, работающих при одинаковых температурах нагревателей и холодильников, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника.
22. Цикл Карно
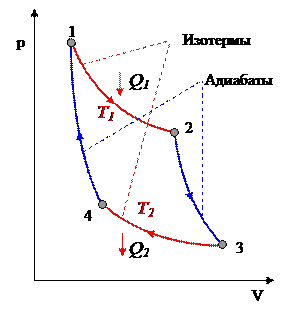
Наиболее экономичный обратимый круговой процесс, состоящий из двух изотерм и двух адиабат.
Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Последовательные термодинамические процессы в цикле Карно:
1 – изотерма – 2 – адиабата – 3 – изотерма – 4 – адиабата – 1
| Изотермическое расширение 1 – 2 T = const; V2 > V1 | 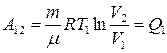
|
| Адиабатическое расширение 2 – 3 δQ = 0; T2 < T1 | 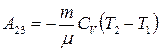
|
| Изотермическое сжатие 3 – 4 T = const; V4 < V3 | 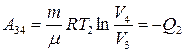
|
| Адиабатическое сжатие 4 – 1 δQ = 0; T1 > T2 | 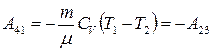
|
Работа, совершаемая в результате кругового процесса:
A = A12 + A23 + A34 + A41 = Q1 + A23 – Q2 – A23 = Q1 – Q2
Для адиабат 2 – 3 и 4 – 1 уравнения Пуассона:
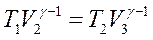 ;
; 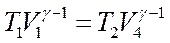 , откуда V1/V2 = V3/V4,
, откуда V1/V2 = V3/V4,
Используя это, определим термический КПД цикла Карно:
 ,
,
который действительно определяется только температурами нагревателя и холодильника.
___________________________
Конец 2-й лекции
Конец молекулярке
|
|
|
|
|
Дата добавления: 2014-12-27; Просмотров: 1919; Нарушение авторских прав?; Мы поможем в написании вашей работы!