
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет рН растворов слабых кислот
|
|
|
|
Если степень диссоциации кислоты мала (h < 5%), то можно полагать, что равновесная концентрация недиссоциированнои кислоты равна ее общей концентрации. Тогда
 (2-4)
(2-4)
Если h > 5%, необходимо учитывать, что [НА] ≠СНА и поэтому
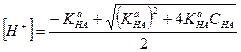 (2-5)
(2-5)
ПРИМЕР 6. Рассчитайте рН 0.10 М раствора уксусной кислоты.
Решение. Поскольку в 0.10 М растворе уксусной кислоты степень диссоциации СН3СООН h < 5% (табличные данные), то в хорошем приближении
[СН3СООН] = С(СН3СООН) = 0.10 М

ПРИМЕР 7. Рассчитайте рН 0.10 М раствора фосфорной кислоты.
Решение. Поскольку константы диссоциации фосфорной кислоты по стадиям значительно различаются (7.08·10-3; 6.17·10-8; 4.68·10-13), то можно пренебречь диссоциацией по второй и третьей стадиям.
Оценим степень диссоциации фосфорной кислоты при концентрации 0.10 М:
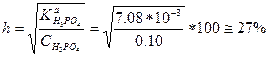
Следовательно, [Н3РО4] ≠ С(Н3РО4) и п о формуле (2-5)
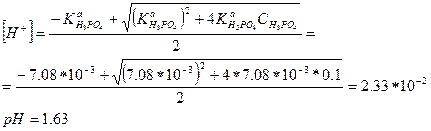
В разбавленных растворах (C < 1·10-4 М) кислот с Ка НА < 1·10-6 диссоциацией растворителя пренебрегать нельзя. Запишем уравнение электронейтральности
[Н+] = [А-] + [ОН-]
Выразим [А-] и [ОН-] через КаНА и Kw соответственно
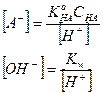
Решим это уравнение относительно Н+:
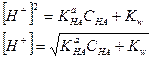 (2-6)
(2-6)
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 2158; Нарушение авторских прав?; Мы поможем в написании вашей работы!