
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фугитивность
|
|
|
|
Фугитивность - это давление реального газа, свойства которого выражены уравнением состояния идеального газа. Фугитивностью пользуются при расчетах равновесных паровой и жидкой фаз и числовых значений констант фазового равновесия.
Для равновесной системы, согласно законам Рауля и Дальтона,
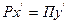 (34)
(34)
откуда
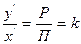
где Р - давление насыщенных паров чистого компонента, Па; х' - мольная концентрация компонента в жидкой фазе, %, мол; П - давление в системе, Па; у' - мольная концентрация компонента в паровой фазе, %, мол; k - константа фазового равновесия (Приложения 10 и 11).
Для идеальной системы значение k равно отношению давления насыщенных паров данного компонента к давлению в системе и характеризует распределение данного компонента между паровой и жидкой фазами. Для реальных систем константа фазового равновесия, вычисленная этим методом, не дает вполне удовлетворительных результатов.
Для реальных газов и растворов давление насыщенных паров Р и давление в системе П заменяют соответственно фугитивностью жидкости 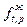 и паров
и паров 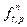 . Уравнение (34) приобретает вид
. Уравнение (34) приобретает вид
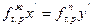
а константа фазового равновесия равна
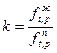 (35)
(35)
Фугитивность характеризует степень отклонения свойств реального газа от идеального в случае изотермического процесса. При низких давлениях и высоких температурах реальный газ приближается к состоянию идеального газа, а величина f - к величине Р. Фугитивность имеет ту же размерность, что и давление. Отношение фугитивности к давлению называется коэффициентом активности
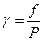 (36)
(36)
Для идеального газа 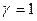 .
.
Установлено, что коэффициент активности является функцией приведенных температуры и давления. Поэтому значение фугитивности можно определить, пользуясь графиком (рис. 9). По приведенной температуре Тпр и приведенному давлению Рпр находят коэффициент активности. Затем, подставляя в уравнение (36) давление насыщенных паров Р или давление системы П, получают соответственно фугитивность жидкости или паров.
|
|
|
Для точных расчетов константы фазового равновесия, когда жидкий компонент находится не под давлением Р своих насыщенных паров, а под любым другим давлением, фугитивность этого компонента в жидкой фазе находят по формуле
 (37)
(37)
где 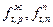 - фугитивность жидкости при давлении в системе П и давлении насыщенных паров Р соответственно, Па; Vж - мольный объем компонента, л/моль, м3/кмоль; П - давление в системе, Па; Р - давление насыщенных паров чистого компонента, Па; R - универсальная газовая постоянная, КДж/(кмоль×К); Т - температура системы, К.
- фугитивность жидкости при давлении в системе П и давлении насыщенных паров Р соответственно, Па; Vж - мольный объем компонента, л/моль, м3/кмоль; П - давление в системе, Па; Р - давление насыщенных паров чистого компонента, Па; R - универсальная газовая постоянная, КДж/(кмоль×К); Т - температура системы, К.
Пример 15. Определить фугитивность паров узкой бензиновой фракции (М = 100), находящейся при 400°С и 4,55 МПа. Критические параметры фракции tкр = 321°С и Ркр = 3,72 МПа.
Решение. Находим значения приведенных температуры и давления
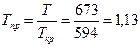

На рис. 9 по вычисленным Тпр и Рпр находим, что коэффициент активности 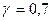 . Полученные данные подставляем в уравнение (34). Фугитивность паров узкой бензиновой фракции при 400°С и 4,55 МПа равна
. Полученные данные подставляем в уравнение (34). Фугитивность паров узкой бензиновой фракции при 400°С и 4,55 МПа равна
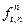 = 4, 55×0,7 = 3,181 МПа
= 4, 55×0,7 = 3,181 МПа 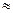 3,2 МПа
3,2 МПа
Пример 16. Рассчитать константу фазового равновесия k для н -гексана при 180°С и 784 кПа. Критические параметры tкр = 234,7°С, Ркр = 2932 кПа. Давление насыщенных паров Р = 1252кПа.
Решение. Приведенные температура и давление равны
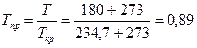
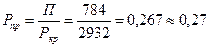
На рис. 9 для Tпр = 0,89 и Рпр = 0,27 находим коэффициент активности 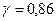 ; фугитивность паров н -гексана
; фугитивность паров н -гексана
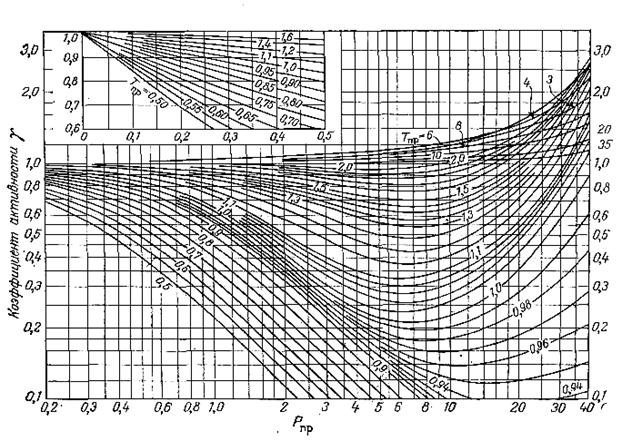
Рис. 9. График для определения коэффициента активности g
при известных приведенных температуре и давлении
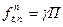 = 0,86 × 784 = 674 кПа
= 0,86 × 784 = 674 кПа
Определяем фугитивность жидкого н -гексана при 180oC, давлении собственных насыщенных паров Р = 1252 кПа. Приведенное давление равно
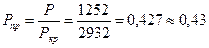
Для значения Tпр = 0,89 и Рпр = 0,43 по графику (рис. 9) находим коэффициент активности 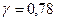 . Фугитивность жидкого н -гексана, находящегося при температуре t и под давлением собственных насыщенных паров Р, равна фугитивности его же паров при тех же условиях, т. е.:
. Фугитивность жидкого н -гексана, находящегося при температуре t и под давлением собственных насыщенных паров Р, равна фугитивности его же паров при тех же условиях, т. е.:
|
|
|
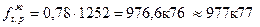
Константа фазового равновесия равна
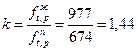
Задача 22. Определить фугитивность паров узкой бензиновой фракции (М = 1000, находящейся при t0 и Р0. Критические параметры фракции tкр и Ркр
| параметры | Варианты | |||||||||
| t00С | ||||||||||
| Р0 МПа | 4,5 | 5,5 | 6,5 | 7,5 | 8,5 | |||||
| tкр0С | ||||||||||
| Ркр МПа | 3,2 | 3,4 | 3,6 | 3,8 | 4,2 | 4,4 | 4,6 | 4,8 |
Задача 23. Рассчитать константу фазового равновесия k для углеводорода при t0 и Р0. Критические параметры tкр и Ркр. Давление насыщенных паров р.
| параметры | Варианты | |||||||||
| t00С | ||||||||||
| Р0 кПа | ||||||||||
| tкр0С | ||||||||||
| Ркр кПа | ||||||||||
| р кПа |
|
|
|
|
|
Дата добавления: 2014-12-24; Просмотров: 2861; Нарушение авторских прав?; Мы поможем в написании вашей работы!