
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Атты дене деген не?
ПРИБОРЫ. МАТЕРИАЛЫ, ОБОРУДОВАНИЕ
В соответствии с требованиями ФГОС ВПО 3 вузы располагать специализированными кабинетами, лабораториями: для преподавания уголовного права используется кабинет уголовного права и процесса.
В учебном процессе по дисциплине используется образовательный сервер Смоленского государственного университета, где размещаются материалы по преподаваемой дисциплине. Студентами может быть использован программный комплекс на образовательном сервере, включая различные варианты контроля знаний, информационно-справочные системы: БД нормативно-правовой информации НТЦ «Система», «Гарант», «Консультант-плюс», комплекс энциклопедий «Рубрикон». Преподаватели кафедры и студенты имеют выход в международные и российские информационные сети (Интернет – 24 часа по выделенной линии).
В процессе занятия используются современные компьютеры для проведения тестирования, проведения лекционных занятий по уголовному праву демонстрирования презентаций, самостоятельной работы с использованием образовательного сервера.
[1] На сайте: http://www.ast-centre.ru/ast/test можно протестировать себя на остаточные знания по уголовному праву.
[2] На сайте: http://www.ast-centre.ru/ast/test можно протестировать себя на остаточные знания по уголовному праву.
[3] На сайте: http://www.ast-centre.ru/ast/test можно протестировать себя на остаточные знания по уголовному праву.
Атомдары немесе молекулалары реттелiп орналасқан және периодты түрде қайталанып тұратын iшкi структурасын түзетiн қатты денелер кристаллдар деп аталады. Кристалдардың қырлары әрқашан жазық және дұрыс геометриялық пiшiндi болып келедi. Бөлшектердiң орналасуының салыстырмалы түрде орныққан скелетi кристалдық торлар деп аталады, ал сол торлардың орналасқан орындары түйiндер деп аталады
Кристалдардың сыртқы пiшiнiнiң дұрыстығы - олардың реттелген құрылысының бiр ғана салдары емес. Олардың ең басты ерекшелiгi кристалдың физикалық қасиеттерiнiң ондағы таңдалған бағытына байланыстылығында. Кристалдардың бұл қасиетi анизотропия деп аталады.
Барлық кристалды денелер анизотропты болып келедi. Анизотропияның бiр себебi - кристалдық тор түйiндерiнiң тығыздығы әр түрлi бағытта әр түрлi болған жағдайдағы, бөлшектердiң дұрыс ретпен орналасуы. Осы бағыттардағы бөлшектердiң өзара әсерi де бiрдей болмайды. Бұдан, әр түрлi бағыттардағы кисталдардың механикалық берiктiгi әр түрлi екендiгi шығады.
Көптеген кристалдар жылу мен электр тогын әр бағытта әр-түрлi өткiзедi. Кристаллдың оптикалық қасиеттерi де оның бағытына байланысты болуы мүмкiн.
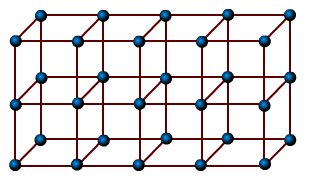
|
| 2.9-сурет |
Белгiлi бiр температураға дейiн қыздырғанда (әр заттың өз температурасы бар) зат қатты кристалдық күйден сұйық күйге өтедi. Осы процесс балқу деп аталады, ал балқуға ұшырататын температура балқу температурасы деп
6. Кристалдар. Өзінің формасын да, көлемін де сақтайтын затты қатты дене деп атайтынымыз Ұқсастықтары және айырмашылықтары. Физикада қатты дене деп тек кристалл денелерді айтады. Аморфты денелердің сырт қарағанда көлемін және пішінін сақтауы оларды қатты дене етіп көрсеткенімен, бұл денелер өте тұтқыр сұйық деп қарастырылады. Температура жоғарылаған сайын олардың сұйыққа тән қасиеттері бірден көріне бастайды, бірте-бірте еріп, сүйықтың барлық қасиеттеріне ие болады.
Аморфты денелер – изотропты. Кристалдың қасиеттері әр түрлі бағыттарда түрліше болады. Кристалдар – анизотропты.
Аморфты денелер. Атомдарының ретті орналасуы алыс қашықтықтарда да қайталанып отыруымен сипатталатын кристалдық денелерден аморфты денелердің айырмашылығы, мұнда тек жуық тәртіп қана орын алады. Кейбір заттар кристалл және аморфтық түрде де бола алады.
Кристалдар. Өзінің формасын да, көлемін де сақтайтын затты қатты дене деп атайтынымыз белгілі. Бірақ бұлар заттың қатты күйін тек сыртқы түріне қарап қана сипаттайды. Физикалық тұрғыдан алғанда біз бұл белгілеріне қарап қатты күйді сұйық күйден айыра аламыз.
Кристалдардың ішкі құрылымсын рентген сәулелерінің көмегімен зерттеулер олардағы бөлшектердің (молекулалар, атомдар және иондардың) дұрыс орналасатынын көрсетті, яғни олар кристалдық (кеңістіктік) тор түзейді. Кристалдық тордағы қатты дененің бөлшектерінің ең орнықты тепе-теңдік қалпына сәйкес нүктелері тордың түйіндері деп аталады.
Кеңістіктік тор. Криталдағы бөлшектердің дұрыс орналасуын кристалдардың кейбір қасиеттерінің бағытқа тәуелділігі, яғни анизотропиясы шығады.
Анизотропия қасиетінің тек монокристалдарға ғана тән болатындығын да айта кетейік. Қатты денелердің көпшілігінің құрылымы поликристалды (грек. поли - көп), яғни микроскоппен ғана көруге болатын өте ұсақ кристалдардың жиынтығынан тұрады. Поликристалды денелер мен аморфты денелердің айырмашылығы мынада: поликристалдық денелердің анизотропия байқалатын өте кішкентай бөлігін бөліп алуға болады, ал аморфты денелердің кез-келген бөлігін қарастырсақ та, ол әрқашан изотропты.
Кристалдық құрылымдардың түрлері. Кристалдардың әр түрлі типтерін және кристалдық торда орналасу мүмкіндіктерін кристаллография зерттейді. Кристал торының түйіндерінде орналасқан бөлшектер арасында әрекет ететін күштердің сипаты бойынша кристалдық құрылымдарды төрт түрге бөледі: иондық, атомдық, молекулалық және металдық.
Тор түйіндерінде бейтарап атомдардың болуымен сипатталатын құрылым, атомдық кристалдық құрылым деп аталады. Олар коваленттік байланысқан. Коваленттік байланыс деп іргелес орналасқан екі атомның өзара екі валенттік электрондар алмасуы кезінде туатын тартылыс күшінің салдарынан пайда болатын байланысты атайды.
3.Құрылымына байланысты қатты денелерінің топтастыру.
Кристалдык тордың түйінінде орналасқан бөлшектердің шығу табиғатына,олардың бір-бірімен әсерлесуіне қарай және құрылымына қарай қатты заттарды 4 топқа бөледі:
1.Иондық кристаллдар.Кристалдық тордың түйіндерінде таңбалары қарама-қарсы иондар орналасады.Олардың арасындағы өзара әрекеттесуші күштер көбінесе электростатикалық болып келеді. Осы айтылған күшпен әрекеттескен болса ол иондық байланыс болып табылады.Қарапайым мысал ретінде ас тұзын алсақ болады NaCl. Иондық кристал молекуладан емес иондардан тұрады. Және осы кристалды толығымен бір үлкен молекула ретінде қарастырса болады.
2. Атомды кристалдар. Кристалдық торлардың түйіндеріне бейтарап атомдар орналасады.Оларды біріктіретін байланыс ковалентті деп аталады.Ковалентті байланыс тек электрон жұптарымен жүзеге асады.Демек,бұл байланыс әр атомнан бір бір электроннан алынған кезде пайда болады, бірақ электрон тек қана валенттік электрон болуы тиіс.Атомды кристалдардың ең қарапайым мысалы ретінде алмас пен графитті алуға болады.
3.Металдық крмсталдар. Кристалдық тордың әр түйінінде оң зарядталған металдық ион орналасады. Олардың арасында электрондар газдың молекуласындағыдай хаосты түрде қозғалады,ионның пайда болу әсерінен атомнан бөлініп кеткендіктен.Оң зарядталған иондарды ұстап тұрғандықтан осы электрондер цементтің рөлін ойнайды,әйтпегенде кристалдық торымыз иондардың тебілуі нәтижесінде қирап қалар еді. Оған қоса иондарда электрондарды кристалдық тордан шығармай ұстап тұрады. 4. Молекулалық кристаллдар.Кристалдық тордың түйінінде белгілі бір тағайындалып қойған молекулалар орналасады.Кристалдағы молекулалардың байланысу күші Вандер-Ваальстік деп аталады. Бұған қарапайым мысал ретінде ұарапайым мұзды немесе сухой ледты алуга болады.
|
Дата добавления: 2014-12-25; Просмотров: 1253; Нарушение авторских прав?; Мы поможем в написании вашей работы!