
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Критическая температура и критическое давление многокомпонентных углеводородных смесей
 |
Эти параметры многокомпонентных углеводородных смесей относятся к числу основных, характеризующих их объемное и фазовое поведение. По значению критического давления и температуры углеводородной смеси можно судить о фазовом состоянии ее при различных р и t. Критические параметры широко используются при расчетах сжижения и компрессии углеводородных смесей, а также при выборе их для закачки в пласт с целью увеличения нефтеотдачи и т. д.
Ранее отмечалось, что критические параметры даже простейших бинарных смесей метана с более тяжелыми углеводородами в широком диапазоне изменяются в зависимости от состава. При изменении количественного соотношения компонентов, как было показано на рис. 4, б критические точки различных смесей С1, С2, С3 и т. д. образуют кривую, которую принято называть огибающей критических точек системы (или критической кривой). Имеется достаточно экспериментальных данных о критических параметрах лишь простых компонентов, по которым можно построить огибающие критических точек этих простых систем. Для сложных многокомпонентных смесей построение таких огибающих сильно осложняется из-за недостатка данных о значениях критических параметров чрезвычайно широкого многообразия смесей, которые встречаются на практике. Поэтому критические параметры сложных смесей обычно определяют расчетным способом.
Г. С. Степановой, например, предложен следующий способ оценки параметров в критической точке многокомпонентных систем. Сложная углеводородная смесь условно приводится к бинарной системе, одним из компонентов которой является метан, а вторым — все остальные компоненты (С2+высшие). Далее для определения критических параметров этой условной бинарной системы используются известные свойства истинных бинарных смесей метана с индивидуальными парафиновыми углеводородами. На рис. 13 и 14 приведены критические кривые (геометрическое место или траектории критических точек) бинарных смесей метана с парафиновыми и другими углеводородами и азотом, а также бинарной смеси азот — этан. Как следует из рис. 13, характер траектории критических точек для различных углеводородов одинаковый. Левая точка со знаком СН4 соответствует критическим параметрам чистого метана. Каждая кривая справа оканчивается точкой соответствующей критическим параметрам второго более тяжелого углеводорода. Между ними находятся критические точки смесей с различным содержанием метана и второго компонента. Во всех случаях критическое давление в системе вначале по мере увеличения в смеси количества более тяжелого углеводорода возрастает и, достигнув максимума, уменьшается. При этом с увеличением молекулярной массы тяжелого компонента критическое давление при одной и той же температуре также возрастает и по существу характер кривой (или точнее сказать ее расположение) определяется критическими параметрами второго компонента. (Несколько иной характер имеют критические кривые ароматических углеводородов (рис. 14) - они пересекаются с другими кривыми.) Это означает, что по молекулярной массе второй тяжелой части системы можно определить кривую критических точек, соответствующую данной смеси. Но при этом следует учитывать, что изопарафиновые и нафтеновые углеводороды при одинаковой молекулярной массе с их нормальными аналогами имеют критические параметры, отличные от критического давления и температуры нормальных парафиновых углеводородов. Поэтому критические кривые изопарафинов приходится рассматривать как бы принадлежащими углеводородам нормального строения, но с другой фиктивной (или эквивалентной) молекулярной массой. Например, из рис. 14 следует, что кривая смеси метана с изобутаном (молекулярная масса 58,12) расположена на месте огибающей критических точек смеси метана с фиктивным парафиновым углеводородом, молекулярная масса которого должна бы быть равной приблизительно 48. Эта величина и принимается за эквивалентную молекулярную массу изобутана. Г. С. Степановой построены диаграммы, позволяющие быстро установить фиктивные молекулярные массы наиболее часто встречающихся в составах конденсатов изопарафиновых, парафиновых и ароматических углеводородов1. Очевидно, что эквивалентная масса парафиновых углеводородов равна их действительной молекулярной массе.
|
|
|
|
|
|
Если смесь многокомпонентная, то по методу Г. С. Степановой сначала определяется средняя эквивалентная молекулярная масса сложного компонента С2 + высшие, которую можно найти по формуле:
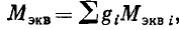
где gi - массовые концентрации углеводородов, входящих в состав второго компонента;
Мэкв i - их эквивалентные молекулярные массы.
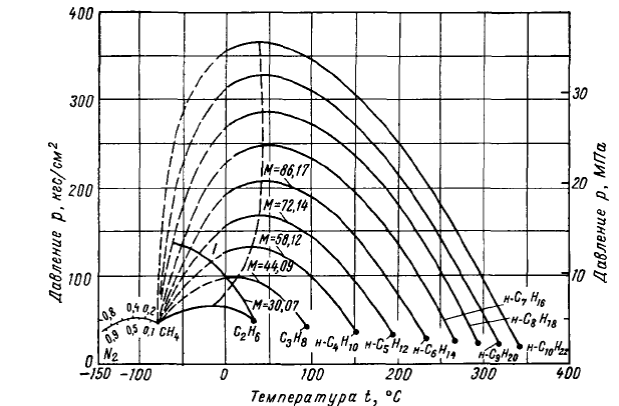
Рис. 13. Критические кривые бинарных смесей метана с парафиновыми углеводородами и азотом.
1 - критическая кривая смеси азот - этан (по Г. С. Степановой).
По значениям эквивалентной молекулярной массы Мэкв на рис. 13 наносится критическая кривая исследуемой смеси (положение ее определяется простой интерполяцией). На этой кривой и будет лежать критическая точка углеводородной смеси. Конкретное ее положение зависит от критической температуры Ткр смеси.
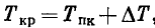
где Тпк — псевдокритическая температура,
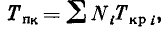
Д Т — поправка на разность между истинной критической и псевдокритической температурами, устанавливаемая по экспериментальным данным;
Ni — мольные концентрации входящих в смесь компонентов;
Tкр i— критические температуры компонентов.
______________
Степанова Г.С. Метод определения давления схождения констант ta3OBoro равновесия многокомпонентных углеводородных смесей. Труды Азерайджанского индустр. ин-та, вып. 16, Баку, Азнефтеиздат, 1957.
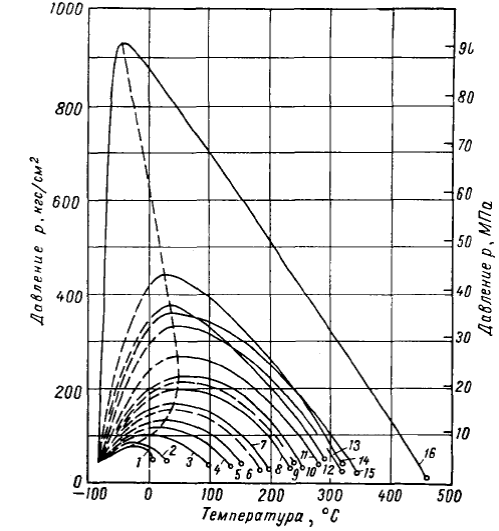
Рис. 14. Критические кривые бинарных систем (по Г. С. Степановой).
1 — метан — этилен; 2 — метан — этан; 3 — метан — пропан; 4 — метан — изобутан;
s — метан — н-бутан; б — метан — циклобутан; 7 — метан — пентан; 8 — метан — гек-
|
|
|
сан- 9 — метан — циклопентан; 10 — метан — изогептан; 11 — метан — циклогексав;
12 метан — бензол; 13 — метан — нонан; 14 — метан — толуол; 15 — метан — декан;
16 — метан — легкая нефть.
Необходимость учета поправки Д Т возникает в связи с отклонением величины псевдокритической температуры углеводородов от истинной критической температуры. С увеличением молекулярной массы углеводорода, составляющего смесь с метаном, отклонение истинной критической температуры от псевдокритической возрастает.
На рис. 15 приведена зависимость разности между критической и псевдокритической температуры от мольного содержания метана в смеси, построенная по данным, опубликованным в литературе об истинных значениях Ткр различных смесей. При определении критической температуры в качестве характеристики состава второго сложного компонента следует пользоваться средней (кажущейся) молекулярной массой М, которая рассчитывается по известной мольнойконцентрации входящих в смесь компонентов
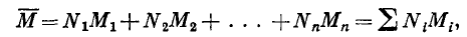
где Mi - относительные молекулярные массы соответствующих компонентов.
В итоге критическая температура многокомпонентных углеводородных смесей по методике Г. С. Степановой определяется в следующей последовательности:
1) вычисляется псевдокритическая температура смеси по формуле (8);
2) разделив смесь условно на два компонента (метан и С2 + высшие), рассчитывают молекулярную массу сложного компонента по формуле (9) (азот относят к первому компоненту системы);
3) используя графики на рис. 15, определяют отклонение истинной критической температуры от псевдокритической Д Т (по мольному содержанию в смеси второго сложного компонента С2 + высшие и его молекулярной массе М). При несовпадении значений вычисленной молекулярной массы М с указанными на графиках рис. 15 значения AT определяются простой интерполяцией по молекулярной массе второго сложного компонента при данном его мольном содержании в смеси.
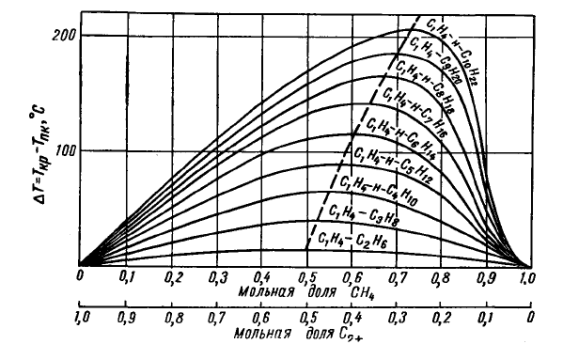
Рис. 15. Зависимость разности между истинной критической и псевдокритической температурами от "мольного содержания метана в бинарных смесях его с парафиновыми углеводородами (по Г. С. Степановой).
|
|
|
Пример1. Найти критическую температуру и критическое давление для смеси природного газа с бутаном молярного состава:
N2=0,003; СО2 = 0,0035; Ci = 0,6524; С2 = 0,0298; С3=0,0113; С4 = 0,3.
Расчетные величины псевдокритической температуры смеси, молекулярной массы второго сложного компонента С2 + высшие и его средней эквивалентной молекулярной массы приведены в табл. 1.
Псевдокритическая температура смеси
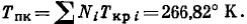
Молекулярная масса компонента С2 + высшие
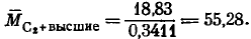
______________
1Степанова Г.С. Метод определения критической точки многокомпонентных углеводородных систем. Новости нефтяной и газовой техники. «Газовое дело», № 3, 1962.
Таблица 1
Расчетные данные псевдокритической температуры смеси, молекулярной и средней эквивалентной молекулярной массы компонента С2 +высшие

Средняя эквивалентная молекулярная масса компонента С2 + высшие
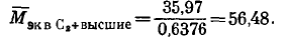
По рис. 15 определяем отклонение истинной критической температуры от псевдокритической Г при содержании С2 + высшие в смеси 0,3411 моля и ^с2+высшие = 55,28:

при М = 58,12 ДГ = 60
при М = 44,09 АГ==33,5
Для М = 55,28 Д7'=54,65
Критическая температура смеси составит:
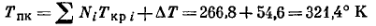
или
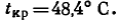
По рис. 13 определяем критическое давление
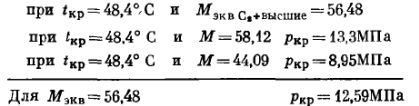
при t K p = 48,4ー,C И Л*эКВс,+высшие.
при <кр = 48,4ーС и ЛГ = 58,12 р к р = 13,ЗМПа
при * к р = 48,4ーС и М= 44,09 рк р=8,95МПа
Для = 56,48 ркр=12,59МПа
В пластовых газах часто содержится азот и поэтому на рис. 13 приведены также кривые азот - метан и азот - этан. С их помощью можно построить критическую кривую для углеводородных смесей, содержащих азот. Цифры на критической кривой азот - метан соответствуют мольному содержанию азота в смеси с метаном. Как уже упоминалось, при разделении углеводородов на условную бинарную смесь азот относят к первому компоненту. Левая начальная точка такой бинарной смеси начинается на кривой азот — метан и положение ее определяется мольным содержанием азота в первом компоненте.
По методике Г. С. Степановой далее из этой точки проводят две кривые эквидистантно двум критическим кривым бинарных смесей метана с углеводородами, молекулярные массы которых наиболее близки к средней эквивалентной молекулярной массе компонента С2 + высшие. И далее интерполяцией между построенными кривыми при данной критической температуре определяют ркр смеси по значению Мэкв компонента С2 + высшие.
Сравнение расчетных и экспериментальных данных показало 1, что критические параметры по методу Г. С. Степановой определяются с удовлетворительной точностью для систем с малым содержанием тяжелых компонентов (конденсата).
По экспериментальным данным Н. А. Тривус и И. И. Чернецкого при массовой доле в системе газа gr < 0,89 расхождения расчетных и экспериментальных величин ркр и Ткр достигают значительных пределов (gr = ^, где gT — газовый фактор, р — плотность газа).
|
|
|
|
|
Дата добавления: 2014-12-23; Просмотров: 4271; Нарушение авторских прав?; Мы поможем в написании вашей работы!