
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Генетические дефекты метаболизма фенилаланина и тирозина
|
|
|
|
Фенилкетонурия развивается как результат потери способности организма синтезировать фенилаланин-4-монооксигеназу, катализирующая превращение фенилаланина в тирозин. Характерной особенностью болезни является резкое замедление умственного развития ребенка, экстракция с мочой больших количеств фенилпировинаградной кислоты и фенилацетилглутамина, а также накопления в тканях фенилаланина.
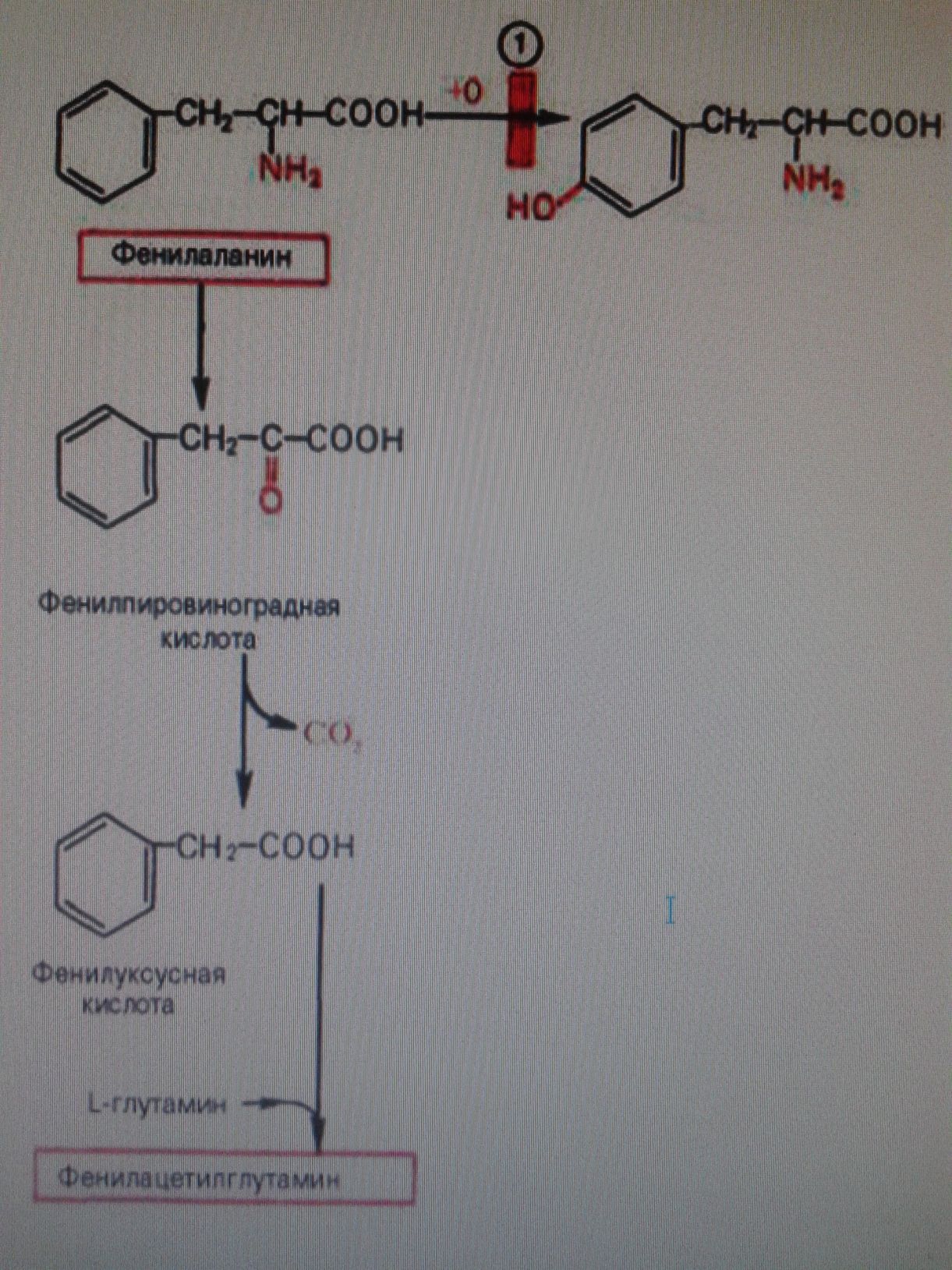
Развитие болезни можно предотвратить, если значительно снизить или исключить прием фенилаланина с пищей с самого рождения.
Альбинизм характеризуется врожденным отсутствием пигментов в коже, волосах и сетчатке. Метаболический дефект связан с потерей меланоцитами способности синтезировать тирозиназу – фермент, катализирующий окисление тирозина в диоксифенилаланин и диоксифенилаланинхинон, являющихся предшественниками меланина.
10.Переваривание белков в желудке. Пепсин, его строение и функция в процессе переваривания белка.
В желудке имеются все условия для переваривания белков. Во-первых в желудочном соке содержится активный фермент пепсин. Во-вторых, благодаря наличию в желудочном соке свободной соляной кислоты для действия пепсина создается оптимальная среда. Соляная кислота переводит неактивный пепсиноген в активный пепсин, создает оптимальную среду для действия пепсина, в присутствии соляной кислоты происходит набухание белков, происходит частичная денатурация, кроме того она ускоряет всасывание железа и оказывает бактерицидное действие. Пепсин вырабатывается в клетках слизистой оболочки желудка в неактивной форме – в виде пепсиногена, активатором которого является соляная кислота. Пепсин гидролизует преимущественно пептидные связи, образованные аминогруппами ароматических аминокислот. Он расщепляет практически все природные белки. Наибольший гидролитический эффект пепсин оказывает на денатурированные белки.
|
|
|
11. Синтез мочевины(схема). Гипераммонемия. 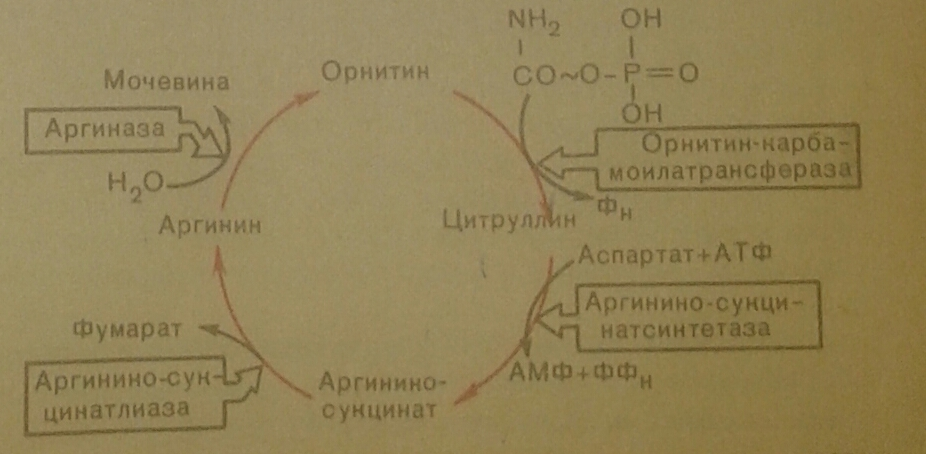
Гипераммонемия – это нарушение обмена веществ, проявляющиеся в недостаточности цикла ферментов мочевины, приводящее к отравлению организма аммиаком. Предельно допустимый уровень аммиака в крови 60 мкмоль/л. При повышении концентрации аммиака до предельных величин может наступить кома или смерть. При хронической гипераммонемии развивается умственная отсталость.

Основа лечения гипераммониемий сводится к ограничению белка в диете, это уже позволяет предотвратить многие нарушения мозговой деятельности.
ФЕРМЕНТЫ
1. Коферментные функции витаминов РР и В2
Витамин PP (ниацин) включает два соединения: никотиновую кислоту и ее амид. Открыт как фактор против пеллагры (отсюда PP), заболевания человека и животных, распространенного в XIX в.
Витамин жизненно необходим для клеточного метаболизма как катализатор окислительно-восстановительных процессов. Как и флавиновые коферменты, образующиеся из ниапина коферментные формы - никотинамида-дениндинуклеотид (НАД) и никотинамидадениндину-клеотидфосфат (НАДФ) (рис. 1), его фосфорилиро-ванные производные, участвуют в транспорте протонов и электронов.
Диапазон действия витамина чрезмерно широк. Он «вмешивается» в обмен белков, углеводов, липидов, обладает гипотензивным, антианемическим, антисклеротическим, сосудорасширяющим действием. С витамином PP связаны процессы обмена глюкозы, аминокислот, биосинтеза жирных кислот, простагландинов, стероидов. Витамин регулирует не только функции оксидоредук-ции, но и практически ферментативные реакции всех видов. Установлена возможность синтеза витамина из аминокислоты триптофана, который, таким образом, наряду с витамином PP является предшественником НАД (Ф)-коферментов. НАД восстановленный является субстратом, компонентом дыхательной цепи митохондрий с самым большим отрицательным потенциалом. Окисление восстановленного НАД сопровождается выделением энергии, кумулирующейся в виде макроэргической химической связи АТФ.
Клинические проявления авитаминоза PP (пеллагры) в основном представлены триадой — дерматит, диаррея, деменция. У больных наблюдаются поносы, бледность, сухость губ, специфический дерматит— поражение открытых для солнца частей тела, особенно лица, а также нарушения сознания — галлюцинации, бред, потеря памяти.
В настоящее время очевидно, что разнообразные физиологические эффекты действия витамина PP реализуются через взаимодействие его с гормонами гипофизарно-адреналовой системы и стероидными гормонами надпочечников.
Практически важное свойство никотиновой кислоты— способность расширять сосуды, влиять на микроциркуляцию крови, процессы свертываемости, очевидно, осуществляется путем активации системы кининов — биологически активных пептидов.
Находит применение и способность витамина PP направлять метаболизм в русло синтеза сукцината из липидов, активировать окисление липидов и снижать их содержание в крови. Это особенно важно при гипермобилизации жира из депо — атеросклерозе, выбросе кортикостероидов и др. В настоящее время
антилипемическое действие никотиновой кислоты и никотинамида доказано.
Много витамина PP или триптофана содержат следующие продукты: отруби злаков (особенно риса), дрожжи и продукты животного происхождения — печень, мясо, молоко
|
|
|
ниацин может синтезироваться в организме из аминокислоты триптофана. Теоретически 60 мг триптофана эквивалентны 1 мг никотиновой кислоты.
Структура витамина B2, как и тиамина, проявляет высокую специфичность: незначительные изменения могут вызвать снижение и даже потерю витаминных свойств или появление антивитаминных. Физиологическая роль витамина связана с его коферментной функцией. Ko-ферменты B2 — рибофлавинфосфат или флавинмоно-нуклеотид (ФМН) и его аденилированное производное флавинадениндинуклеотид (ФАД) (рис. 1), который синтезируется при взаимодействии ФМН с АТФ. В настоящее время известно несколько десятков ферментов, содержащих ФМН или ФАД и составляющих семейство флавиновых ферментов.
|
|
|
Именно кофермент, а точнее — изоаллоксазиновое кольцо рибофлавина, выполняет основную каталитическую функцию, присоединяя или отдавая два атома водорода. Таким образом, флавиновые ферменты—важнейшие участники процессов биологического окисления практически во всех клетках животных, чем и определяется влияние витамина на процессы роста и развития организма. В тканях витамин B2 содержится в виде коферментных форм (более 90 %), преимущественно ФАД. Свободный витамин обнаруживается в молоке, крови, моче, сетчатке глаза.
В активном центре ряда флавиновых ферментов обнаружены металлсодержащие производные рибофлавина — его комплексы с железом, медью, молибденом. Среди флавиновых ферментов имеются энзимы, переносящие водород от субстратов (различных веществ) на кислород, называемые оксида-зами и восстанавливающие другие акцепторы протонов и электронов в отсутствие кислорода — дегид-рогеназы. Несомненно, центральная «фигура» — фермент сукцинатдегидрогеназа, окисляющий янтарную кислоту и являющийся звеном цикла Кребса. Уникальная функция сукцинатдегидрогеназы заключается в том, что в условиях напряжения механизмов синтеза АТФ (гипоксия, различные стрессорные воздействия), когда другие окислительные процесы цикла угнетены, сукцинатдегидрогеназа активно пропускает поток протонов и электронов на дыхательную цепь, минуя НАД-зависимое звено. Это имеет огромный физиологический смысл в плане адаптации на уровне клетки.
Другой флавиновый фермент — глутатионредук-таза — поддерживает в клетке определенную концентрацию важнейшего тиолового соединения глутатио-на, постоянно регенерируя его из окисленной формы. Этим фермент регулирует окислительно-восстановительный статус клетки и участвует в детоксикации избытка окислителей. Глутатионредуктаза — важный компонент глутатионовой антиперекисной системы, фермент-антиоксидант, поэтому и витамин B2 относят к веществам, косвенно обладающим антиокси-дантными свойствами.
ФАД вместе с тиаминдифосфатом является компонентом пируват- и а-кетоглутаратдегидрогеназных комплексов. Флавиновые оксидазы катализируют окисление пуринов и образование мочевой кислоты (ксантиоксидаза), превращения адреналина и других биологически активных аминов (моноаминоксидаза).
|
|
|
Наконец, ФАД — компонент дыхательной цепи митохондрий, в которых окисление химических веществ завершается образованием воды и выделением энергии в виде АТФ.
Даже этот краткий перечень «заслуг» рибофлавина дает представление о нем как о важнейшем катализаторе окислительно-восстановительных процессов в клетке, чем и определяется картина витаминной недостаточности, для которой характерны такие общие поражения, как слабость, нарушения роста, поражения слизистых, заболевания глаз (конъюк-тивит, нарушение темновой адаптации, светобоязнь), анемия. Для недостаточности рибофлавина характерны сухость и трещины губ и особенно трещины в углах рта, сухой ярко-красный язык.
Источники витамина B2 для человека в основном те же, что и тиамина: мясо, печень, яичный желток, молоко, злаки, шпинат, капуста, картофель, дрожжи.
2. ФАД. Зависимые дегидрогеназы: сукцинатдегидрогеназы
Дыхательная цепь (ферменты тканевого дыхания) - это переносчики протонов и электронов от окисляемого субстрата на кислород. Окислитель - это соединение, способное принимать электроны. Такая способность количественно характеризуется окислительно-восстановительным потенциалом по отношению к стандартному водородному электроду, рН которого равен 7,0. Чем меньше потенциал соединения, тем сильнее его восстанавливающие свойства и наоборот.
Т. о. любое соединение может отдавать электроны только соединению с более высоким окислительно-восстановительным потенциалом. В дыхательной цепи каждое последующее звено имеет более высокий потенциал, чем предыдущее.
Дыхательная цепь состоит из:
НАД - зависимой дегидрогеназы;
ФАД- зависимой дегидрогеназы;
Убихинона (КоQ);
Цитохрмов b, c, a+a3.
НАД-зависимые дегидрогеназы. В качестве кофермента содержат НАД и НАДФ. Пиридиновое кольцо никотинамида способно присоединять электроны и протоны водорода.
ФАД и ФМН-зависимые дегидрогеназы содержат в качестве кофермента фосфорный эфир витамина В2 (ФАД).
Убихинон (КоQ) отнимает водород у флавопротеидов и превращается при этом в гидрохинон.
Цитохромы - белки хромопротеиды, способные присоединять электроны, благодаря наличию в своем составе в качестве простетических групп железопорфиринов. Они принимают электрон от вещества, являющегося немного боле сильным восстановителем, и передают его более сильному окислителю. Атом железа связан с атомом азота имидазольного кольца аминоксилоты гистидина с одной стороны от плоскости порфиринового цикла, а с другой стороны с атомом серы метионина. Поэтому потенциальная способность атома железа в цитохромах к связыванию кислорода подавлена.
В цитохроме с порфириновая плоскость ковалентно связана с белком через два остатка цистеина, а в цитохромах b и а, она ковалентно не связано с белком.
В цитохроме а+а3 (цитохромоксидазе) вместо протопорфирина содержатся порфирин А, который отличатся рядом структурных особенностей. Пятое координационное положение железа занято аминогруппой, принадлежащей остатку аминосахара, входящего в состав самого белка.
В отличии от гема гемолгобина атом железа в цитохромах может обратимо переходить из двух в трехвалентное состояние это обеспечивает транспорт электронов (См. подробнее приложение 1 "Атомная и электронная структура гемопротеинов ").
Вопрос 3
Ферментативный ингибитор — вещество, замедляющее протекание ферментативной реакции. Различают обратимые и необратимые ингибиторы (см. ниже).
Изучение ингибирования ферментов играет важную роль в создании лекарств, в изучении механизма действия и структуры ферментов
Обратимое ингибирование
Конкурентное ингибированиеКонкурентный ингибитор обычно структурно схож с субстратом, однако фермент не способен катализировать реакцию в присутствии ингибитора из-за отсутствия у последнего необходимых функциональных групп.
Схема конкурентного ингибирования и уравнение Михаэлиса-Ментен для него выглядят следующим образом:
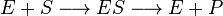 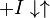 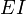
| 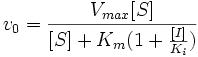
|
Видно, что при конкурентном ингибировании максимальная скорость реакции Vmax не меняется, а кажущаяся константа Михаэлиса увеличивается в (1 + [ I ]/ Ki) раз. Поэтому в двойных обратных координатах Лайнуивера-Берка (зависимость 1/ v 0 от 1/[ S ]) при разных концентрациях ингибитора получают семейство прямых с различным наклоном, пересекающихся в одной точке на оси ординат.
Константу ингибирования Ki обычно определяют так: проводят ряд измерений кажущейся константы Михаэлиса при различных концентрациях ингибитора, затем строят зависимость этой величины от концентрации ингибитора. Тангенс угла наклона полученной прямой равен Km / Ki.
Неконкурентное ингибирование
Неконкурентный ингибитор не мешает связыванию субстрата с ферментом. Он способен присоединяться как к свободному ферменту, так и к фермент-субстратному комплексу с одинаковой эффективностью. Ингибитор вызывает такие конформационные изменения, которые не позволяют ферменту превращать субстрат в продукт, но не влияют на сродство фермента к субстрату.
Схема и уравнение Михаэлиса-Ментен в случае неконкурентного ингибирования:
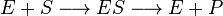  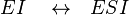
| 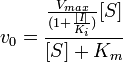
|
При неконкурентном ингибировании константа Михаэлиса не изменяется, а максимальная скорость реакции уменьшается в (1 + [ I ]/ Ki) раз. Поэтому в двойных обратных координатах семейство прямых, отвечающих разным концентрациям ингибитора, пересекается в одной точке на оси абсцисс.
Бесконкурентное ингибирование
При бесконкурентном ингибировании ингибитор связывается только с фермент-субстратным комплексом, но не со свободным ферментом. Субстрат, связываясь с ферментом, изменяет его конформацию, что делает возможным связывание с ингибитором. Ингибитор, в свою очередь, так меняет конформацию фермента, что катализ становится невозможным.
Схема и уравнение Михаэлиса-Ментен в случае бесконкурентного ингибирования:
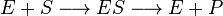
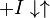
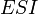
| 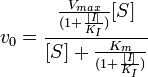
|
Максимальная скорость реакции и кажущаяся константа Михаэлиса уменьшаются в одинаковое число раз. Поэтому в двойных обратных координатах для разных концентраций ингибитора получаем семейство параллельных прямых.
Ингибирование субстратом
Ингибирование субстратом — частный случай бесконкурентного ингибирования, когда две молекулы субстрата связываются с ферментом, что препятствует образованию продукта.
Схема и уравнение Михаэлиса-Ментен в случае ингибирования субстратом:
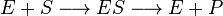
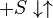
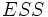
| 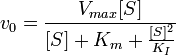
|
Необратимое инги бирование
Формирование стабильного комплекса ингибитора с ферментом, ведущее к его необратимой инактивации. Случай необратимого ингибирования можно обнаружить по тому признаку, что при разбавлении раствора не происходит повышения удельной активности фермента, как в случае обратимого ингибирования
Аллостерическое ингибирование
Аллостерические ингибиторы связываются с отдельными участками фермента вне активного центра. Такое связывание влечет за собой конформационные изменения в молекуле фермента, которые приводят к уменьшению его активности. Аллостерические эффекты встречаются практически только в случае олигомерных ферментов. Кинетику таких систем нельзя описать с помощью простой модели Михаэлиса-Ментен.
4 вопросВторичные энзимопатии
Вторичные энзимопатии являются следствием тех или иных патологических процессов, сопровождающихся нарушением активности ферментов. Они наблюдаются при многих заболеваниях. Так например, причиной развития вторичной лактазной недостаточности могут являться: кишечные инфекции вирусной и бактериальной этиологии, паразитарные заболевания (лямблиоз и др.), синдром короткой кишки (пострезекционный), целиакия, токсическое и лекарственное поражения кишечника (на фоне лучевой и химиотерапии, антибиотикотерапии).
Одним из вариантов вторичных энзимопатий являются алиментарные энзимопатии – патологические состояния, обусловленные стойкими нарушениями активности ферментов в связи с характером питания. Алиментарные энзимопатии могут быть обусловлены длительным дефицитом белка в питании (например при квашиоркоре), нарушением биосинтеза коферментов при витаминной недостаточности, угнетением синтеза металлоферментов при низком содержании в рационе соответствующих минеральных веществ. Кроме того, они могут возникать при несбалансированном питании в целом. К развитию алиментарных энзимопатий может приводить также нарушение поступления пищевых веществ из желудочно-кишечного тракта в кровь при длительных поносах, атрофии или поражении слизистой оболочки кишечника и др. К алиментарным энзимопатиям относят и так называемые токсические энзимопатии, связанные с угнетением активности или биосинтеза отдельных ферментов различными естественными компонентами пищевых продуктов (ингибиторы протеолитических ферментов, антивитамины и др.) или чужеродными веществами (например пестицидами), содержащимися в них.
Клинические проявления приобретенных энзимопатий зависят от вида фермента, функция которого нарушена и характеризуется нарушениями того или иного вида обмена веществ.
Энзимопатии углеводнго обмена
Галактоземия – возникает при нарушении обмена галактозы, обусловленном наследственным дефектом одного из трех ферментов, включающим галактозу в метаболизм глюкозы. Галактоземия, вызванная недостаточностью галактозо-1-фосфатуридилилтрансферазы (ГАЛТ) наиболее хорошо изучена. Это заболевание проявляется очень рано и особенно опасно для детей, так как основным источником углеводов для них служит материнское молоко, содержащее лактозу. Ранние симптомы дефекта ГАЛТ: рвота, диарея, дегидратация, уменьшение массы тела, желтуха, гепатомегалия, катаракта, задержка психического развития. Лабораторные исследования при этом выявляют галактоземию, галактозурию, галактозо-1-фосфатемию, тенденцию к гипогликемии.
При дефекте фермента галактокиназы у пациентов отмечается галактоземия, галактозурия, катаракта. Гораздо реже причиной возникновения галактоземии является дефект уридилфосфат-4-эпимеразы, при котором не отмечается тяжелых клинических проявлений.
При диагностике галактоземии исследуют мочу на содержание галактозы, собранную после нескольких кормлений молоком. При обнаружении у ребенка катаракты его обследуют на недостаточность галактокиназы и ГАЛТ.
^ Недостаточность дисахаридаз. Дисахаридазы локализованы в щеточной каемке клеток слизистой тонкого кишечника и участвуют в расщеплении дисахаридов на моносахариды, что является необходимым условияем их всасывания. Дисахаридазы подразделяются на α-гликозидазы (изомальтаза, сахараза, мальтаза) и β-гликозидазы (лактаза, β-галактозидаза).
К этой группе нарушений относится отсутствие активности сахаразы и изомальтазы. Дисахариды не расщепляются и не могут быть утилизированы. Они осмотически активны, связывают воду в просвете кишечника и вызывают диарею после пероральной нагрузки дисахаридами. Кроме того, после такой нагрузки в крови не удается обнаружить повышение гликемии в интервале 30-90 минут, как это отмечается у здоровых людей. Непереносимость лактозы обусловлена дефектом лактазы и проявляется также, как и вышеперечисленные состояния.
^ Нарушения метаболизма мукополисахаридов (гликозаминогликанов). Важнейшей составной частью соединительной ткани являются протеогликаны, состоящие из агрегированных мономерных субъединиц, содержащих центрально расположенное «белковое ядро», с которым связаны гликозидные цепи различных гликозаминогликанов (ГАГ). Количество и соотношение различных протеогликанов зависит от типа соединительной ткани. Они образуются в специальных клетках этой ткани – фибробластах, в лизосомах этих же клеток они после эндоцитоза разрушаются. Функции ГАГ – поддержание структурной целостности соединительной ткани и организация межклеточного матрикса. ГАГ взаимодействуют с компонентами клеточных мембран в таких процессах, как рост клеток, межклеточные коммуникации, восприятие информации, взаимодействие некоторых плазменных белков с сосудистой стенкой. Разрушение ГАГ начинается с терминального моносахарида под влиянием специфических гликозидаз. Если какие-либо из этих лизосомальных ферментов отсутствуют или их активность нарушена в соединительной ткани начинается накопление неразрушенных или частично разрушенных ГАГ. Это приводит к возникновению ряда заболеваний, объединенных общим названием мукополисахаридозы. Мукополисахаридозы отличаются прогрессирующим течением с различной степенью тяжести. Общие признаки различных форм этих заболеваний: деформация черт лица, изменение скелета, деформация суставов, поражение печени, селезенки, сердца, кровеносных сосудов. Характерна также задержка психомоторного и умственного развития. Ниже приводится характеристика некоторых форм мукополисахаридозов. Синдром Гурлера – обусловлен дефицитом α-L-идуронидазы. Протекает тяжело – больные умирают в возрасте до 10 лет. У детей отмечается деформация позвоночника, суставов, отставание в росте, комбинированная проводниковая и нейросенсорная глухота, гепатоспленомегалия. С мочой экскретируются гепаран- и дерматан-сульфаты.
^ Синдром Моркио – вызван дефектом галактозо-6-сульфатазы, которая расщепляет связь, имеющуюся только в кератансульфате. Это ведет к накоплению последнего в составе хрящей межпозвоночных дисков и роговицы, что и определяет клинику заболевания. Поражается преимущественно скелет – выступают нижние ребра, наступает х-образное искривление ног, характерно выпирание грудины и очень короткая шея. С мочой выделяется кератансульфат.
^ Дефицит глюкуронидазы – дефект, проявляющийся огрублением черт лица, гепатоспленомегалией, изменениями скелета. Лабораторно выявляется: наличие дерматан- и гепаран-сульфатов в моче, метахроматические гранулы в гранулоцитах периферической крови, снижение активности фермента в лейкоцитах и сыворотке крови.
|
|
|
|
|
Дата добавления: 2015-03-29; Просмотров: 1594; Нарушение авторских прав?; Мы поможем в написании вашей работы!