
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергия Гиббса и направление хим. реакции
|
|
|
|
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (Δ H), и энтропийным T Δ S, обусловленным увеличением беспорядка в системе вследствие роста ее энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж): При Δ G < 0 реакция термодинамически разрешена и система стремится к достижению условия Δ G = 0, при котором наступает равновесное состояние обратимого процесса; Δ G > 0 указывает на то, что процесс термодинамически запрещен. Стандартная молярная свободная энергия образования это изменение свободной энергии Гиббса, которым сопровождается образование одного моля данного вещества в их стандартных состояниях. Итак, в химических процессах одновременно изменяются энергетический запас системы (энтальпийный фактор) и степень ее беспорядка (энтропийный фактор, не совершающая работу энергия).1.Если Δ H < 0 и Δ S > 0, то всегда Δ G < 0 и реакция возможна при любой температуре.2.Если Δ H > 0 и Δ S < 0, то всегда Δ G > 0, и реакция с поглощением теплоты и уменьшением энтропии невозможна ни при каких условиях.3.В остальных случаях (Δ H < 0, Δ S < 0 и Δ H > 0, Δ S > 0) знак Δ G зависит от соотношения Δ H и T Δ S. Реакция возможна, если она сопровождается уменьшением изобарного потенциала;
|
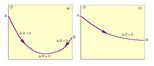
3. Фазовые диаграммы двухкомпонентных систем. Фракционная перегонка.
Диаграмма состояния представляет собой графическое изображение зависимости между величинами, характеризующими состояние системы, и фазовыми превращениями в системе (переход из одного состояния в другое). Диаграммы состояния широко применяются в химии. Равновесия между различными фазами одной с-мы называют фазовыми, а описывают эти фазовые равновесия посредством фазовых диаграмм или диаграмм состояния. Фазовая диаграмма позволяет установить условия равновесия между числом фаз, числом компонентов и числом степеней свободы (вариантностью) с-мы. Фаза (Ф) – гомогенная (однородная по химическому составу и термодинамическим свойствам) часть с-мы, отделенная от других частей поверхностью раздела. Так, два нерастворимых друг в друге твердые в-ва, как и две несмешивающиеся жидкости, образуют две фазы. Компоненты (К) – химически индивидуальные вещества, наименьшее число которых достаточно для образования фаз с-мы. Число компонентов определяется количеством индивидуальных веществ в системе за вычетом числа возможных между ними обратимых взаимодействий. Например, система из трех индивидуальных веществ H2O, H2, O2 будет двухкомпонентной, поскольку для образования всех фаз достаточно любых двух веществ. Степени свободы (С) – число параметров (температура, давление, состав системы), которые можно произвольно менять без изменения числа фаз в системе. Правило фаз Гиббса: в изолированной равновесной системе число степеней свободы равно числу компонентов системы плюс два минус число фаз.
|
|
|
Перегонка = ДИСТИЛЛЯЦИЯ (от лат. distillatio — стекание каплями) (перегонка), разделение многокомпонентных жидких смесей на отличающиеся по составу фракции; основано на различии в составах жидкости и образующегося из нее пара. Осуществляется путем частичного испарения жидкости и последующей конденсации пара. Полученный конденсат обогащен низкокипящими компонентами, остаток жидкой смеси — высококипящими. Дистилляция применяется в химической, нефтеперерабатывающей, фармакологической промышленности, в лабораторной практике.
|
|
|
Фракции нефти: Бензин, керосины, соляровые масла, мазут.
Билет 21… 1. Ковалентная связь. Основные положения теории отталкивания валентных электронных пар (ОВЭП), теории валентных связей (ТВС). Гибридизация. Полярная и неполярная ковалентная связь.
Ковалентная связь - хим. связь между двумя атомами, осуществляемая общей для этих атомов парой электронов. Неполярная (между атомами неметаллов с одинаковой элеткроотрицательностью) полярная (между атомами неметаллов с разной электроотрицательностью). Связь становится полярной когда один из атомов перетягивает к себе общую эл пару.
Свойства ковалентной связи: 1)ковалентная связь насыщенная, это значит что между атомами ограниченное число связей; 2)Связь направлена по оси ох, оу, оz;(Направленность связи. Образование ковалентной связи взывается перекрыванием электронных облаков взаимодействующих атомов. Но такое перекрывание возможно только при определенной взаимной ориентации электронных облаков; при этом область перекрывания располоагется в определенном направлении по отношению к взаимодействующим атомам.) 3)Связь поляризуемая - деформируется во внешнем эл.поле.
|
|
|
|
|
Дата добавления: 2015-04-23; Просмотров: 439; Нарушение авторских прав?; Мы поможем в написании вашей работы!