
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Билет №7. Закон Авогадро. Следствие закона Авогадро
|
|
|
|
Закон Авогадро. Следствие закона Авогадро.
В равных объемах различных газов и паров при нормальных условиях содержится одинаковое число молекул.
H2 + O2 = 2H2O
4. 1 моль любого газа или пара при н.у. содержит 6,02*1023 структурных единиц.
н.у. всегда задаются 273 град. К
p=105Па
5. 1 моль любого газа или пара при н.у. занимает объем 22,4л.
6. Отношение масс равных объемов различных газов равно отношению их молярных масс и называется относительной плотностью первого газа по второму.
m1/m2=M1/M2=D
 1. Электрохимия. Уравнение Нернста.
1. Электрохимия. Уравнение Нернста.
Если любой металл (Al, Fe) опустить в воду, то часть ионов металла с поверхности перейдет в воду.
Me0-2e=Me4+
На поверхности раздела фаз возникает двойной электрический слой, обладающий определенным значением электронного потенциала.
Скорость растворения у разных металлов разная.
Если металл опускать раствор своей соли, то получится следующее:
1)  для активных металлов (стоящие до водорода) наблюдается та же картина: пластина заряжена отрицательно, часть ионов переходит в воду.
для активных металлов (стоящие до водорода) наблюдается та же картина: пластина заряжена отрицательно, часть ионов переходит в воду.
DGраств<0
Энергия гидротации больше, чем работа выхода ионов на поверхности металла.
Zn0-2e=Zn2+
восст. окисл.
2) для металлов за водородом, энергетически более выгоден следующий процесс: ионы металла из раствора внедряются в кристаллическую структуру металла, заряжая его положительно.
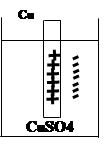 |
Cu2++2e=Cu0
В обоих случаях на границах раздела фаз возникает электронный потенциал. Его величина зависит от:
- природы металла
- концентрации раствора
- температуры
Влияние этих факторов описывается уравнением Нернста:
восстановительную форму одного и того же элемента.
 |
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 514; Нарушение авторских прав?; Мы поможем в написании вашей работы!