
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Стационарное состояние
|
|
|
|
Принцип производства энтропии. Организм как открытая система
Выше была описана направленность термодинамических процессов в изолированной системе. Однако реальные процессы и состояния в природе и технике являются неравновесными, а многие системы – открытыми.
Эти процессы и системы рассматриваются в неравновесной термодинамике. Аналогично тому как в равновесной термодинамике особым состоянием является состояние равновесия, так в неравновесной термодинамике особую роль играют стационарные состояния. Несмотря на то что в стационарном состоянии необходимые процессы, протекающие в системе (диффузия, теплопроводность и др.), увеличивают энтропию, энтропия системы не изменяет.
Представим изменением энтропии DS системы в виде суммы двух слагаемых:
DS =DSi + DSl,
где DSi – изменение энтропии, обусловленное необратимыми процессами в системе; DSl – изменение энтропии, вызванное взаимодействием системы с внешними телами (потоки, проходящие через систему). Необратимость процессов приводит к DSi > 0, стационарность состояния – к DSi = 0; следовательно: DSl = DS – DSi < 0. Это означает, что энтропия в продуктах (вещество и энергия), поступающих в систему, меньше энтропии в продуктах, выходящих из системы.
Начальное развитие термодинамики стимулировалось потребностями промышленного производства. На этом этапе (XIX в.) основные достижения заключались в формулировке законов, разработке методов циклов и термодинамических потенциалов применительно к идеализированным процессам.
Биологические объекты являются открытыми термодинамическими системами. Они обмениваются с окружающей средой энергией и веществом. Для организма – стационарной системы – можно записать dS = 0, S = = const, dS i> 0, dSe < 0. Это означает, что большая энтропия должна быть в продуктах выделения, а не в продуктах питания.
При некоторых патологических состояниях энтропия биологической системы может возрастать (dS > 0), это связано с отсутствием стационарности, увеличением неупорядоченности. Формула может быть представлена:

или для стационарного состояния
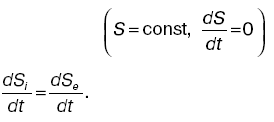
Из этого видно, что при обычном состоянии организма скорость изменения энтропии за счет внутренних процессов равна скорости изменения отрицательной энтропии за счет обмена веществ и энергией с окружающей средой.
|
|
|
|
|
Дата добавления: 2015-03-29; Просмотров: 313; Нарушение авторских прав?; Мы поможем в написании вашей работы!