
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Предельные одноатомные спирты, общая формула. Этанол, строение, физические и химические свойства, применение
|
|
|
|
Билет №8
Предельные одноатомные спирты - это производные предельных углеводородов, в молекуле которых один атом водорода замещён на гидроксильную группу.
Общая формула: CnH2n+1OH
Виды изомерии спиртов:
·  Изомерия углеродного скелета
Изомерия углеродного скелета
СН3- СН2-СН2-СН2-ОН – бутанол1
·  Изомерия положения функциональной группы ОН
Изомерия положения функциональной группы ОН
СН3-СН2-СН2-ОН пропанол1,
· Межклассовая изомерия с простыми эфирами
СH3CH2OH – этиловый спирт СH 3 - O -CH3 - диметиловый эфир
Этано́л — C2H5OH
Физические свойства: в обычных условиях представляет собой бесцветную жидкость с характерным запахом, может растворяться в воде, высокая температура плавления и кипения. Молекулы спирта между собой связаны водородной связью.
Химические свойства:неэлектролит, не обладает ярко выраженными основными свойствами или кислотными, не изменяют окраску индикаторов.
· Со щелочными и щелочно-земельными металлами:
2C2H5OH + 2К → 2С2Н5ОК + Н2
· Горение:
C2H5OH+3O2 →2CO2+ H2O
· C галогеноводородами:
C2H5OH+HBr → C2H5Br+H2O
· C кислотами (образуются сложные эфиры):
· C2H5OH+СH3COOH →CH3COOC2H5
· Окисление:
C2H5OH+CuO →CH3COH+H2O+Cu
+ Ме щелочной металл
+ O2 (горение)
+НСl, HBr
+спирт (образуется простой эфир)
+карбоновая кислота (образуется сложный эфир)
+ СuO (качественная реакция) – образуется альдегид
Применение:
· Производство синтетического каучука
· Материал для получения медикаментов, духов, лаков, красителей
· Получают уксусную кислоту и др. вещества
· Растворитель лекарственных препаратов
· Дезинфицирующее средство
· Используют для приготовления экстрактов и настоек
· Спиртные напитки
Билет № 9
1. Глицерин – представитель многоатомных спиртов. Строение, физические, химические свойства, применение.
|
|
|
Глицерин (пропан триол- 1,2,3)
Химическая формула:
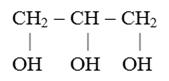
Физические свойства
Бесцветная, вязкая, гигроскопичная жидкость, неограниченно растворимая в воде. Сладкий на вкус, отчего и получил своё название (гликос — сладкий). Хорошо растворяет многие вещества.
Химические свойства
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 5502; Нарушение авторских прав?; Мы поможем в написании вашей работы!