
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тугоплавкие металлы и сплавы на их основе. Примеры применения
|
|
|
|
Тугоплавкие металлы — класс химических элементов (металлов), имеющих очень высокую температуру плавления и стойкость к изнашиванию. Определение тугоплавких металлов относится к каждому элементу группы по разному. Основными представителями данного класса элементов являются элементы пятого периода — ниобий имолибден; шестого периода — тантал, вольфрам и рений. Все они имеют температуру плавления выше 2000 °C, химически относительно инертны и обладают повышенным показателем плотности. Благодаря порошковой металлургии из них можно получать детали для разных областей промышленности.
Вольфрам. Рений используется в сплавах с вольфрамом в концентрации до 22 %, что позволяет повысить тугоплавкость и устойчивость к коррозии. Торий применяется в качестве легирующего компонента вольфрама. Благодаря этому повышается износостойкость материалов. В порошковой металлургии компоненты могут быть использованы для спекания и последующего применения. Для получения тяжёлых сплавов вольфрама применяются никель и железо или никель и медь. Содержание вольфрама в данных сплавах как правило выше 90 %. Смешивание легирующего материала с ним низкое даже при спекании.
Вольфрам и его сплавы по-прежнему используются там, где присутствуют высокие температуры, но нужна однако высокая твёрдость и где высокой плотностью можно пренебречь. Нити накаливания, состоящие из вольфрама, находят свое применение в быту и в приборостроении. Лампы более эффективно преобразовывают электроэнергию в свет с повышением температуры. В вольфрамовой газодуговой сварке (англ.) оборудование используется постоянно, без плавления электрода. Высокая температура плавления вольфрама позволяет ему быть использованным при сварке без затрат. Высокая плотность и твёрдость позволяют вольфраму быть использованным в артиллерийских снарядах. Его высокая температура плавления применяется при строении ракетных сопел, примером может служить ракета «Поларис». Иногда он находит свое применение благодаря своей плотности. Например, он находит свое применение в производстве клюшек для гольфа. В таких деталях применение не ограничивается вольфрамом, так как более дорогой осмий тоже может быть использован.
|
|
|
Широкое применение находят сплавы молибдена. Наиболее часто используемый сплав — титан-цирконий-молибден — содержит в себе 0,5 % титана, 0,08 % циркония и остальное молибден. Сплав обладает повышенной прочностью при высоких температурах. Рабочая температура для сплава — 1060 °C. Высокое сопротивление сплава вольфрам-молибден (Mo 70 %, W 30 %) делает его идеальным материалом для отливки деталей из цинка, например, клапанов.
Молибден используется в ртутных герконовых реле, так как ртуть не формирует амальгамы с молибденом.
Молибден является самым часто используемым тугоплавким металлом. Наиболее важным является его использование в качестве усилителя сплавов стали. Применяется при изготовлении трубопроводов вместе с нержавеющей сталью. Высокая температура плавления молибдена, его сопротивляемость к износу и низкий коэффициент трения делают его очень полезным материалом для легирования. Его прекрасные показатели трения приводят его к использованию в качестве смазки где требуется надежность и производительность.
Ниобий почти всегда находится вместе с танталом; ниобий был назван в честь Ниобы, дочери Тантала в греческой мифологии. Ниобий находит множество путей для применения, некоторые он разделяет с тугоплавкими металлами. Его уникальность заключается в том, что он может быть разработан путем отжига для того, чтобы достичь широкого спектра показателей твёрдости и упругости; его показатель плотности самый малый по сравнению с остальными металлами данной группы. Он может применяться вэлектролитических конденсаторах и является самым частым металлом всуперпроводниковых сплавах. Ниобий может применяться в газовых турбинахвоздушного судна, в электронных лампах и ядерных реакторах.
|
|
|
Сплав ниобия C103, который состоит из 89 % ниобия, 10 % гафния и 1 % титана, находит свое применение при создании сопел вжидкостных ракетных двигателях, например таких как Apollo CSM (англ.). Применявшийся сплав не позволяет ниобию окисляться, так как реакция происходит при температуре от 400 °C.
Тантал является самым стойким к коррозии металлом из всех тугоплавких металлов.
Важное свойство тантала было выявлено благодаря его применению в медицине — он способен выдерживать кислую среду(организма). Иногда он используется в электролитических конденсаторах. Применяется в конденсаторах сотовых телефонов и компьютера.
38.  Характеристика диаграммы состояния сплавов 3-ого типа (эвтектического и перитектического типа). Правило фаз и отрезков.
Характеристика диаграммы состояния сплавов 3-ого типа (эвтектического и перитектического типа). Правило фаз и отрезков.
Она соответствует сплавам, компоненты которых имеют неограниченную растворимость в жидком и ограниченную - в твердом состоянии.
Диаграмма состояния эвтектического типа. По этой диаграмме кристаллизуются сплавы, компоненты которых имеют следующие свойства:1) в жидком состоянии неограниченно взаимно растворяются; 2) в твердом состоянии обладают ограниченной растворимостью: один компонент растворяется в другом не в любых количествах, а только до некоторого предела;3) не образуют между собой химических соединений;4) образуют эвтектику.В реальных сплавах подобное взаимодействие компонентов встречается очень часто, например, в сплавах Cu-Ag, Cu-Sb, Al-Mg и др.Возможны два случая: I) оба компонента взаимно ограниченно растворяются друг в друге; 2) первый компонент растворяется во втором, а второй - не растворяется в первом.
Первое положение правила отрезков: чтобы определить концентрации компонентов в фазах, через данную точку, хар-щую состояние сплава, проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область; проекции точек пересечения на ось концентраций показывают составы фаз.
|
|
|
Второе положение правила отрезков: для того, чтобы определить количественное соотношение фаз через заданную точку проводят горизонтальную линию. Отрезки этой линии между заданной точкой и точками, определяющими составы фаз, обратно пропорциональны количествам этих фаз.
Правило фаз — соотношение, связывающее число веществ (компонентов), фаз и степеней свободы в гетерогенной системе.
Правило фаз записывается следующим образом:

где j — число фаз (например, агрегатных состояний вещества);
v — число степеней свободы, то есть независимых параметров (температура, давление, концентрация компонентов), которые полностью определяют состояние системы при равновесии и которые можно менять без изменения числа и природы фаз;
k — число компонентов системы — число входящих в систему индивидуальных веществ за вычетом числа химических уравнений, связывающих эти вещества. Иначе говоря, это минимальное количество веществ, из которых можно приготовить каждую фазу системы.
n — число переменных, характеризующих влияние внешних условий на равновесие системы.
При переменных давлении и температуре правило фаз сводится к выражению:
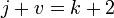
В случае однокомпонентной системы оно упрощается до:
 ,
,
Отсюда видно, например, что в однокомпонентной системе три фазы (j=3) могут сосуществовать при числе степеней свободы v, равном нулю, то есть при фиксированных давлении и температуре, что соответствует тройной точке на фазовой диаграмме. Две фазы (j=2) сосуществуют при произвольном измененнии либо давления, либо температуры, когда вторая из этих переменных не является независимой (v=1), то есть двухфазному равновесию на фазовой диаграмме соответствует линия. Если фаза одна (j=1), число степеней свободы системы равно двум, то есть температура и давление могут менятся независимо в пределах некоторой области на фазовой диаграмме — пока система не окажется на одной из линий двухфазного равновесия.
Иногда правило фаз записывают следующим образом:
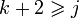
то есть при равновесии число фаз в системе меньше либо равно числу компонентов плюс 2.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1488; Нарушение авторских прав?; Мы поможем в написании вашей работы!