
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Атомная орбиталь 2 страница
|
|
|
|
[Сr(H2O)3F3] — трифторотриаквахром
[Сo(NH3)3Cl(NO2)2] — динитрохлоротриамминкобальт
[Pt(NH3)4Cl2]Cl2 — хлорид дихлоротетраамминплатины(IV)
[Li(H2O)4]NO3 — нитрат тетрааквалития
[править]Структура и стереохимия
Строение комплексных соединений рассматривают на основе координационной теории, предложенной в 1893 г. швейцарским химиком Альфредом Вернером, лауреатом Нобелевской премии. Его научная деятельность проходила в Цюрихском университете. Ученый синтезировал много новых комплексных соединений, систематизировал ранее известные и вновь полученные комплексные соединения и разработал экспериментальные методы доказательства их строения.
В соответствии с этой теорией в комплексных соединениях различают комплексообразователь, внешнюю и внутреннюю сферы. Комплексообразователем обычно является катион или нейтральный атом. Внутреннюю сферусоставляет определенное число ионов или нейтральных молекул, которые прочно связаны с комплексообразователем. Их называют лигандами. Число лигандов определяет координационное число (КЧ) комплексообразователя. Внутренняя сфера может иметь положительный, отрицательный или нулевой заряд.
Остальные ионы, не разместившиеся во внутренней сфере, находятся на более далеком расстоянии от центрального иона, составляя внешную координационную сферу.
Если заряд лигандов компенсирует заряд комплексообразователя, то такие комплексные соединения называют нейтральными или комплексами-неэлектролитами: они состоят только из комплексообразователя и лигандов внутренней сферы. Таким нейтральным комплексом является, например, [Pt(NH3)2Cl2].
Природа связи между центральным ионом (атомом) и лигандами может быть двоякой. С одной стороны, связь обусловлена силами электростатического притяжения. С другой — между центральным атомом и лигандами может образоваться связь по донорно-акцепторному механизму по аналогии с ионом аммония. Во многих комплексных соединениях связь между центральным ионом (атомом) и лигандами обусловлена как силами электростатического притяжения, так и связью, образующейся за счет неподеленных электронных пар комплексообразователя и свободных орбиталей лигандов.
Комплексные соединения, имеющие внешнюю сферу, являются сильными электролитами и в водных растворах диссоциируют практически нацело на комплексный ион и ионы внешней сферы.
При обменных реакциях комплексные ионы переходят из одних соединений в другие, не изменяя своего состава.
Наиболее типичными комплексообразователями являются катионы d-элементов. Лигандами могут быть:
а) полярные молекулы — NH3, Н2О, CO, NO;
б) простые ионы — F−, Cl−, Br−, I−, H+;
в) сложные ионы — CN−, SCN−, NO2−, OH−.
Для описания взаимосвязи пространственного строения комплексных соединений и их физико-химических свойства используются представления стереохимии. Стереохимический подход — удобный прием представления свойств вещества в части влияния того или иного фрагмента структуры вещества на свойство.
Объекты стереохимии — комплексные соединения, органические вещества, высокомолекулярные синтетические и природные соединения. А. Вернер, один из основоположников координационной химии, приложил большие усилия к развитию неорганической стереохимии. Именно стереохимия является центральной в этой теории, до сих пор остающийся ориентиром в координационной химии.
[править]Изомерия координационных соединений
В статистическом аспекте стереохимии центральным оказывается явление изомерии координационных соединений. Свойство изомерии химических соединений было известно еще при разработке классической теории химического строения. Изомерия молекул открыта в 1823 г. Ю.Либихом, обнаружившим, что серебряная соль гремучей кислоты и изоцианат серебра имеют один и тот же элементный состав, но разные физические и химические свойства.
Под изомерией понимают способность к разному взаимному расположению атомов и атомных фрагментов в соединениях одинакового общего состава, диктующую отличия в химических и физических свойствах соответствующих соединений — изомеров. В случае координационных соединений указанные различия могут быть связаны как со спецификой расположения лигандов во внутренней координационной сфере, так и с распределением лигандов между внутренней и внешними сферами.
Изомерия прямо связана с наличием или отсутствием в соединении тех или иных элементов симметрии: поворотных осей, зеркально-поворотных осей, центра и плоскостей симметрии.
Стереохимическая конфигурация характеризует относительное пространственное расположение атомов или групп атомов в молекуле химического соединения. Смысл этого термина зависит от конкретного пространственного расположения атомов в структуре комплекса. Его используют для описания фигуры или многогранника вместе с дополнительным определением, характеризующим специфику пространственного расположения атомов. Так, можно говорить о цис- или транс-конфигурации; D (d), L(l), DL (dl) — соответственно право-, левовращающая конфигурация, рацемат.
Существуют изомеры двух типов:
1) соединения, в которых состав внутренней сферы и строение координированных лигандов идентичны (геометрические, оптические, конформационные, координационного положения);
2) соединения, для которых возможны различия в составе внутренней сферы и строении лигандов (ионизационные, гидратные, координационные, лигандные).
[править] Пространственная (геометрическая) изомерия
Этот вид изомерии вызван неодинаковым размещением лигандов во внутренней сфере относительно друг друга. Необходимым условием геометрической изомерии является наличие во внутренней координационной сфере не менее двух различных лигандов. Геометрическая изомерия проявляется преимущественно у комплексных соединений, имеющих октаэдрическое строение, строение плоского квадрата или квадратной пирамиды. С увеличением числа различных лигандов во внутренней сфере растет число геометрических изомеров.
[править] Оптическая изомерия
Оптическая изомерия связана со способностью некоторых комплексных соединений существовать в виде двух форм, не совмещаемых в трехмерном пространстве и являющихся зеркальным отображением друг друга, как левая рука и правая. Поэтому оптическую изомерию называют иногда еще зеркальной изомерией.
Структурная изомерия
Гидратная (сольватная) изомерия заключается в различном распределении молекул растворителя между внутренней и внешней сферами комплексного соединения, в различном характере химической связи молекул воды с комплексообразователем. Например: [Cr(H2O)6]Cl3 (фиолетовый), [Cr(H2O)5Cl]Cl2 ∙ H2O (светло-зеленый), [Cr(H2O)Cl2]Cl ∙ 2H2O (темно-зеленый).
Ионизационная изомерия определяется различным распределением заряженных лигандов между внутренней и внешней сферами комплекса и характеризует способность координационных соединений с одним и тем же элементным составом давать в растворе разные ионы. Примеры соединений: [Co(NH3)5Br]SO4 (красно-фиолетовый), [Co(NH3)5SO4]Br (красный).
Координационная изомерия связана с переходом лигандов от одного комплексообразователя к другому: [Co(NH3)6][Cr(CN)6] и [Cr(NH3)6][Co(CN)6].
[править]Электронные свойства
[править] Окраска
Окраска комплексных соединений зависит от типа лигандов и комплексообразователя. Из-за расщепления энергии d-орбиталей появляется возможность перехода электронов с подуровней dxy, dzy, dxz на вакантные подуровни с более высокой энергией dz2,dz2-y2 под действием поглощаемых квантов света. Эти явления можно наблюдать с помощью электронной спектроскопии. В зависимости от разности расщепленных уровней комплексы поглощаюткванты света определенных диапазонов длин волн, поэтому имеют соответствующую окраску.
[править]Применение
Комплексные соединения имеют важное значение для живых организмов, так гемоглобин крови образует комплекс с кислородом для доставки его к клеткам, хлорофилл находящийся в растениях является комплексом.
Комплексные соединения находят широкое применение в различных отраслях промышленности. Химические методы извлечения металлов из руд связаны с образованием КС. Например, для отделения золота от породы руду обрабатывают раствором цианида натрия в присутствии кислорода. Метод извлечения золота из руд с помощью растворов цианидов был предложен в 1843 г. русским инженером П. Багратионом. Для получения чистых железа,никеля, кобальта используют термическое разложение карбонилов металлов. Эти соединения - летучие жидкости, легко разлагающиеся с выделением соответствующих металлов.
Широкое применение комплексные соединения получили в аналитической химии в качестве индикаторов.
Многие КС обладают каталитической активностью, поэтому их широко используют в неорганическом и органическом синтезах. Таким образом, с использованием комплексных соединений связана возможность получения многообразных химических продуктов: лаков, красок, металлов, фотоматериалов, катализаторов, надежных средств для переработки и консервирования пищи и т.д.
Комплесные соединения цианидов имеют важное значение в гальванопластике, так как из обычной соли бывает невозможно получить настолько прочное покрытие как при использовании комплексов.
8 вопрос
Химическое превращение – это качественный скачок, при котором исчезают одни вещества и появляются другие. Происходящая при этом перестройка электронных структур атомов, ионов и молекул сопровождается выделением или поглощением тепла, света, электричества и т.д. – превращением химической энергии в другие виды энергии.
Энергетические эффекты химических реакций изучает термохимия. Данные об энергетических эффектах используются для выяснения направленности химических процессов, для расчета энергетических балансов технологических процессов и т.д. С их помощью можно рассчитать температуру горения различных веществ и материалов, температуру пожаров и т.п.
Состояние системы (вещества или совокупности рассматриваемых веществ) описывают с помощью ряда параметров состояния – t, p, m. Для характеристики состояния системы и происходящих в ней изменений важно знать также изменение таких свойств системы, как ее внутренняя энергия U, энтальпия Н, энтропия S, энергия Гиббса (изобарно-изотермический потенциал) G. По изменению этих свойств системы можно судить, в частности, об энергетике процессов.
Химические реакции обычно протекают при постоянном объеме V = const, DV = 0 (например, в автоклаве) или при постоянном давлении p = const (например, в открытой колбе), т.е. является соответственно изохорными или изобарными процессами.
Энергетический эффект химического процесса возникает за счет изменения в системе внутренней энергии U или энтальпии H. Внутренней энергией системы называют энергию всех видов движения и взаимодействия тел или частиц, составляющих систему (кинетическая энергия межмолекулярного взаимодействия, вращательная энергия, колебательное движение атомов и групп в молекуле, энергия взаимодействия электронов между собой и с ядрами).
Предположим, что некоторая система за счет поглощения теплоты q переходит из состояния 1 в состояние 2. В общем случае эта теплота расходуется на изменение внутренней энергии системы DU и на совершение работы против внешних сил А: 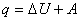 или
или 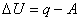 .
.
Приведенное уравнение выражает закон сохранения энергии (который называется также первым законом термодинамики), т.е. означает что сумма изменения внутренней энергии и совершенной системой (или над нею) работы равна сообщенной (или выделенной ею) теплоте. Так, если теплота сообщается газу в цилиндре, закрытом поршнем, то газ, во-первых, нагревается, т.е. его внутренняя энергия возрастает, а во-вторых, расширяется, т.е. производит работу подъема поршня А.
Вообще, следует отметить, что ни запасом теплоты, ни запасом работы система не обладает. Система обладает лишь запасом внутренней энергии, а теплота и работа показывают, каким способом изменяется внутренняя энергия системы.
Для химических реакций под работой против внешних сил в основном подразумевается работа против внешнего давления. В первом приближении (при p = const) она равна произведению давления р на изменение объема системы DV при переходе ее из состояния 1 в состояние 2:
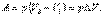
При изохорном процессе (V = const), поскольку изменения объема системы не происходит, А = 0. Тогда переходу системы из состояния 1 в состояние 2 отвечает равенство: 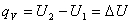 . Таким образом, если химическая реакция протекает при постоянном объеме, то выделение или поглощение теплоты qv связано с изменением внутренней энергии системы.
. Таким образом, если химическая реакция протекает при постоянном объеме, то выделение или поглощение теплоты qv связано с изменением внутренней энергии системы.
При изобарном процессе (p = const) тепловой эффект qр равен:
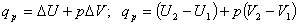 или
или
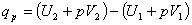 .
.
Введем обозначение 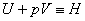 .
.
Тогда qp = H2 – H1 = DH.
Величину Н называют энтальпией. Энтальпию можно рассматривать как энергию расширенной системы. Таким образом, если при изохорном процессе энергетический эффект реакции равен изменению внутренней энергии системы 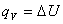 , то в случае изобарного процесса он равен изменению энтальпии системы
, то в случае изобарного процесса он равен изменению энтальпии системы  .
.
Химические и физические изменения в системе, как правило, сопровождаются выделением и поглощением теплоты. Наибольшую теплоту, которую можно получить при химическом процессе при данной температуре, называют тепловым эффектом процесса. Процессы в химии, при которых теплота выделяется, называются экзотермическими, а процессы, при которых теплота поглощается, - эндотермическими. Тепловые эффекты экзотермических реакций в термохимии принято считать положительными, а эндотермических функций – отрицательными. В отличие от термохимии в химической термодинамике, наоборот, положительные значения принимаются для тепла (Q), поглощенного системой. С целью согласовать систему знаков, будем тепловой эффект процесса обозначать через Q и считать, что
Q = -q, т.е. QV = -DU; QP = -DH
(В химической термодинамике: q – поглощаемая энергия - положительна; q - отдаваемая (излучаемая) энергия – отрицательна.)
Энергетический эффект реакции, протекающей при постоянном давлении, отличается от энергетического эффекта реакции, протекающей при постоянном объеме, на величину pDV. Для химического процесса, протекающего изобарически, DV представляет собой разность между суммой объемов исходных веществ и продуктов реакции. Так, для реакции, записанной в общем виде:
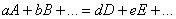 ,
,
изменение объема определяется равенством
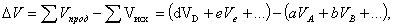
где VA, VB, …, VD, VE… - молярные объемы веществ A, B, …, D, E…; åVпрод – сумма молярных объемов продуктов реакции; åVисх – сумма молярных объемов исходных веществ.
Следует отметить, что подавляющее большинство химических реакций происходит при постоянном давлении. Поэтому таким реакциям в дальнейшем будет уделено наибольшее внимание.
Тепловые эффекты реакций определяют как экспериментально, так и с помощью термохимических расчетов. Абсолютные значения внутренней энергии и энтальпии определить невозможно. Однако для термохимических расчетов это несущественно, т.к. здесь представляет интерес энергетический эффект процесса, т.е. изменение состояния системы – изменение значений U и H (DU и DН).
При экзотермических реакциях теплота выделяется, т.е. уменьшается энтальпия, или внутренняя энергия системы, и значения DН и DU для них отрицательны.
При эндотермических реакциях теплота поглощается, т.е. Н и U системы возрастают, а DН и DU имеют положительные значения (это значит, что продукт реакции менее устойчив, чем исходное вещество).
Для того, чтобы можно было сравнивать энергетические эффекты различных процессов, термохимические расчеты обычно относят к 1 моль вещества и условиям, принятым за стандартные. За стандартные принимают давление 101325 Па и температуру 25 оС (298,15 К). Стандартные тепловые эффекты принято обозначать 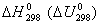 .
.
Уравнения химических реакций с указанием тепловых эффектов называют термохимическими уравнениями.
Термохимическое уравнение реакции синтеза 1 моля воды имеет вид:
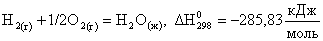 .
.
В термохимических уравнениях указывается также агрегатное состояние и полиморфная модификация реагирующих и образующихся веществ: г – газовое, ж – жидкое, к – кристаллическое и т.д.
В основе термохимических расчетов лежит закон, сформулированный Гессом Г.И. (1841):
Тепловой эффект зависит только от вида (природы) и состояния исходных веществ и конечных продуктов, но не зависит от пути процесса, т.е. от числа и характера промежуточных стадий.
Согласно закону Гесса, тепловые эффекты образования СО2 как непосредственно из простых веществ, так и через промежуточную стадию образования и сгорания СО равны
По приведенному равенству нетрудно вычислить одну из величин DН, зная две другие. Как известно, тепловые эффекты образования СО2 (DН1) и горения СО (DН3) определяются экспериментально. Тепловой же эффект образования СО (DН2) измерить невозможно, т.к. при горении углерода в условиях недостатка
Следствия из закона Гесса:
Тепловой эффект обратной реакции равен тепловому эффекту прямой реакции с обратным знаком, т.е. для реакций
Если в результате ряда последовательных химических реакций система приходит в состояние, полностью совпадающее с исходным (круговой процесс), то сумма тепловых эффектов этих реакций равна нулю, т.е. для ряда реакций
сумма их тепловых эффектов=0
В термохимических расчетах широко используют энтальпии (теплоты) образования веществ.
Под энтальпией образования понимают тепловой эффект реакции образования 1 моля вещества из простых веществ. Обычно используют стандартные энтальпии образования. Их обозначают 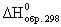 или
или 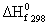 (часто один из индексов опускают; f – от англ. formation).
(часто один из индексов опускают; f – от англ. formation).
Стандартные энтальпии образования простых веществ, устойчивых в стандартных условиях (газообразный кислород, жидкий бром, кристалллический иод, ромбическая сера, графит и т.д.), принимают равными нулю.
Согласно закону Гесса тепловой эффект реакции равен сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ.
тепловой эффект DНх.р. определяется равенством
Энтальпии образования известны примерно для 4000 веществ в различных агрегатных состояниях. Это позволяет чисто расчетным путем установить энергетические эффекты самых разнообразных процессов.
Большинство процессов представляет собой два одновременно происходящих явления: передачу энергии и изменение в упорядоченности расположения частиц относительно друг друга.
Частицам (атомам, ионам) присуще стремление к беспорядочному движению, поэтому система стремится перейти из более упорядоченного состояния в менее упорядоченное.
Так, если, например, баллон с газом соединить с сосудом, то газ из баллона будет распределяться по всему объему сосуда. При этом система из более упорядоченного состояния (с меньшим беспорядком) переходит в состояние менее упорядоченное (с большим беспорядком).
Количественной мерой беспорядка является энтропия S.
Или другими словами: энтропия – мера неупорядоченности системы. Ее представляют как логарифмическое выражение вероятности существования вещества или различных его форм:
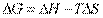 .
.
Характер изменения энергии Гиббса позволяет судить о принципиальной возможности или невозможности осуществления процесса. Условием принципиальной возможности являются неравенство:
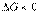 (условие самопроизвольности).
(условие самопроизвольности).
Иными словами, самопроизвольно протекают реакции, если энергия Гиббса в исходном состоянии системы больше, чем в конечном.
Пожарную опасность веществ и их смесей можно определить по энергии Гиббса 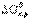 , которая является мерой реакционной способности веществ. Как было показано ранее, реакции между веществами, сопровождающиеся большой потерей энергии Гиббса, протекают самопроизвольно и до конца, иногда приобретают взрывной характер. В этих реакциях энергия Гиббса отрицательна, то есть в исходном состоянии системы (реагирующих веществ) она больше, чем в конечном (продуктов реакции).
, которая является мерой реакционной способности веществ. Как было показано ранее, реакции между веществами, сопровождающиеся большой потерей энергии Гиббса, протекают самопроизвольно и до конца, иногда приобретают взрывной характер. В этих реакциях энергия Гиббса отрицательна, то есть в исходном состоянии системы (реагирующих веществ) она больше, чем в конечном (продуктов реакции).
Ориентировочно за величину, определяющую направленность процесса, принимают значение 41,8 кДж/моль. Если для реакции расчетом получено 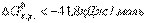 , то реакция возможна не только в стандартных, но и в нестандартных условиях.
, то реакция возможна не только в стандартных, но и в нестандартных условиях.
Если 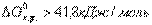 , то процесс невозможен как в стандартных, так и в иных условиях. По изменению энергии Гиббса от -41,8 до 41,8 кДж/моль нельзя сделать заключения о возможности протекания процесса в стандартных условиях, но вещества относятся к пожароопасным, хотя эти свойства у них появляются в условиях, отличных от стандартных (например, во время пожара).
, то процесс невозможен как в стандартных, так и в иных условиях. По изменению энергии Гиббса от -41,8 до 41,8 кДж/моль нельзя сделать заключения о возможности протекания процесса в стандартных условиях, но вещества относятся к пожароопасным, хотя эти свойства у них появляются в условиях, отличных от стандартных (например, во время пожара).
Если для веществ по расчету получено 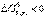 , то вещества, участвующие в реакции, пожароопасны и несовместимы. К совместному хранению такие вещества не допускаются. При
, то вещества, участвующие в реакции, пожароопасны и несовместимы. К совместному хранению такие вещества не допускаются. При 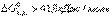 вещества совместимые и допускаются к совместному хранению.
вещества совместимые и допускаются к совместному хранению.
Теплотворная способность топлива.
Теплотворная способность топлива - количество теплоты, выделяемое при сжигании 1 кг. твердого или 1 куб.м. газообразного топлива. Теплотворность каждого вида топлива зависит:
- от его горючих составляющих: углерода, водорода, летучей горючей серы и др.; а также
- от его зольности и влажности.
Теплотворная способность топлива Качество топлива характеризуется его теплотворной способностью Q и измеряется количеством тепла, выделяющегося при полном сгорании 1 кг твердого или жидкого или I нормального кубического метра (1 нм3)1 газообразного топлива. Для твердого и жидкого топлива эта величина имеет размерность ккал1кг, для газообразного — ккал/нм3.Теплотворная способность рабочей массы топлива обозначается: <?р ккал/кг — для твердого и жидкого топлива и Qp ккал1нм3 — для газообразного.Принято считать, что если теплотворная способность топлива учитывает, кроме тепла, выделившегося при его сгорании, также и тепло, полученное при преобразовании продуктов горения в воду при 100°С, то такая теплотворность называется высшей (QP).
Если при определении теплотворной способности топлива было учтено тепло, расходованное на испарение влаги, такая теплотворность называется низшей (Qp). При практических расчетах пользуются последней.
Теплотворная способность твердого и жидкого топлива определяется либо опытным путем, либо расчетным по формуле Д. И. Менделеева:
Qp = 81Ср + 300НР — 26(0? — SP) ККАЛ/КГ;
Qp = 81Ср + 300НР — 26(Ор — Sp) — 6(9Нр +WP) ККАЛ/КГ
Теплотворная способность газообразного топлива определяется по формулам, полученным методом суммирования произведений тепловых эффектов горения газов на их процентное содержание:
QB = 30.5СО + 30,5Н2 + 95,ЗСН4 + 152,5С2Н4 + 4- 60,0H2S ККАЛ/НМ3;
Q„ = 30.5СО + 25,8Н2 + 85,9СН4 + 143,0С2Н4 + 4- 55,2H2S ККАЛ/НМ3.
Для сравнения тепловой ценности различных видов топлива применяется общая единица измерения—так называемое условнее топливо, теплотворная способность которого 7000 ккал/кг. Для перевода любого топлива в условное необходимо действительную теплотворную способность разделить на 7000 ккал/кг. Полученное отношение называется калорийным эквивалентом. Естественно, что чем больше калорийный эквивалент топлива, тем оно ценнее.Теплотворная способность и калорийные эквиваленты некоторых наиболее распространенных видов топлива приведены в табл. у. Сжигание топлива и использование тепла отходящих газовТеплотворная способность и калорийные эквиваленты некоторых видов топлива
Горение топлива начинается только в том случав,- когда температура в топливосжигающем устройстве доведена до температуры воспламенения. Последняя величина переменная и зависит от вида топлива и условий, в которых совершается процесс горения.Горение топлива считается полным, если в продуктах горения произошло окисление горючих составляющих до ССЬ, ШО, SO2 и -при этом отсутствует свободный кислород.Зная состав топлива, можно подсчитать по формулам, приведенным в специальной литературе, теоретическое количество воздуха, необходимое для полного его сжигания. Так как практически нельзя достичь равномерного смешения воздуха с горючими составляющими топлива, то для обеспечения полного его сгорания необходимо подвести большее количество возудха по сравнению с теоретически необходимым.Отношение количества практически подведенного воздуха 1пр к количеству теоретически необходимому LTeop называется коэффициентом" избытка воздуха:
Величина коэффициента избытка воздуха колеблется в пределах от 1,03 до 1,7. Нижний предел относится к газообразному и жидкому топливу, верхний — к твердому топливу.
Следует помнить, что увеличение избытка воздуха вызывает дополнительный расход тепла для его нагрева, а также увеличение количества отходящих продуктов горения, которые уносят большое количество тепла в атмосферу и тем самым снижают температуру нагревательной среды печи. Поэтому необходимо всегда стремиться к полному сжиганию топлива при минимальном коэффициенте избытка воздуха.
Критерием полноты горения служит цвет пламени. При недостатке воздуха пламя длинное, красного цвета с черными прожилками. Большой недостаток воздуха вызывает неполное сгорание топлива и появление черного дыма.При избытке воздуха получается короткое, острое (колючее) пламя с ярко светящимися язычками. Такое пламя нагревает маталл неравномерно, вызывает местный его перегрев и даже оплавление. При этом увеличивается расход топлива, угар металла и вместе с тем снижается температура в печи.
Пламя молочно-белого цвета, без ярких языков в топливо-сжигающем устройстве является признаком оптимального количества воздуха
12 вопрос
Скорость химической реакции (v) характеризуется изменением концентрации реагирующих веществ (моль/л или моль/см3) в единицу времени (сек., мин., ч.).
Для гомогенной (однородной) системы скорость химической реакции измеряется количеством веществ, вступивших в реакцию или образовавшихся в результате реакции за единицу времени в единице объема системы. Для гетерогенной системы скорость химической реакции измеряется количеством веществ, вступивших в реакцию или образовавшихся в результате реакции за единицу времени на единице поверхности раздела фаз.
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 705; Нарушение авторских прав?; Мы поможем в написании вашей работы!