
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Применение первого закона термодинамики к различным тепловым процессам в идеальном газе
|
|
|
|
Применение первого закона термодинамики к различным процессам;
Формула 4 — элементарный заряд
Формула 3 — электрическая постоянная
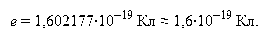
Направление силы зависит от знака заряда. Если заряды одноименные, то есть одинакового знака, то они отталкиваются. Если разноименные то притягиваются. Сила Кулона направлена по прямой линии, которая соединяет заряды. В случае одноименных зарядов Кулоновская сила направлена вдоль радиус вектора проведенного из одного заряда к другому.

Рисунок — 1 определение направления силы Кулона
Первый закон (первое начало) термодинамики — это закон сохранения и превращения энергии в применении к тепловым процессам.
Если механическая энергия системы не изменяется, а система не замкнута и между ней и окружающей средой происходит теплообмен, то изменяется внутренняя энергия:
Δ U = Q + Avn. (1)
Уравнение (1) — первый закон термодинамики, который формулируется так: изменение внутренней энергии при переходе термодинамической системы из одного состояния в другое равно работе внешних сил и количеству теплоты, переданному термодинамической системе в процессе теплообмена.
Если вместо работы внешних сил A vn ввести работу A системы над внешними телами А = - A vn, то выражение (1) запишется:
Q =Δ U + A. (2)
Тогда первый закон термодинамики можно сформулировать так: количество теплоты, сообщенное термодинамической системе, идет на изменение ее внутренней энергии и на совершение работы системой против внешних сил.
Из первого закона термодинамики вытекает невозможность создания вечного двигателя первого рода, т.е. такого двигателя, который совершал бы работу без затраты энергии извне.
|
|
|
Действительно, если к системе не подводится энергия (Q = 0), то A = -Δ U и работа может быть совершена за счет убыли внутренней энергии системы. После того как запас энергии окажется исчерпанным, двигатель перестанет работать.
Если система замкнута (A vn = 0) и теплоизолирована (Q = 0), то первый закон термодинамики будет иметь вид:
Δ U =0.
Если в такой системе имеются тела с различной температурой, то между ними будет происходить теплообмен: тела, у которых температура выше, будут отдавать энергию и охлаждаться, а тела с меньшей температурой будут получать энергию и нагреваться. Это будет происходить до тех пор, пока температуры у всех тел не станут одинаковыми. При этом
Δ U 1+Δ U 2+…+Δ Un =0
или
Q 1+ Q 2+…+ Qn =0.(3)
Первый закон термодинамики (3) для замкнутой и адиабатически изолированной системы называют уравнением теплового баланса. Выражение (3) представляет собой алгебраическую сумму: слагаемые, соответствующие нагреванию, парообразованию, плавлению, положительны, а соответствующие охлаждению, конденсации, кристаллизации, — отрицательны.
1) Изохорный процесс.
Объем не изменяется: V = const => Δ V = 0 — работа не совершается. Первый закон термодинамики будет иметь вид:
Q =Δ U.
При изохорном процессе энергия, сообщаемая газу путем теплообмена, расходуется целиком на увеличение его внутренней энергии, причем согласно (1)
Δ U = i 2 mMR Δ T.
2) Изотермический процесс.
Температура газа не изменяется: Τ = const. Следовательно, Δ U = 0. Первый закон термодинамики имеет вид:
Q = A.
При изотермическом процессе все подведенное к газу количество теплоты идет на совершение газом работы.
3) Изобарный процесс.
Давление не изменяется: p = const.
При расширении газ совершает работу Α = pΔ V и нагревается, т.е. изменяется его внутренняя энергия:
Δ U = i 2 mMR Δ T.
Первый закон термодинамики запишется так:
Q = A +Δ U.
При изобарном процессе подведенное к газу количество теплоты частично идет на увеличение его внутренней энергии, а частично на работу, совершаемую газом в процессе его расширения.
|
|
|
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 1001; Нарушение авторских прав?; Мы поможем в написании вашей работы!