
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ход работы
|
|
|
|
Билет № 9
ЭТАЛОН ОТВЕТА К БИЛЕТУ №9
Ход работы
Билет № 8
ЭТАЛОН ОТВЕТА К БИЛЕТУ №8
Билет № 7
ЗАДАНИЕ №1
Текст задания:
1.
2.
ЗАДАНИЕ №2
Текст задания:
1.Задача
Вычислить тепловой эффект реакции горения ацетилена и составьте термохимическое уравнение этой реакции, если известно, что при сжигании 1,12 л (н.у.) ацетилена выделяется 67,5 кДж.
| Дано: V(С2Н2) = 1,12 л Q = 67,5 кДж | Решение: n(С2Н2) = 1,12 л / 22,4 л/моль = 0,05 моль Уравнение реакции горения ацетилена: 2С2Н2 + 5O2 → 4СO2 + 2Н2O + Q При горении 0,05 моль С2Н2 выделяется 67,5 кДж При горении 2 моль С2Н2 выделяется Х кДж Х = 2·67,5 / 0,05 = 2700 Q = 2700 кДж Термохимическое уравнение реакции: 2С2Н2 + 5O2 → 4СO2 + 2Н2O + 2700 кДж | |
| Найти: Qреакции -? | ||
| Ответ: Q = 2700 кДж |
ЗАДАНИЕ №1
Текст задания:
1.
2.
ЗАДАНИЕ №2
Текст задания:
1.Опыт:
Получите амфотерный гидроксид и проделайте реакции, характеризующие его свойства (гидроксид алюминия).
Реактивы:
· раствор NaOH,
· раствор AlCl3,
· раствор HCl.
Оборудование:
· штатив с пробирками,
· спиртовка,
· держатель для пробирок.
1) Получаем гидроксид меди:
3NaOH + AlCl3 → ↓Аl(OH)3 + NaOH
2) Доказываем амфотерность Аl(OH)3, для этого разделяем полученный осадок на две пробирки и добавляем раствор соляной кислоты и избыток гидроксида натрия – происходит растворение осадка в обоих случаях, т. е. проявление кислотных и основных свойств:
Аl(OH)3 + 3НСl → AlCl3 + 3H2O
Al(OH)3 + NaOH → NaAlO2 + 2H2O
ЗАДАНИЕ №1
Текст задания:
1.
2.
ЗАДАНИЕ №2
Текст задания:
1.Опыт:
Распознайте с помощью характерных реакций растворы глицерина и глюкозы.
Реактивы:
· раствор глюкозы,
· раствор сульфата меди (II),
· раствор гидроксида натрия,
· глицерина.
Оборудование:
· штатив с пробирками,
· спиртовка,
· держатель для пробирок.
Глицерин и глюкоза являются многоатомными спиртами, поэтому при добавлении к осадку гидроксида меди (II) происходит растворение осадка и появление яркосинего (василькового) окрашивания. Но в отличие от глицерина, глюкоза имеет альдегидную группу, поэтому при нагревании в пробирке с глюкозой происходит появление красного окрашивания, а в пробирке с глицерином - не происходит.
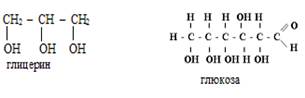
1) Получаем гидроксид меди(II):
СuSO4 + 2NaOH 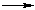 Cu(OH)2↓ + Na2SO4
Cu(OH)2↓ + Na2SO4
2) Добавляем глицерин:
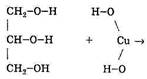 | 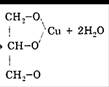 | ||
Васильковый глицерат меди
3) Добавляем глюкозу:
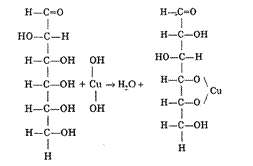 |
4) Нагреваем пробирки:
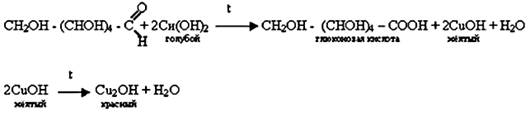 |
|
|
|
|
|
Дата добавления: 2015-04-24; Просмотров: 738; Нарушение авторских прав?; Мы поможем в написании вашей работы!