
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вопрос73
Вопрос 72
Датский физик Нильс Бор (1885–1962) в 1913 г. создал первую квантовую теорию атома, связав в единое целое эмпирические закономерности линейчатых спектров водорода, ядерную модель атома Резерфорда и квантовый характер излучения и поглощения света.
В основу своей теории Бор положил три постулата
Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн.
В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантованные значения момента импульса, удовлетворяющие условию mvr=nћ (n=1.2.3…)
где т, - масса электрона, v - его скорость по n-й орбите радиуса rn,
ℏ = h/(2p).
Второй постулат Бора (правило частот): при переходе электрона с одной стационар ной орбиты на другую излучается (поглощается) один фотон с энергией hv=Eп-Еm
равной разности энергий соответствующих стационарных состоянии (Еn и Еm- соответственно энергии стационарных состояний атома до и после излучения (поглощения)). При Ет<Еп происходит излучение фотона (переход атома из состояния с боль шей энергией в состояние с меньшей энергией, т. с. переход электрона с более удален ной от ядра орбиты на более близлежащую), при Ет>Еn - его поглощение (переход атома в состояние с большей энергией, т. е. переход электрона на более удаленную от ядра орбиту). Набор возможных дискретных частот v = (Еn – Еm)/hквантовых переходов и определяет линейчатый спектр атома.
Будучи уверенным, что постоянная Планка должна играть основную роль в теории атома, Бор ввел третий постулат (правило квантования): на стационарных орбитах момент импульса электрона Ln= meυnrn кратен величине = h/(2π), то есть
meυnrn = nh, n = 1, 2, 3, …,
где = 1,05 · 10-34 Дж · с – постоянная Планка (величина h/(2π)) встречается столь часто, что для нее введено специальное обозначение («аш» с чертой; в данной работе «аш»– прямое); m е = 9,1 · 10-31 кг – масса электрона; r п – радиус n-й стационарной орбиты; υ n – скорость электрона на этой орбите.
Во́лны де Бро́йля — волны, связанные с любыми микрочастицами и отражающие их волновую природу. Каждую движующейся частице,обладающей импульсом p и энергией Е сопоставляется волновой процесс, называемый волной де Бройля. Длина волны де Бройля λ=ћ/р
А частота V=E/ћ е 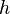 — постоянная Планка
— постоянная Планка
Фазовая скорость волны де Бройля v=E/p=C^2/v, где v- скорость частицы
Групповая скорость волны u=pc^2/Е=v
Волна де Бройля является не материальной и ее часто называют волной вероятности
Физ смысл- интенсивность волны де Бройля (квадрат амплитуды волны) определяет плотность вероятности обнаружения частицы в той или иной точке пространства
Для частиц не очень высокой энергии, движущихся со скоростью v<<c (скорости света), импульс равен p=mv (где m — масса частицы), и. λ=ћ/р = λ=ћ/mv Следовательно, длина волны де Бройля тем меньше, чем больше масса частицы и её скорость.
Первое подтверждение гипотезы де Бройля было получено в 1927 году в опытах американских физиков К. Дэвиссона и Л. Джермера. Пучок электронов ускорялся в электрическом поле с разностью потенциалов 100—150 В (энергия таких электронов 100—150 эВ, что соответствует λ=0.1 нм) и падал на кристалл никеля, играющий роль пространственной дифракционной решётки. Было установлено, что электроны дифрагируют на кристалле, причём именно так, как должно быть для волн, длина которых определяется соотношением де Бройля.[1]
В основу теории — волновой, или квантовой механики — и легла концепция де Бройля. Это отражается даже в названии «волновая функция» для величины, описывающей в этой теории состояние системы. Квадрат модуля волновой функции определяет вероятность состояния системы, и поэтому о волнах де Бройля часто говорят[3] как о волнах вероятности (точнее, амплитуд вероятности). Для свободной частицы с точно заданным импульсом p (и энергией E), движущейся вдоль оси 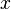 , волновая функция имеет вид[1]:
, волновая функция имеет вид[1]:
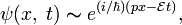 Ѱ(x.t)~e^(i/ћ)(px-Et)
Ѱ(x.t)~e^(i/ћ)(px-Et)
где t — время,.ћ=h/2П
В этом случае, IѰI^2= const то есть вероятность обнаружить частицу в любой точке одинакова.
Корпускуля́рно-волново́й дуализм – Электромагнитное излучение имеет двойственную природу, то есть оно обладает волновыми свойствами(интерференция,дифракция) и корпускулярными и квантовыми свойствами (тепловое излучение черного тепла, внешний фотоэффект, эффект Комптона и др), Эту двойственность электромагнитного излучения называют корпускулярно-волновым дуализмом E= hv
Соотношение неопределенности Гейзенберга
Следствие волновых свойств микрочастиц является соотношение неопределенности Гейзенберга
Нельзя одновременно точно опредилить координату частицы (x.y.z.)и соответсвующую проекцию импульса (Рх,Ру,Рz), причем удовлетворенности удовлетворяют условию
∆Px*∆x>=ћ
∆Py*∆y>=ћ
∆Pz*∆z>=ћ
∆Px- неопределенность импульса частицы в проекции на ось х
∆х- неопределенность координаты частицы
Для неопределенности энергии частицы ∆Е в некотором стационарном состоянии и промежутка времени ∆t, в течение которого частицы находятся в этом состоянии, также выполняется соотношение неопределенностей ∆E*∆t=>ћ
Чем больше время жизни частицы в данном стационарном состоянии, тем меньше неопределенность энергии частицы в этом стационарном состоянии
|
|
Дата добавления: 2015-04-24; Просмотров: 428; Нарушение авторских прав?; Мы поможем в написании вашей работы!