
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Іонообмінна хроматографія
|
|
|
|
РІДИННА ХРОМАТОГРАФІЯ
Сорбційні методи аналізу розчинених в рідині речовин назвають методами рідинної хроматографії. В якості сорбентів використовують тверді гранульо-вані речовини, спеціальний папір, тонкий шар тонкодисперсних твердих ре-човин, закріплений на плоскій інертній підложці; органічні розчинники, які не змішуються з РФ. Сорбенти не повинні змішуватись з РФ, повинні бути механічно та хімічно стійкими в умовах аналізу, забезпечувати необхідну се-лективність та ефективність. Рідинну хроматографію проводять в колоночному та площинному варіантах.
Колоночну хроматографію проводять за наступною схемою: скляну трубку діаметром 0,2-5 см і довжиною 2-100 см заповнюють НФ, а РФ переміщується через НФ під дією сили тяжіння (класичний варіант) або під тиском до 40 МПа (високоефективна рідинна хроматографія ВРХ). На виході з колонки відбирають проби елюата і аналізують їх за допомогою різних хімічних або фізико-хімічних методів.
Цей метод базується на хімічній реакції об-міну іонами між твердими гранульованими сорбентами (іонітами) і розчина-ми електролітів. Іоніти практично нерозчинні в РФ, з якими вони контактують. Основу гранули іоніту складає полімерний каркас (матриця), на якому закріплені функціональні групи. Заряд цих груп компенсується зарядом іонів протилежного знаку (протиіонів) і в цілому гранула іоніту нейтральна. Про-тиіони можуть заміщуватись на іони такого ж знаку при проходженні РФ че-рез іоніт. Протиіон функціональної групи визначає іонну форму іоніту.
Процес іонного обміну проходить такі головні стадії: 1) переміщення (дифузія) іона–витіснювача з розчину до функціональної групи гранули іоніту і витіснення протиіону; 2) переміщення витісненого протиіону з об’єму гранули іоніту до її поверхні; 3) дифузія витісненого іону з поверхні гра-нули іоніту в об’єм РФ.
|
|
|
Іоніти в залежності від природи функціональних груп можуть обмінюва- тись з розчином: катіонами (катіоніти), або аніонами (аніоніти). Катіоніти мають функціональні групи кислотної природи (-SO3-, -AsO32-, -PO32-, –COO-, –O-, -CH2COO- та ін.) і в якості протиіонів - катіони. Аніоніти містять функціональні групи основної природи (=N+=, =S+-, =P+=, –NH3+, =NH2+, ≡NH+ та ін.) і містять в якості протиіонів - аніони.. Іоніти, які мають групи кислотної і основної природи, обмінюються з розчином катіонами і аніонами (амфоліти). Властивості іонітів мають природні речовини (силікагелі, бентоніти, глини, модифікована целюлоза, активоване вугілля та ін.). Однак вони, як правило, мають невелику обмінну ємність і не завжди відповідають вимогам до сорбентів. Найбільшого поширення набули синтетичні іоніти – високомолекулярні органічні речовини тривимірної структури. Їх отримують методами поліконденсації або емульсійної полімеризації органічних мономерів (стирол, дивінілбензол, фенолформальдегідні смоли та ін.). Процес іонного обміну відображають рівняннями хімічних реакцій:
катіонний обмін R-H + NaCl = R-Na + HCl
2R–Na + ZnSO4 = R2–Zn + Na2SO4
де R-H, R-Na, R2 – Zn – умовні позначення катіоніту в водневій, натрієвій, цинковій формах;
аніонний обмін: R-OH + NaCl = R-Cl + NaOH
2R–Cl + Na2SO4 = R2–SO4 + 2NaCl
де – R – OH, R – Cl, R2 – SO4 – умовні позначення аніоніту в гідроксильній, хлоридній, сульфатній формах.
Процеси іонного обміну проводять в умовах, які забезпечують строгу сте- хіометричність реакцій. Константа рівноваги іонного обміну описується рів- нянням Нікольського
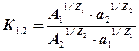
де А1, А2 - активності іонів сорбату і протиіонів в НФ; а1, а2 – активності іонів сорбату і протиіонів в РФ; z1, z2 - заряди іону сорбату і протиіону.
Кожний іон має певний коефіцієнт розподілу, за величинами яких роблять висновки про можливість розділення суміші іонів. Розділення іонів тим ефективніше, чім більше різниця в їх коефіцієнтах розподілу. Відношення кое-фіцієнтів розподілу двох іонів називають коефіцієнтом розділення іонів, який залежить від концентрації іонів в РФ, ступеня дисоціації функціональних груп іоніту, рН, іонної сили розчину, температури.
|
|
|
Підготовка іонітів до роботи полягає в замочувані їх в 5% -ному розчині хлориду натрію на 24 – 48 годин для набухання, очищенні їх від органічних і неорганічних домішок послідовним промиванням розчинами гідроксиду натрію і хлороводню (2 моль/л). Надлишки реагентів вимивають дистильова-ною водою. Очищений іоніт переводять у необхідну іонну форму, промива- ючи його розчином відповідного електроліту. Іоніти можна багаторазово переводити з однієї іонної форми в іншу (регенерувати) практично без зміни їх сорбційних характеристик.
Іонний обмін в практиці аналізу застосовують для розділення сумішей
іонів, концентрування мікроелементів, видалення домішок. Цей процес широ ко застосовують для очищення води, технологічних розчинів, синтезу складних речовин тощо.
Гель-проникаюча хроматографія (молекулярне сито)
Заснована на розподілі сорбатів між РФ, яка оточує гранули гелю (набухлої структурованої сис-теми, яка має пори певного розміру) і розчинником, який знаходиться в порах гелю. Розділення сорбатів залежить від співвідношення розмірів їх молекул та пор гелю. Першими виходять з НФ молекули з розмірами більшими за діаметр пор гелю, оскільки вони не проникають в пори і швидко рухаються по каналам між гранулами гелю. Молекули з розмірами близькими або меншими за діаметр пор гелю частково або повністю проникають в пори гелю і процес їх розділення буде залежати від їх коефіцієнтів дифузії D
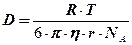 .
.
де R – універсальна газова стала; T –абсолютна температура, оК; η – в’язкість середовища; π = 3,14; r – радіус молекули; NA – число Авогадро.
Гел і, які використовують поділяють на: м’які – високомолекулярні органічні речовини з невеликою кількістю поперечних зв’яків, які значно збільшують об’єм при набуханні (сефадекси, агарові гелі, крохмаль та ін.); напівжорсткі – продукти сополімеризації стиролу та дивініл бензолу з великою кількістю поперечних зв’язків, які несуттєво (не більше, ніж в два рази) збільшують свій об’єм при набузанні; жорсткі – мають фіксований розмір пор і не набухають в розчиннику (силікагелі, пористе скло).
|
|
|
Розчинники, які використовують в гель-проникаючій хроматографії повин ні розчиняти всі компоненти суміші, змащувати гель і не сорбуватись на його поверхні.
Гель-проникаючу хроматографію використовують для визначення молеку- лярних мас білків, полімерів, вуглеводнів та ін. При цьому використовують лінійну залежність об’єму виходу речовини від її молекулярної маси
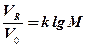 ,
,
де VR, V0 - об’єми виходи речовини, що визначається, і високомолекулярної речовини,яка не здатна проникати в пори гелю; k – коефіцієнт пропорційно- сті; M – молекулярна маса речовини, яку визначають.
Площинна хроматографія. Схема методу полягає в наступному: на стар- тову лінію (або точку) плоского сорбенту наносять невеликий об’єм проби, а потім край сорбенту занурюють в чистий розчинник (або наносять його пор- ціями на точку старту) (рис. 25). Під дією капілярних сил розчинник рухаєть ся вздовж шару сорбенту і з різною швидкістю переносить компоненти сумі- ші, що приводить до їх просторового розділення. Коли фронт розчинника
досягає лінії фінішу хроматограму підсушують, обробляють реагентами
(проявниками), які утворюють з сорбатами забарвлені сполуки (якщо компо ненти суміші незабарвлені) і аналізують
Якісний аналіз проводять по величині фактору запізнення Rf, який є інди-відуальною характеристикою речовини: Rf = a/b, де а – відстань від лінії (точки) старту до лінії фінішу (шлях, який пройшов розчинник); в – відстань від лінії (точки) старту до центру хроматографічної плями (шлях, який пройшла речовина). Ідентифікацію речовин проводять, порівнюючи їх фактори запізнення із стандартами або по характерному забарвленню хроматографіч-них плям.
Кількісний аналіз можна виконувати безпосередньо на сорбенті або в елюаті після вимивання сорбату з нього.
|
|
|
При проведенні аналізу безпосередньо на площині вімірюють площу хро- матографічної плями і знаходять масу речовини по градуйовочному графіку, побудованому в координатах:: площа плами – масса речовини. Також за допомогою денсиметру можна виміряти оптичну густину сорбенту в центрі плями і знайти масу речовини за градуйовочним графіком: оптична густина – маса речовини.
Найбільш точним вважається метод, в якому сорбати після розділення вимивають з сорбенту відповідним розчинником і аналізують отриманий елю ат фізико-хімічними методами аналізу (спектрофотометрія, електрохімія).
До аналізуємих систем в площинній хроматографії пред’являють наступні вимоги: 1) значна відмінність факторів запізнення (від 0,05 до 0,9), що приводить до розміщення сорбатів по всій довжині сорбенту; 2) розділення двух речовин можливе, якщо в вибраних умовах Rf 1 - Rf 2 > 0.05; 3) ізотерми сорбції речовин повинні бути лінійними, а плями мати круглу форму і невеликий розмір; 4) органічний розчинник не повинен взаємодіяти з реагентом-проявником; 5) склад рідких фаз повинен бути сталим на протязі аналізу.
В паперовій хроматографії в якості сорбенту використовують папір спе-
ціальних сортів, який відповідає наступним вимогам: відсутність зольних та органічних домішок; однорідність по товщині; забезпечення певної швидко- сті руху розчинника; відсутність хімічної взаємодії з рухомим розчинником та речовиною, що аналізується; можливість чіткого розділення речовин.
Хроматографічний папір виробляють з високосортної бавовни. Найчіткі- ше розділення речовин спостерігається, коли напрямок руху розчинника спів падає з напрямком розташування волокон паперу. Для розділення гідрофоб- них речовин папір імпрегнують різноманітними гідрофобними речовинами (нафталіном, парафіном, розчином каучуку та ін.).
Для розділення багатьох речовин використовують полярні розчинники або їх суміші (спирти, прості та складні ефіри, кетони, органічні основи, хлоро- форм, трибутифосфат). Всі ці розчинники насичують водою і мінеральними кислотами для попередження гідролізу, створення умов утворення комплек- сів металів, необхідного рН середовища та ін.
В тонкошаровій хроматографії в якості сорбентів використовують тонко дисперсні силікагель, оксид алюмінію, крохмаль, целюлозу та інші речовини з високою сорбційною здатністю. Їх наносять тонким шаром (0,1 – 10 мм) на підложку (пластинку) з скла, алюмінієвої фольги або поліефірної плівки у вигляді пасти(закріплений шар) або порошку (незакріплений шар). Сорбент з силікагелю може бути виготовленим при плавленні на скляний пластинці.
Вибір розчинника залежить від природи сорбенту і сорбату.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 1865; Нарушение авторских прав?; Мы поможем в написании вашей работы!