
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Другий закон термодинаміки. Ентропія
|
|
|
|
Теоретична частина
Висновок про недостатність першого закону термодинаміки для визначення напрямку і межі перебігу процесів привів до встановлення другого закону термодинаміки. Останній, як і перший закон, є постулатом. Доказом другого закону термодинаміки може служити те, що всі висновки, що витікають з нього, до цього часу завжди знаходили підтвердження на досліді. У середині XIX ст. Р. Клаузіус, У. Томсон і Дж. Максвел показали, що другий закон термодинаміки – це один із найбільш загальних законів природи. Можливість, напрямок і межу перебігу самодовільного процесу визначає другий закон термодинаміки.
Запропоновано багато різних формулювань другого закону термодинаміки. Всі вони рівноцінні і можуть бути виведені логічно один з другого. Наведемо найбільш поширені з них:
· єдиним результатом будь-якої сукупності процесів не може бути перехід теплоти від холодного тіла до гарячого (Р. Клаузіус, 1850 р.);
· теплота найбільш холодного із тіл, що беруть участь у процесі, не може бути джерелом роботи (У. Томсон, 1851 р.);
· єдиним результатом будь-якої сукупності процесів не може бути негативний процес.
Для кількісної характеристики процесу розсіювання енергії у 1865 р. німецьким фізиком Р. Клаузіусом була введена нова термодинамічна функція, яку він назвав ентропією і позначив літерою S:

Ентропія – функція стану, тому її зміна не залежить від шляху процесу, а визначається тільки початковим і кінцевим станами системи.
Математичний вираз другого закону термодинаміки для оборотних і необоротних процесів має вигляд:
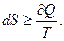
За фізичним змістом ентропія – це кількість зв'язаної енергії, віднесена до одного градусу:

Зв'язана енергія – це та частка внутрішньої енергії, яка не може бути перетворена в корисну роботу:
|
|
|
U = F + q,
де q – зв'язана енергія; F – вільна енергія, за рахунок якої можна виконати роботу.
Ентропія – екстенсивна властивість системи і виражається в Дж/(моль∙К).
Співвідношення другого закону термодинаміки приводить до висновку, що в адіабатних процесах (¶Q = 0) і dS ≥ 0.
Тобто ентропія ізольованої системи в оборотних процесах не змінюється (S2 = S1),а в необоротних (самодовільних) – збільшується (S2 > S1).
При цьому самодовільний процес відбувається доти, поки система не перейде в рівноважний стан, в якому ентропія досягає максимуму.
Отже, в ізольованих системах, для яких V = const і U = const, напрям перебігу самодовільних процесів визначається зміною ентропії.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 4676; Нарушение авторских прав?; Мы поможем в написании вашей работы!