
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рівняння ізотерми хімічної реакції
 |
З термодинамічних позицій стан рівноваги можна характеризувати також зміною термодинамічних потенціалів ( Δ G, Δ F) або величиною максимальної роботи хімічної реакції.
Максимальна робота хімічної реакції при постійній температурі складається з алгебраїчної суми усіх робіт, що виконують компоненти системи при переході від вихідних парціальних тисків або концентрацій до рівноважних:
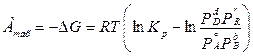 .
.
При постійних V і Т данерівняння набуває такого вигляду
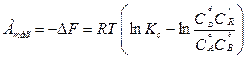 .
.
Дані рівняння називають рівняннями ізотерми хімічної реакції, або рівняннями Вант-Гоффа. Вони показують залежність між зміною термодинамічного потенціалу (ΔG або ΔF), константою хімічної рівноваги (Кр або Кс) і величиною парціальних тисків (концентрацій) складових реакції у вихідному стані.
За рівнянням ізотерми хімічної реакції можна розрахувати зміну енергій Гіббса і Гельмгольца і відповідно з'ясувати можливість, напрямок і межу перебігу довільного процесу.
При значеннях концентрацій або парціальних тисків компонентів, рівних одиницям, рівняння ізотерми хімічної реакції дають відповідно вирази для стандартного ізохорного потенціалу реакції
∆F0 = – RT ln Kc
і стандартного ізобарного потенціалу реакції
∆G0 = – RT ln Kр.
Величини стандартних потенціалів відображають властивість речовин вступати у взаємодію і є мірою хімічної спорідненості. Хімічні реакції здійснюються самочинно при позитивних значеннях максимальної роботи.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 2943; Нарушение авторских прав?; Мы поможем в написании вашей работы!