
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вплив температури на швидкість реакції
Теоретична частина
ЗАНЯТТЯ № 9
Тема: Вплив температури на швидкість хімічних реакцій. Каталіз. Ферментативний каталіз. Визначення температурного коефіцієнту та енергії активації розкладу тіосульфатної кислоти.
Актуальність: Температура є важливим фактором впливу на перебіг фізико-хімічних та біологічних процесів. У фармації на впливові температурного фактору на швидкість хімічної реакції грунтується метод “прискореного старіння ліків” який застосовують для визначення строків придатності лікарських засобів. Цей метод дозволяє скоротити час, необхідний для встановлення строку придатності ліків, і визначити оптимальну температуру їх зберігання.
Швидкість протікання біохімічного процесів в багатьох випадках пов'язана з каталітичною дією хімічних речовин, як неорганічного, так і органічного походження, які виступають в якості регулятора цих процесів. Тому визначення активності каталізаторів та ефективності їх дії має важливе діагностичне значення і широко практикується в клінічних лабораторіях. Крім цього, каталізатори знайшли широке використання у виробництві лікарських речовин: фенацетину, гвалколу, аміназину, галогенпохідних ароматичних сполук та ін.
Навчальні цілі:
Знати:
- правило Вант-Гоффа, методи визначення температурного коефіцієнту реакції;
- рівняння Арреніуса, фізичний зміст енергії активації та передекспоненційного множника;
- методи розрахунку енергії активації та передекспоненційного множника;
- основні положення теорії зіткнень, розрахунок констант швидкості хімічних реакцій, фізичний зміст передекспоненційного множника, поняття про стеричний фактор;
- основні положення теорії зіткнень, розрахунок константи швидкості, поняття про ентропію активації;
- основні положення каталізу.
Вміти:
- за даними кінетичних досліджень визначити температурний коефіцієнт та енергію активації реакції;
- розрахувати константу швидкості реакції, вказавши її розмірність.
Температура дуже впливає на константу швидкості реакції, як правило, вона із зростанням температури збільшується. У відповідності з емпіричним правилом Вант-Гоффа при підвищенні температури на кожні 10 °С константа швидкості збільшується у 2 – 4 рази:
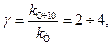
де γ – температурний коефіцієнт швидкості реакції.
При підвищенні температури на n десятків градусів рівняння приймає вигляд:
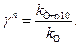
Але при високих температурах температурний коефіцієнт швидкості перестає бути сталим та знижується до одиниці. Тобто ця залежність виконується при не дуже великих температурах.
На правилі Вант-Гоффа ґрунтується метод «прискореного старіння ліків», який застосовують для визначення строків придатності лікарських засобів. Цей метод дозволяє скоротити час, необхідний для встановлення строку придатності ліків, і визначити оптимальну температуру їх зберігання.
Препарат витримують при підвищеній температурі Т певний час τT і знаходять кількість препарату т, яка розклалася. Середня швидкість розкладання
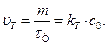
Якщо початкова концентрація речовини с0 і кількість речовини, що розклалася (т) при стандартній температурі такі самі, як і при температурі Т, то:
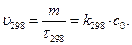
З двох останніх виразів витікає, що
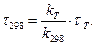
 Тобто, у скільки раз швидкість розкладення більша при високій температурі, в стільки раз треба менше витримувати нашу дослідну речовину.
Тобто, у скільки раз швидкість розкладення більша при високій температурі, в стільки раз треба менше витримувати нашу дослідну речовину.
Якщо температуру, при якій проводять дослід, записати як
Т = 298 + n ∙ 10.
Тоді, приймаючи γ = 2 (у відповідності до Державної Фармакопеї при визначенні терміну зберігання ліків температурний коефіцієнт швидкості реакції розкладення ліків приймають рівним двом), одержимо вираз для еквівалентного терміну зберігання препарату при 298 К:
τ298 = 2n ∙ τT.
|
|
Дата добавления: 2015-05-23; Просмотров: 1100; Нарушение авторских прав?; Мы поможем в написании вашей работы!