
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ковалентний зв’язок
Властивості ковалентного зв’язку
Насиченість ковалентного зв’язку пояснюється тим, що число ковалентних зв’язків, які утворює певний атом, обмежується числом неспарених електронів. Тобто атом, який містить один неспарений електрон, утворює з неспареним електроном іншого атома одну спільну електронну пару, отже, один хімічний зв’язок. Атом з двома неспареними електронами утворює дві спільні електронні пари, тобто два хімічних зв’язки тощо.
Напрямленість ковалентного зв’язку полягає в тому, що хімічний зв’язок утворюється у напрямку найбільшого ступеня перекривання електронних хмар взаємодіючих атомів. Саме у цьому випадку виділяється найбільша кількість енергії і зв’язок є найміцнішим.
Способи перекривання електронних хмар.
Якщо ділянка перекривання електронних хмар знаходиться на осі, що з’єднує ядра взаємодіючих атомів, такий спосіб перекривання електронних хмар називається s-зв’язком. Саме таким способом відбувається перекривання s-електронних хмар двох взаємодіючих атомів, s-електронної хмари одного атома та р-електронної хмари іншого атома, р-електронних хмар обох атомів:
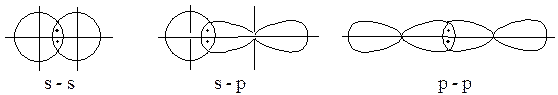
Але перекривання р-електронних хмар двох атомів може відбуватись іншим способом, який називається p-зв’язком. В цьому випадку ділянки перекривання р-електронних хмар знаходяться по обидва боки від осі, що з’єднує ядра взаємодіючих атомів.

p-Зв’язок є слабшим, ніж s -зв’язок за участю р-електроних хмар, тому що в цьому випадку ніщо не заважає відштовхуватись ядрам атомів один від одного, що призводить до меншого ступеня перекривання р-електронних хмар.
Слід пам’ятати, що s - та p-зв’язки – це не типи хімічного зв’язку, а способи перекривання електронних хмар.
|
|
Дата добавления: 2015-05-23; Просмотров: 330; Нарушение авторских прав?; Мы поможем в написании вашей работы!