
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методичні вказівки. Питання для самоперевірки
|
|
|
|
ГІДРОЛІЗ СОЛЕЙ
Питання для самоперевірки
Оформлення результатів роботи
Дослід 2. Реакції в розчинах електролітів.
1. У пробірку налити 2-3 мл розчину нітрату калію і додати туди стільки ж розчину хлориду натрію. Відзначити, що відбувається.
2. Налити в одну пробірку 2 мл розчину сульфату магнію, в другу стільки ж розчину сульфату хрому, в третю – сірчаної кислоти. У кожну з пробірок додати по 3 мл хлориду барію. Відзначити, що відбувається.
3. Налити в одну пробірку 2 мл розчину сульфату хрому, в другу стільки ж розчину хромату калію і додати в кожну з них по кілька крапель розчину гідроксиду калію. Відзначити, що відбувається в кожній пробірці.
4. Налити в пробірку 2 мл розчину карбонату натрію і додати туди стільки ж розчину соляної кислоти. Відзначити, що відбувається.
Дослід 1. Написати рівняння дисоціації оцтової кислоти і гідроксиду амонію, вираз швидкостей прямої і зворотної реакцій, а також констант дисоціації для вказаних рівноважних систем. Записати рівняння дисоціації ацетату натрію і хлориду амонію.
Зробити висновок щодо причини зміни забарвлення розчинів.
Зробити загальний висновок про вплив додання однойменного іону на дисоціацію слабкого електроліту.
Дослід 2. Написати рівняння реакцій в молекулярній та іонній формах.
На якій основі можна зробити висновок про те, що реакції в розчинах електролітів відбуваються між іонами, а не між молекулами? Пояснити, в яких випадках відбуваються реакції в розчинах електролітів.
1. Що таке електроліти та неелектроліти?
2. Який процес називається електролітичною дисоціацією?
3. Що таке ступінь та константа дисоціації? Від яких факторів вони залежать?
|
|
|
4. За якою ознакою електроліти поділяють на слабкі та сильні?
5. В яких випадках можуть відбуватися реакції в розчинах електролітів?
6. Написати рівняння ступінчатої дисоціації сірководневої кислоти і вираз для констант дисоціації.
Лабораторна робота № 8
Мета роботи - вивчення реакції середовища в розчинах різних солей а також факторів, які впливають на перебіг гідролізу.
Гідроліз є реакцією обмінної взаємодії іонів розчиненої солі з водою, в результаті якої утворюються малодисоційовані сполуки (молекули слабких кислот або основ, аніони кислих або катіони основних солей) і змінюється 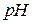 середовища.
середовища.
Щоб зрозуміти суть гідролізу, треба знати, що усі солі є сильними електролітами. Іони основних і кислотних залишків, на які дисоціюють солі, можуть зв’язувати 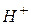 або
або 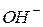 іони води. Внаслідок зв’язування одного з іонів води відбувається зміщення рівноваги процесу дисоціації води вправо і нагромадження в розчині одного з іонів
іони води. Внаслідок зв’язування одного з іонів води відбувається зміщення рівноваги процесу дисоціації води вправо і нагромадження в розчині одного з іонів 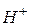 або
або 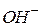 , в результаті чого змінюється
, в результаті чого змінюється 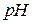 середовища. При цьому необхідно пам’ятати, що з іонів солі можуть зв’язуватися з іонами води тільки ті, які утворюють слабку кислоту або слабку основу. Тому гідролізують солі, до складу яких входить катіон слабкої основи (
середовища. При цьому необхідно пам’ятати, що з іонів солі можуть зв’язуватися з іонами води тільки ті, які утворюють слабку кислоту або слабку основу. Тому гідролізують солі, до складу яких входить катіон слабкої основи (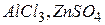 ) або аніон слабкої кислоти (
) або аніон слабкої кислоти (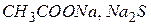 ) або і катіон і аніон одночасно (
) або і катіон і аніон одночасно (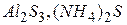 ).
).
Солі, утворені сильною основою і сильною кислотою, не гідролізують, тому що їхні іони не можуть утворити з водою слабких електролітів.
Залежно від типу солі процес гідролізу буде відбуватися по-різному. Розрізняють гідроліз солей: 1) за катіоном (катіон від слабкої основи), 2) за аніоном (аніон від слабкої кислоти), 3) за катіоном і аніоном (обидва від слабких електролітів).
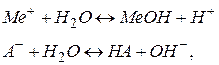
де 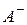 і
і 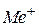 відповідно умовні аніон слабкої кислоти
відповідно умовні аніон слабкої кислоти 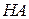 і катіон слабкої основи
і катіон слабкої основи 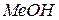 .
.
Солі, утворені багатозарядним катіоном або багатозарядним аніоном, гідролізують ступінчасто. Взаємодія багатозарядних іонів (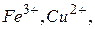
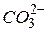
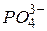 та ін.) з водою, звичайно відбувається до утворення основного або кислого іона (перший ступінь гідролізу), наприклад:
та ін.) з водою, звичайно відбувається до утворення основного або кислого іона (перший ступінь гідролізу), наприклад:
|
|
|
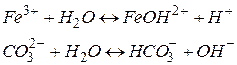
Гідроліз за катіоном призводить до зв’язування гідроксид–іонів води і нагромадження іонів водню, середовище кисле,  .
.
Гідроліз за аніоном призводить до зв’язування іонів водню від води і нагромадження іонів 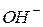 , середовище лужне,
, середовище лужне, 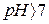 .
.
Необхідно пам’ятати, що гідроліз – процес оборотний і в більшості випадків до кінця не проходить.
Найбільш сильно гідролізують солі, утворені слабкою основою і слабкою кислотою. У цьому випадку реакція гідролізу може практично відбуватися до кінця, необоротно, якщо продукти гідролізу виводяться із сфери реакції, наприклад:
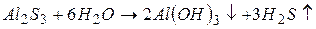
Продуктами гідролізу є слабка основа і слабка кислота, крім того, вони виходять із сфери реакції, зміщуючи тим самим рівновагу гідролізу праворуч.
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 311; Нарушение авторских прав?; Мы поможем в написании вашей работы!