
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Будова молекул альдегідів
|
|
|
|
.
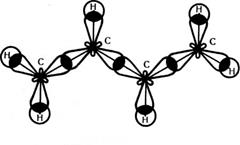
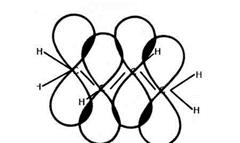
Мал.27 Схема утворення о-зв'язків у молекулі бутадієну та схема перекривання хмар р-електронів
У молекулі ацетилену відстань між ядрам атомів Карбону – 0,12 нм, атоми Карбону перебувають у стані sp – гібридизації.
У випадку потрійного зв’язку в гібридизації беруть участь по одному s – і p -електрону. В кожного атома Карбону є дві гібридизовані орбіталі, які максимально віддалені одна від одної (кут 180 о). По одній орбіталі вони витрачають на утворення 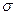 - зв’язку С – С, інші орбіталі ідуть на утворення зв’язків C - Н (мал. 28.)
- зв’язку С – С, інші орбіталі ідуть на утворення зв’язків C - Н (мал. 28.)

Схема утворення двох гібридних електронних хмар атома Карбону.
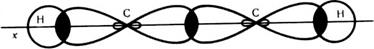
Мал. 28 Схема утворення о-зв'язків у молекулі ацетилену.
Ті дві негібридизовані р- орбіталі, які залишилися в кожного атома Карбону, взаємно перекриваються, в результаті чого утворюються два 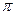 - зв’язки, розташовані взаємно перпендикулярно (мал.29.)
- зв’язки, розташовані взаємно перпендикулярно (мал.29.)
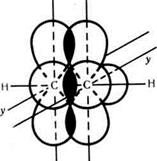
Мал.29 Схема утворення 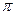 - зв’язків у молекулі ацетилену
- зв’язків у молекулі ацетилену
Атоми Карбону в молекулі бензену перебувають у стані sp2 – гібридизації.В кожного атома Карбону три гібридні орбіталі розташовані в одній площині під кутом 120 о. З них дві орбіталі перекриваються з такими ж орбіталями сусідніх атомів Карбону з утворенням 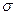 - зв’язків С – С, а третя орбіталь, перекриваючись з s – орбіталлю атома Гідрогену, утворює ще один
- зв’язків С – С, а третя орбіталь, перекриваючись з s – орбіталлю атома Гідрогену, утворює ще один 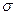 - зв’язок С – Н. В результаті цих перекривань утворюються
- зв’язок С – Н. В результаті цих перекривань утворюються 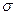 - зв’язки, розташовані в одній площині (мал.30)
- зв’язки, розташовані в одній площині (мал.30)
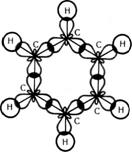
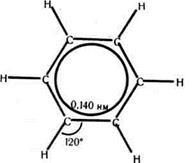
Мал.30 Схема утворення о-зв'язків у молекулі бензену і геометрія молекули.
Але у кожного атома Карбону залишається ще по одній негібридизованій орбіталі у формі симетричної вісімки. Оскільки ці орбіталі розташовані паралельно одна до одної і перпендикулярно до площини 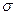 - зв’язку, вони взаємно перекриваються і утворюється єдина для всієї молекули
- зв’язку, вони взаємно перекриваються і утворюється єдина для всієї молекули 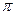 - електронна хмара, густина якої симетрично ділиться на дві частини площиною
- електронна хмара, густина якої симетрично ділиться на дві частини площиною 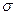 - зв’язків (мал.31). Під впливом
- зв’язків (мал.31). Під впливом 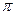 - електронної системи ядра атомів Карбону зближуються, відстань між ними скорочується до 0,14 нм. Електронна густина в молекулі бензену розподіляється рівномірно, томі зв’язки між атомами Карбону однакові. Таким чином, бензенове ядро - це стійка, міцна система. Хімічний зв’язок у молекулі бензену та його гомологах часто називають ароматичним.
- електронної системи ядра атомів Карбону зближуються, відстань між ними скорочується до 0,14 нм. Електронна густина в молекулі бензену розподіляється рівномірно, томі зв’язки між атомами Карбону однакові. Таким чином, бензенове ядро - це стійка, міцна система. Хімічний зв’язок у молекулі бензену та його гомологах часто називають ароматичним.
|
|
|
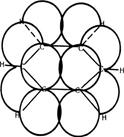
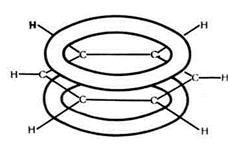
Мал. 31 Схема перекривання хмар р-електронів у молекулі бензену та 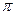 - електронна хмара
- електронна хмара
Одноатомні спирти можна розглядати як похідні насичених вуглеводнів, в молекулах яких один атом Гідрогену заміщений на гідроксильну групу. У цих молекулах атоми сполучені між собою ковалентними 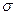 - зв’язками. (мал.32)
- зв’язками. (мал.32)
Мал. 32 Схема утворення 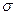 -зв'язків у молекулі метанолу.
-зв'язків у молекулі метанолу.
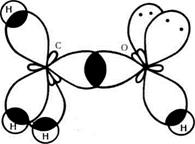
Особливості електронної будови альдегідів і кетонів зумовлені наявністю в їх молекулах карбонільної групи. В карбонільні групі атом Карбону перебуває в стані sp2 –гібридизації. В формальдегіді три орбіталі атома Карбону витрачаються на утворення 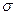 - зв’язків з двома атомами гідрогену і атомом Оксигену (мал. 33). Ці зв’язки, як і в молекулі етилену, розташовані в одній площині під кутом 120 о. Орбіталь негібридизованого р – електрона атома Карбону розташована перпендикулярно до площини
- зв’язків з двома атомами гідрогену і атомом Оксигену (мал. 33). Ці зв’язки, як і в молекулі етилену, розташовані в одній площині під кутом 120 о. Орбіталь негібридизованого р – електрона атома Карбону розташована перпендикулярно до площини 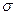 - зв’язку. Атом Оксигену однією р – орбіталлю сполучений з атомом Карбону (зв’язок С – О), другою р – орбіталлю, розташованою перпендикулярно до першої, утворює з не гібридизованою р – орбіталлю Карбону
- зв’язку. Атом Оксигену однією р – орбіталлю сполучений з атомом Карбону (зв’язок С – О), другою р – орбіталлю, розташованою перпендикулярно до першої, утворює з не гібридизованою р – орбіталлю Карбону 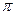 - зв’язок. Не дивлячись на певну подібність в електронній будові карбонільної групи і подвійного зв’язку молекули етилену, між ними існує велика різниця: електронна густина в молекулі етилену рівномірно і симетрично розподілена між атомами Карбону; в карбонільній групі електронна густина зміщена від Карбону до Оксигену як до більш електронегативного атома, тобто зв’язок С = О сильно полярний: на атомі Карбону виникає частковий позитивний заряд, на атомі Оксигену – частковий негативний:
- зв’язок. Не дивлячись на певну подібність в електронній будові карбонільної групи і подвійного зв’язку молекули етилену, між ними існує велика різниця: електронна густина в молекулі етилену рівномірно і симетрично розподілена між атомами Карбону; в карбонільній групі електронна густина зміщена від Карбону до Оксигену як до більш електронегативного атома, тобто зв’язок С = О сильно полярний: на атомі Карбону виникає частковий позитивний заряд, на атомі Оксигену – частковий негативний:
|
|
|
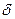 +
+ 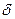 -
- 
R 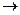 C = O
C = O
I
H
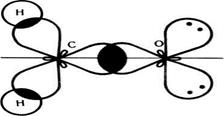
Мал. 33 Схема утворення о-зв'язків у молекулі формальдегіду.
Карбонові кислоти характеризуються наявністю функціональної групи атомів – СООН, яка називається карбоксильною. Її можна розглядати як сукупність карбонільної та гідроксильної груп (мал.34)
|
|
|
|
|
Дата добавления: 2015-05-23; Просмотров: 802; Нарушение авторских прав?; Мы поможем в написании вашей работы!