
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Речовини еквівалента, молярний об’єм еквівалента
|
|
|
|
Еквівалент, чинник еквівалентності, кількість
Молярний об’єм
Маса атома і маса молекули
Маса атома – це відношення молярної маси елемента до сталої Авогадро:
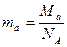 .
.
Так, 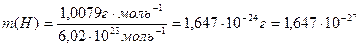 кг,
кг,
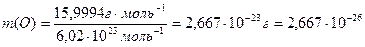 кг.
кг.
Маса атома дорівнює також добутку відносної атомної маси на атомну одиницю маси. Тоді m(O) = 15,9994 . 1,6605 . 10-27 кг = 2,667 . 10-26 кг.
Маса молекули – це відношення молярної маси речовини до сталої Авогадро: 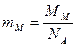 .
.
Так, 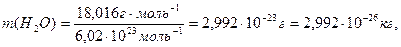 або
або
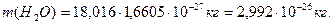
Молярний об'єм VМ - відношення об’єму речовини до кількості речовини в цьому об’ємі:
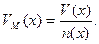
Одиниця вимірювання в СІ – м3/моль, в інших системах – л/моль. За нормальних умов (р = 101325 Па, Т = 273,15 К), якщо n(x) =
= 1 моль, VM = 22,4 л або 22,4.10-3м3.
Структурними одиницями речовин можуть бути реальні частинки – атоми, молекули, йони або умовні – йонні асоціати (NaCl, K2SO4, NH4NO3) для речовин з йонними кристалічними гратками і йонно-ковалентні асоціати (Al2O3, BaO, ZnS) для кристалів з гратками, проміжними між йонними і атомними. Формули NaCl, Al2O3 тощо показують лише атомний склад речовин.
Отже, якщо речовина складається з частинок (х), то еквівалентом речовини називається та частка структурної одиниці (х), яка рівноцінна одному йону Гідрогену в кислотно-основних або йоннообмінних реакціях або одному електрону в окисно-відновних реакціях:
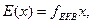
де fЕКВ - чинник еквівалентності.
Чинник еквівалентності – число, яке дорівнює тій частці частинки (х), яка є еквівалентом речовини в даній реакції:
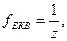
де z - еквівалентне число.
При визначенні еквівалентів простих речовин структурними одиницями є атоми, а z дорівнює їх валентності:
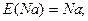
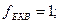
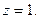
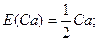
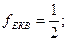
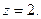
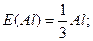
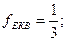
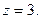
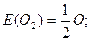
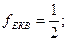
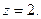
Для кислот в реакціях йонного обміну z дорівнює основності кислот, тобто числу йонів H+, заміщених на основні залишки:
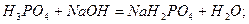
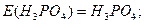
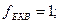
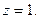
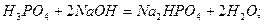
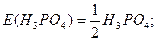
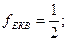
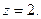
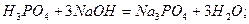
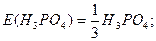
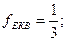
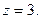
|
|
|
Для основ z дорівнює кислотності основ – числу гідроксид-йонів, заміщених на кислотні залишки:
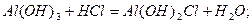
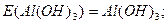
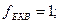
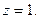
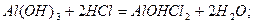
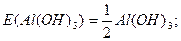
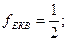
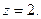
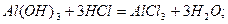
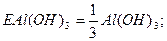
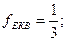
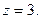
Для основних і амфотерних оксидів, а також для солей z дорівнює добутку валентності метала на число його атомів.
Для хром(ІІІ) оксиду і алюміній сульфату еквівалентами будуть умовні частинки:
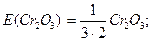
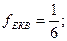
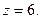
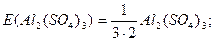
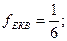
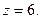
Маса одного моль еквівалента називається молярною масою еквівалента.
Молярна маса еквівалента МЕ = М(fЕКВх) - добуток чинника еквівалентності на молярну масу речовини: М(fЕКВx)=fЕКВМ(х).
Так,
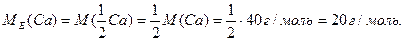
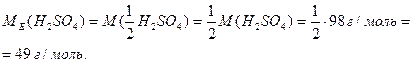
Для визначення молярних мас еквівалентів оксидів і солей можна користуватись формулами:
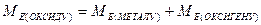
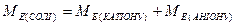
Кількість речовини еквівалента 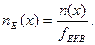
Наприклад, якщо n(Ca) = 2 моль, то nЕ(Са) = 2 моль: ½ = 4 моль.
Для визначення маси речовини можна використати формулу:
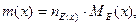
Об’єм одного моль еквівалента називається молярним об’ємом еквівалента VE(x). Для газів, молекули яких двоатомні (Н2, О2, Cl2 тощо),
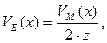
де z - валентність відповідного елемента.
Наприклад, 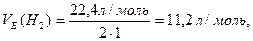
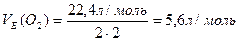 .
. 
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 2519; Нарушение авторских прав?; Мы поможем в написании вашей работы!