
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Квантові числа
Наслідком хвильових властивостей електрона є квантованість його енергетичних станів. Можливі енергетичні стани електрона в атомі визначаються величиною головного квантового числа  , яке може приймати значення цілих чисел 1, 2, 3, 4, 5, 6, 7...
, яке може приймати значення цілих чисел 1, 2, 3, 4, 5, 6, 7...  . Із збільшенням
. Із збільшенням  енергія електрона зростає.
енергія електрона зростає.
Стан електрона, який характеризується певним значенням головного квантового числа, називають енергетичним рівнем електрона в атомі.
Головне квантове число визначає розмір електронної хмари.
Для енергетичних рівнів в атомі прийняті такі позначення:
| Головне квантове число | |||||||
| Позначення енергетичних рівнів | K | L | M | N | O | P | Q |
Не тільки розмір, але й форма електронної хмари в атомі не може бути довільною. Вона визначається орбітальним квантовим числом 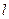 , яке може приймати значення цілих чисел від 0 до (
, яке може приймати значення цілих чисел від 0 до ( ).
).
Якщо 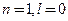



Стан електрона, який характеризується певним значенням 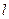 , називають енергетичним підрівнем електрона в атомі. Підрівні мають такі позначення:
, називають енергетичним підрівнем електрона в атомі. Підрівні мають такі позначення:
| Орбітальне квантове число | ||||
| Позначення енергетичних підрівнів | s | p | d | f |
Число підрівнів дорівнює номеру енергетичного рівня, але не може бути більше чотирьох.
Електронна хмара  - стану має сферичну форму, у
- стану має сферичну форму, у 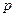 - електро-нів хмара має форму гантелі, у
- електро-нів хмара має форму гантелі, у 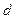 - електронів форма електронної хмари більш складна – розетка з чотирма пелюстками (рис. 2, 3, 4).
- електронів форма електронної хмари більш складна – розетка з чотирма пелюстками (рис. 2, 3, 4).
Орієнтація електронної хмари в електричному полі не може бути довільною. Вона визначається значенням третього квантового числа – магнітного me.
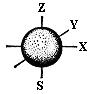
Магнітне квантове число може приймати значення чисел в межах від -l до +l. Отже, число можливих значень магнітного квантового числа дорівнює 2l+l. Якщо l =0, магнітне квантове число має тільки одне значення: me =0 (рис. 2).
| |
| Рис. 2. Електронна s -хмара (l =0) | |

| |
2 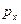 - орбіталь 2 - орбіталь 2 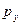 - орбіталь 2 - орбіталь 2  - орбіталь - орбіталь
| |
| Рис. 3. Електронні p -хмари (l =1) |
При значенні орбітального квантового числа одиниці (l =1) магнітне квантове число має три значення: me = -1, me = 0, me = 1. Три значення магнітного квантового числа характеризують три стани p -електронів, що відповідає орієнтації p -хмар в просторі по осях координат x, y, z (рис. 3).
При значенні орбітального квантового числа двом (l =2)магнітне квантове число має п’ять значень: me = -2, me = -1, me = 0, me = 1, me = 2. П’ять значень me відповідають п’яти просторовим положенням d -електронних хмар (рис. 4).
Орбітальному квантовому числу, що дорівнює трьом (l=3), відповідає сім значень магнітного квантового числа і сім просторових положень f -хмар.
Отже, магнітне квантове число характеризує число енергетичних станів електрона на підрівні.
Стан електрона в атомі, який характеризується певними значеннями квантових чисел n, l і me, тобто визначеним розміром, формою і орієнтацією в електромагнітному полі електронної хмари, називають атомною електронною орбіталлю.
Отже, орбіталь характеризує і енергію, і форму просторового розподілення електронної хмари.
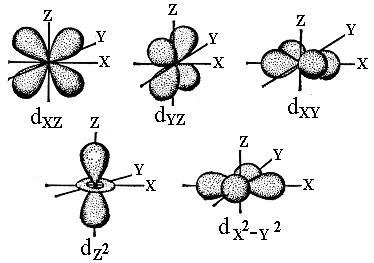
Рис. 4. Електронні d -хмари
Електрон характеризується ще однією квантовою величиною, яка визначає власний його стан – власний момент імпульсу, який характеризує обертання електрона навколо своєї осі. Ця величина одержала назву спінового квантового числа і позначається 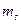 . Спінове квантове число може мати тільки два значення
. Спінове квантове число може мати тільки два значення 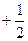 і
і 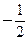 . Чотири квантових числа n, l, me та mS повністю визначають енерге-тичний стан електрона в атомі.
. Чотири квантових числа n, l, me та mS повністю визначають енерге-тичний стан електрона в атомі.
|
|
Дата добавления: 2015-05-24; Просмотров: 576; Нарушение авторских прав?; Мы поможем в написании вашей работы!