
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Елементів Д.Менделєєва
|
|
|
|
Періодичний закон і періодична система
До середини ХІХ ст. було накопичено досить багатий експериментальний матеріал про властивості хімічних елементів і їх сполук. Робились спроби класифікувати хімічні елементи (Деберейнер, Ньюлендс, Лотар Майєр).
Д.Менделєєв, на відміну від попередників, виходив з переконання, що між всіма хімічними елементами повинен існувати закономірний взаємозв’язок. В основу систематики елементів він поклав їх атомну масу.
В 1869 році Д.Менделєєв розмістив відомі тоді 64 хімічні елементи в ряд в порядку зростання атомних мас, що дало можливість встановити закономірності зміни їх властивостей. На цій підставі він залишив в цьому ряду вільні місця для ще невідкритих елементів і виправив в деяких випадках невірно розраховані атомні маси елементів. Досліджуючи зміни властивостей хімічних елементів, розташованих в ряд за зростаючими значеннями їх атомних мас, Менделєєв встановив, що близькі за хімічними властивостями елементи зустрічаються через певні проміжки (числа елементів) і, таким чином, одні і ті ж властивості періодично повторюються в цьому ряду. На цій основі Менделєєв вивів періодичний закон, який сформулював так: властивості простих тіл, а також форми і властивості сполук елементів знаходяться в періодичній залежності від величини атомних ваг елементів.
На основі відкритого закону Менделєєв склав періодичну систему елементів. Він розділив весь ряд елементів на відрізки (періоди), в яких починається і закінчується періодична зміна властивостей і розташував ці відрізки один під одним.
Менделєєв запропонував дві форми періодичної системи – довгу і коротку. Перший варіант системи мав довгу форму, тобто в ній періоди розміщувались одним рядком. В грудні 1870 р. він опублікував так звану коротку форму. В цьому варіанті періоди поділені на ряди, а групи на підгрупи.
|
|
|
У нас найбільш поширений варіант короткої форми як більш компактний.
Періодична система Менделєєва складається з семи горизонтальних періодів і восьми вертикальних груп.
Перший період містить всього два елементи (Н, Не), другий і третій періоди – по вісім, четвертий і п’ятий – по вісімнадцять, шостий – тридцять два, сьомий - незакінчений період, складається з двадцяти трьох елементів. Всього на даний час відомо 110 хімічних елементів. Перші три періоди називаються малими, а наступні – великими.
Елементи з однаковою максимальною валентністю розміщені в одному вертикальному стовпчику (групі). Великі періоди поділяють на ряди. В кожній групі елементи великих періодів поділяються на дві підгрупи – головну і побічну. Елементи малих періодів належать до головної підгрупи. Номер групи відповідає максимальній валентності всіх елементів групи. Виняток - Оксиген, Флуор, Неон, елементи побічних підгруп VIII-ої і І-ої груп.
Кожний період починається лужним металом (перший період Гідрогеном) і закінчується благородним газом. З ростом порядко-вого номера металічні властивості елементів послаблюються, а неметалічні – посилюються.
В шостому періоді розміщені 14 елементів з порядковими номерами 58-71, - лантаноїди, дуже подібні до лантану.
В сьомому періоді 14 елементів з порядковими номерами 90-103 – родина актиноїдів. Вони розміщені під лантаноїдами, тому що їх властивості дуже подібні.
Періоди позначені арабськими цифрами, групи – римськими з буквою А (головні) і з буквою В (побічні).
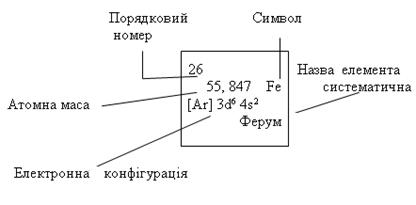
В кожній клітинці розміщені символ елемента, систематична назва, порядковий номер, атомна маса, електронна конфігурація. Наприклад:
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 578; Нарушение авторских прав?; Мы поможем в написании вашей работы!