
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакції в розчинах електролітів
В реакціях обміну в розчинах електролітів можуть брати участь сильні електроліти, слабкі електроліти, тверді речовини і гази. Сутність цих процесів виражається найбільш повно йонно-молекулярними рівняннями.
В таких рівняннях слабкі електроліти, малорозчинні сполуки і гази записують в молекулярній формі, а сильні електроліти – у вигляді йонів.
Наприклад, реакції нейтралізації сильних кислот сильними основами виражаються такими молекулярними рівняннями:
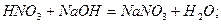

Але ці реакції не показують сутність процесів, що відбуваються в розчинах електролітів, де реакції відбуваються між йонами. Запишемо сильні електроліти у вигляді йонів, а слабкі у вигляді молекул:
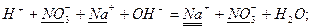
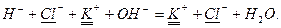
Одержані рівняння називаються йонно-молекулярними.
Виключивши з обох частин рівнянь однакові йони, одержимо для обох реакцій однакове скорочене йонно-молекулярне рівняння:
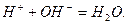
Отже, сутність реакцій нейтралізації сильних кислот сильними основами полягає в утворенні молекул води (малодисоційованої сполуки) з йонів Гідрогену і гідроксид-йонів.
Аналогічно реакції між речовинами, одні з яких містять катіони Барію (Ва2+), а другі сульфат-аніони (SO42-), наприклад:
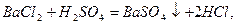
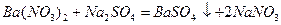
виражаються однаковим скороченим йонно-молекулярним рівнян-ням утворення малорозчинного електроліту BaSO4:
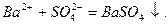
В цьому можна переконатись, написавши йонно-молекулярні рівняння цих реакцій і виключивши однакові йони:
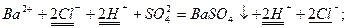
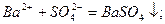
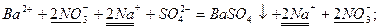
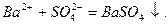
Взагалі реакції обміну в розчинах електролітів є необоротними (проходять до кінця), якщо вихідні речовини – сильні електроліти, а один з продуктів реакції осад, газоподібна малорозчинна речовина або малодисоційована сполука (див.додаток, табл.2).
Перший і третій випадки ми вже розглянули, розглянемо ще випадок, коли утворюється газоподібна речовина:
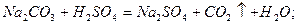
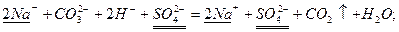
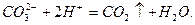
В тих випадках, коли малорозчинні речовини або слабкі електроліти є серед вихідних речовин і продуктів реакції, рівновага зсувається в напрямку утворення найменш розчинних або найменш дисоційованих сполук. Наприклад, при нейтралізації слабкої кислоти сильною основою:
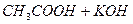 L
L 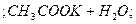
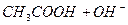 L
L 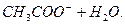
в реакції беруть участь два слабких електроліти – СН3СООН і вода. Рівновага зсувається в напрямку утворення більш слабкого електроліту – води. Але до кінця така реакція не проходить: в розчині залишиться деяка кількість молекул СН3СООН і йонів ОН -. Реакція буде слабколужною.
Аналогічно при нейтралізації слабкої основи сильною кислотою в розчині залишиться деяка кількість молекул слабкої основи і йонів Н+. Реакція буде слабкокислою
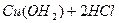 L
L 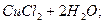
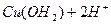 L
L 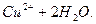
Отже, ці реакції є оборотними.
|
|
Дата добавления: 2015-05-24; Просмотров: 795; Нарушение авторских прав?; Мы поможем в написании вашей работы!