
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторна робота №11
|
|
|
|
ТЕМА: АМІНИ. АМІНОКИСЛОТИ. БІЛКИ
1. Одержання аміну і дослідження деяких його властивостей
Реактиви: хлорид метиламонію (кристалічний), натронне вапно – кристалічне, червоний лакмусовий папір.
У пробірку з газовідвідною трубкою помістити 0,5 г хлориду метиламонію і біля 1г натронного вапна. Суміш старанно перемішати. Нагріти пробірку. Метиламін, що виділяється, підпалити біля газовідвідної трубки. До отвору газовідвідної трубки піднести вологий індикаторний папірець, скляну паличку змочену концентрованою соляною кислотою. Опишіть спостереження. Навести рівняння одержання метиламіну і взаємодію його з водою і HCl. Який висновок можна зробити про природу аміногрупи.
2.Реакції a- амінокислот
Реактиви: гліцин, аланін та інші амінокислоти, універсальний індикаторний папірець, оксид міді – порошок, розчин NaOH, 0,1 н розчин нінгідрину.
а) Визначення рН - середовища
Налийте в пробірки 1-2 мл. розчинів різних амінокислот і за допомогою універсального індикатора визначте рН-середовища. Напишіть формулу внутрішньої солі гліцину.
б). Утворення комплексної мідної солі аміно оцтової кислоти
Помістити в пробірку невеличку кількість оксиду міді, додати 1,0 мл. розчину гліцину. Після відстоювання видно синє забарвлення розчину. Відлити трохи розчину і додати декілька крапель розчину гідроксиду натрію. Випадає осад гідроксиду міді (ІІ). Іншу рідину злити з осаду оксиду міді, остудити в стакані з крижаною водою. Випадають кристали мідної солі гліцину. Представити рівняння утворення комплексної мідної солі гліцину.
в) Реакція a- амінокислот з нінгідрином
До кількох крапель різноманітних a-амінокислот долити 2-3 краплі розчину нінгідрину. Струснути. Спостерігати характерне забарвлення.
|
|
|
3. Буферні властивості розчину білка
Реактиви: білок, 0,01н розчин NaOH, 0,01н розчин HCl, конго, фенолфталеїн.
а) До 0,01н розчину HCl додайте декілька крапель розчину індикатора конго. Розчин забарвлюється в яскраво-синій колір. Цей розчин потроху додайте до 2-3 мл. розчину білка. Забарвлення змінюється від синього до червоного.
б) До 0,01н розчину NaOH додайте декілька крапель розчину фенолфталеїну. Розчин забарвлюється в яскраво-рожевий еолір. Якщо цей розчин додати до 2-3 мл. розчину білка, то забарвлення зникає.
Зміна забарвлення індикаторів відбувається завдяки буферним властивостям білка, який може зв’язувати як водневі так і гідроксильні іони. У першому випадку (а) білок знижує кислотність, а в другому випадку (б) – основність системи.
4. Осадження білків солями важких металів
Реактиви: розчин яєчного білка, 5% розчин сульфату міді, 5% розчин ацетату свинцю.
У дві пробірки помістити 1-2 мл розчину білка, повільно по краплях додати в одну пробірку розчин сульфату міді, у другу – розчин ацетату свинцю. До пластівчастих осадів, що випали, долити надлишок цих реактивів. Яке осадження викликають вищевказані солі.
5. Осадження білків мінеральними кислотами
Реактиви: концентровані кислоти:HCl, H2SO4, HNO3, розчин білка.
У три пробірки вміщують по 10 крапель концентрованих кислот. HCl, H2SO4, HNO3. У кожну з пробірок обережно по стінках доливають розчину білка. На межі кислота – білок утвориться білий осад білка. Збовтати суміші в пробірках. У яких кислотах осадження білка зворотне?
6. Висолювання білків з розчинів
Реактиви: розчин яєчного білка, насичений розчин сульфату амонію, кристалічний сульфат амонію.
До 1,0 мл розчину білка додати рівний об'єм насиченого розчину сульфату амонію, перемішати. Спостерігати коагуляцію глобулінів. Дослідіть зворотне або незворотне осадження глобулінів? Для цього до невеличкої частини каламутної рідини додати велику кількість води. Що спостерігається? Висновок. Іншу частину каламутної рідини профільтрувати і до фільтрату додати кристалічний сульфат амонію до припинення його розчинення. Спостерігайте потемніння розчину - осадження альбумінів. До невеличкої частини каламутної суміші долити надлишок води. Зробіть висновок про тип осадження альбумінів.
|
|
|
7. Осадження білків при нагріванні
Реактиви: розчин яєчного білка, 1% розчин оцтової кислоти.
Помістити в дві пробірки по 1,0-2 мл розчину білка. У одну з пробірок внести декілька крапель розчину оцтової кислоти. Обидві пробірки нагріти до кипіння. Звернути увагу в якій пробірці з'являється більш інтенсивне помутніння? Чому. До отриманих каламутних сумішей додати велику кількість води. Чи зворотне осадження білка при нагріванні?
8. Кольорові реакції білка.
Реактиви: яєчний білок, концентрований розчин лугу, розчин сульфату міді, концентрована нітратна кислота, 2% розчини тирозину і гліцину.
а) Біуретова реакція білків
У пробірку внести 1,0-2 мл розчину білка, стільки ж концентрованого розчину лугу і 3-4 краплі розчину сульфату міді. Струснути пробірку. Спостереження. Що доводить дана реакція?
б) Ксантопротеінова реакція на білки й ароматичні амінокислоти
У приготовлені три пробірки відповідно внести по 3-4краплі розчину таких речовин. У першу пробірку внести розчин білка, у другу - розчин тирозину, у третю - розчин гліцину. У кожну пробірку внести 2-3 краплі концентрованої азотної кислоти. Нагріти протягом 2-3 хвилин. Спостереження. Остудити вміст пробірок і додати в кожну з них по декілька крапель концентрованого розчину лугу. Спостереження. Що доводить проведена реакція? Написати рівняння нітрування тирозину і фенілаланіну.
9. Відкриття аміногруп і сірки у білках
Реактиви: білок, ацетат свинцю – 10% розчин, концентрований розчин NaOH.
До 2 мл розчину білка додайте 4 мл концентрованого розчину NaOH і прокип’ятіть протягом 2 хв. За запахом зафіксуйте виділення аміаку. При дії лугу, крім часткового гідролізу по пептидних зв’язках, відбувається відщеплення аміногруп у вигляді аміаку.
До одержаного гарячого розчину додайте 1 мл розчину солі свинцю і знову прокип’ятіть, рідина забарвлюється в темно-коричневий колір, а іноді випадає коричневий або чорний осад сульфіду свинцю. Якщо білок містить сірку, то при кип’ятінні з лугом вона виділяється у вигляді сірководню.
|
|
|
H2S +(CH3 COO)2Pb ® PbS¯ + 2 CH3COOH
Завдання для самостійної роботи
1. Назвіть нижченаведені сполуки:
CH3 –CH –NH2 CH3 –N – CH –CH3 CH2 – CH2 – CH2
| | | | |
CH3 CH3 –CH2 CH3 NH2 NH2
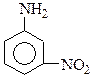
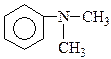
2. Напишіть структурні формули амінів складу C4H11N. Назвіть їх.
3. Здійсніть перетворення: бензол ® нітробензол ® анілін® фенілдіазоній-хлорид ® п -диметиламінобензол.
4. На прикладі b- аміномасляної кислоти поясніть амфотерність амінокислот. Напишіть відповідні реакції.
5. Напишіть схему утворення пептидів із:
а) гліцину та цистеїну;
б) метіоніну та триптофану;
в) аланіну, гліцину та серину.
Назвіть їх.
СПИСОК РЕКОМЕНДОВАНОЇ ЛІТЕРАТУРИ
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1739; Нарушение авторских прав?; Мы поможем в написании вашей работы!