
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Самостійна робота на занятті. Тема: Визначення буферної ємності
|
|
|
|
Тема: Визначення буферної ємності. Роль буферів в біосистемах.
Актуальність теми: Буферні системи крові забезпечують стабільність рН крові. При дії кислотних агентів (СО2) кислотно-основна рівновага забезпечується лужним резервом крові. Визначення буферної ємності крові є важливим показником стану організму, його можливості чи певної патології.
Навчальні цілі:
Знати: основні буферні системи організму, механізм дії білкових систем крові. Способи вимірювання резервної лужності крові.
Вміти: визначити буферну ємність буферних систем методами об’ємного титрування за допомогою індикаторів, а також розрахувати буферну ємність.
Самостійна позааудиторна робота студентів.
1. Механізм дії буферних систем.
2. Білкові буферні розчини, їх хімічний склад.
3. Буферні розчини крові.
4. Буферна ємність, її визначення.
5. Фактори, які обумовлюють буферну ємність.
6. Кислотно-лужна рівновага крові. Ацидоз і алкалоз.
7. Резервна лужність крові. Фактори, які її обумовлюють.
8. Вплив екологічного забруднення на кислотно-лужну рівновагу в організмі.
9. Методи практичного визначення буферної ємності.
Контрольні питання.
1. Що таке буферна ємність?
2. Які Ви знаєте буферні системи організму?
3. Механізм дії на гідрокарбонатну буферну систему кислоти, лугу.
4. Механізм дії на гідрофосфатну буферну систему кислоти, лугу.
6. Механізм дії на білкову буферну систему кислоти, лугу.
7. Механізм дії на ацетатну буферну систему кислоти, лугу.
8. Як визначити буферну ємність?
9. Що таке ацидоз, алкалоз? Яке рН крові?
10.Які фактори обумовлюють буферну ємність?
11.Що таке резервна лужність крові?
12.До 100 мл крові для зміни рН від 7,36 до 6,9 треба прилити 40 мл розчину хлоридної кислоти з молярною концентрацією еквівалентів 0,05 моль/л. Обчислити буферну ємність крові за кислотою.
|
|
|
13.Обчислити ступінь електролітичної дисоціації та рН для розчину нітритної кислоти з молярною концентрацією еквівалентів 0,002 моль/л. (К=4,6.10-6).
14.Обчислити скільки мл розчину НСl з молярною концентрацією 0,02 моль /л треба додати до 50 мл крові, щоб змінити її рН з 7,36 до 7,1.
Виконати лабораторні роботи:
1. Приготувати ацетатний буфер з певним значенням рН.
2. Визначити буферну ємність за кислотою.
3. Визначити буферну ємність за лугом.
4. Визначити буферну ємність сироватки крові.
Методика виконання роботи
Робота 1. Приготування ацетатного буферу.
Кожна пара студентів готує 20 мл ацетатного буферу, змішуючи 10 мл 0,1 М розчину оцтової кислоти і 10 мл 0,1 М розчину її натрієвої солі. За допомогою рН метра чи універсального індикатора визначають рН одержаного буферу. Розчин зберігають для наступних робіт.
Робота 2. Визначення буферної ємності приготовленого розчину за лугом.
10 мл буферного розчину, одержаного в роботі 1 (рН = 4,6), розливають порівну в дві колбочки для титрування. До кожної додають 2-3 кр. індикатора метилового червоного. Бюретку для титрування заповнюють 0,1 М розчину гідроксиду натрію. Титрування проводять до появи лимонно-жовтого забарвлення (рН = 6,3). Проводять розрахунки за рівняннями:
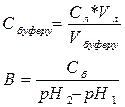
Робота 3. Визначення буферної ємності розчинуза кислотою.
10 мл буферного розчину, одержаного в роботі 1 (рН = 4,6), розливають порівну в дві колбочки для титрування. До кожної додають 2-3 кр. індикатора метилового оранжевого. Титрують 0,1 М розчином НС1 до появи малинового забарвлення (рН = 3,1).
Проводять розрахунки буферної ємності за відомими формулами для кислоти.
Робота 4. Визначення буферної ємності сироватки крові.
Буферну ємність сироватки крові (рН = 7,4) визначити за кислотою і лугом. Для цього в 2 колбочки прилити по 1 мл сироватки крові. В першу колбочку прилити 1-2 краплі фенолфталеїну і титрувати 0,1 М розчином лугу до появи рожевого забарвлення (рН = 9,0). В другу колбочку прилити 1-2 краплі метилоранжу і титрувати 0,1н розчином соляної кислоти до появи стійкого оранжевого забарвлення (рН = 4,0). Титрування повторити 2-3 рази. Буферну ємність розрахувати як в попередніх роботах. Зробити висновки.
|
|
|
Заняття 12
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1057; Нарушение авторских прав?; Мы поможем в написании вашей работы!