
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Застосування. Завдяки своїй здатності горіти на повітрі, з виділення великої кількості світла, застосовувався у фотосправі як спалах
|
|
|
|
Завдяки своїй здатності горіти на повітрі, з виділення великої кількості світла, застосовувався у фотосправі як спалах, до винаходу електричних ламп спалахів.
Сплави на основі магнію є важливим конструкційним матеріалом в автомобільній і авіаційній промисловості завдяки їх легкості і міцності. Ціни на магній в злитках в 2006 році склали в середньому 3 долл/кг.
Гідрид магнію — один з найбільш ємких акумуляторів водню, що вживаються для його зберігання. Оксид магнію застосовується в медицині і як вогнетривкий матеріал для виробництва тиглів і спеціальної футеровки металургійних печей.
Перхлорат магнію (ангидрон) застосовується для глибокого осушення газів в лабораторіях. Природний мінерал бішофіт як натуральне джерело іонів магнію та мікроелементів широко застосовується у медицині - реабілітації опорно-рухового апарату, серцево-судинної та нервової систем, санаторно-курортному оздоровленні.
44.Манган. Природні сполуки одержання властивості застосування.
Манга́н, ма́рганець (Mn) – хімічний елемент з атомним номером 25. Метал, який відповідає цьому елементу — марганець.
Атомна маса манґану 54,9381. Це сріблясто-білий крихкийметал. Густина 7,470 (293 К). tплав 1244°С, tкип 2095°С. Манґанпарамагнітний при низьких температурах. Це поширений елемент, його кларк в земній корі 0,1% (за масою), вультраосновних породах – 0,15%, основних - 0,2%, середніх - 0,12%, кислих - 0,06%, осадових - 0,07%, кам. метеоритах – 0,2%. Вміст манґану в океанічній воді 2·10-7 %, в живій речовині Землі 1·10-3%, у ґрунті 8,5·10-2%.
Манґан повільно реагує з водою, розчиняється в кислотах, реагує з усіма неметалами (при нагріванні), крім водню. Представлений в основному оксидами, карбонатами і в меншій мірі – силікатами манґану. Основні мінерали манґану:піролюзит, гаусманіт, псиломелан, манганіт, брауніт,родохрозит, родоніт. Крім того, манґан містять мінерали: велініт. Внаслідок кристалохімічної близькості манґану до трьох найважливіших петрогенних елементів – Fe, Mg, Ca – широко представлений як ізоморфна домішка в породотвірнихмінералах (олівінах, ґранатах, слюді, карбонатах). Значну кількість манґану містять залізо-марганцеві конкреції.
|
|
|
Манґан використовується в основному в чорній металургії(майже 95% мангану іде на розкиснення і десульфуризаціюсталі і чавуну і на добавки в спеціальні сталі), при виплавці різних сплавів кольорових металів, для створення антикорозійних покриттів. Добавка мангану до заліза і сталі істотно підвищує їх в’язкість, ковкість і твердість. У розплав манган вводять у вигляді феромарганцю (70-80% Mn, 0,5-1% С, інше Fe). У кольоровій металургії манган застосовується для отримання марганцевистої бронзи, латуні та інших сплавів з кольоровими металами, що підвищує їхню міцність і додає антикорозійні властивості. У металургії використовуються руди із вмістом 30-36% мангану і менше 0,2% фосфору. Сполуки мангану широко використовують при виробництві скла, оліфи і в гальванічних елементах (піролюзит), в медицині (перманганат калію), у фарбувальній справі (хлорид і сульфат мангану). Є також складовою частиною мікродобрив. Діє на центральну нервову систему. Гранична допустима концентрація 0,2 мг/м³.
45.Хром. Природні сполуки одержання властивості застосування.
Хром (Cr) — хімічний елемент із атомним номером 24, а такожпроста речовина, перехідний метал.
Хроміт заліза (хромистий залізняк) при 1200 °C перетворюють в хромат: 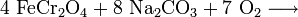
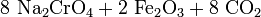
Хромат розчиняють у воді і сірчаною кислотою переводять у дихромат:
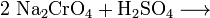
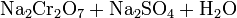
Дихромат натрію кристалізується при охолоджені як дигідрат. При наступному відновленні вуглецем отримують Хром(III) оксид:
|
|
|
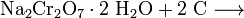
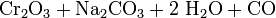
У кінцеві стадії відновлюють хром алюмотермічно:
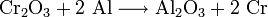
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1650; Нарушение авторских прав?; Мы поможем в написании вашей работы!