
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теоретичний вступ
|
|
|
|
ЛАБОРАТОРНА РОБОТА № 9
ВИЗНАЧЕННЯ ЗАГАЛЬНОЇ ЛУЖНОСТІ І КАРБОНАТНОЇ ТВЕРДОСТІ ВОДИ
Лужність води може бути обумовлена наявністю розчинних основ, середніх і кислих солей, утворених сильними основами і слабкими кислотами (карбонати, гідрогенкарбонати, гідроген-силікати, гідрогенсульфіди тощо).
Активна лужність характеризується показником рОН.
Лужність визначається нейтралізацією води сильними кислотами.
Звичайно лужність природних вод обумовлена наявністю гідрогенкарбонатів лужних і лужноземельних металів, і значення рН таких вод не перевищує 8,3. Визначення загальної лужності проводиться нейтралізацією проби води сильною кислотою до рН = 4,5 в присутності індикатора метилового оранжевого (інтервал переходу рН 3,1-4,4).
Якщо рН >8,3, то визначають вільну лужність. Вона характеризується кількістю сильної кислоти (ммоль-екв/л), необхідної для зниження рН до цього значення (індикатор – фенолфталеїн, інтервал переходу рН складає 8,2-10,7). Вільна лужність обумовлена наявністю вільних лугів і розчинних солей – карбонатів, силікатів, сульфідів. Якщо рН <8,3, то вільна лужність дорівнює нулю.
Загальна лужність більшості природних вод обумовлена присутністю тільки гідрогенкарбонатів (йонів НСО3-).
Для переважної більшості природних вод йони НСО3- зв’язані тільки з йонами Са2+ і Mg2+.
Саме тому, коли лужність за фенолфталеїном дорівнює нулю, можна вважати, що загальна лужність води дорівнює її карбонатній твердості.
Твердість води зумовлена присутністю в ній розчинних кальцієвих та магнієвих солей різних кислот – карбонатної, сульфатної, хлоридної, нітратної, фосфатної та силікатної.
Твердість води поділяють на карбонатну та некарбонатну. Карбонатна твердість зумовлена присутністю у воді гідрогенкарбонатів кальцію і магнію. Її називають тимчасовою тому, що її майже повністю можна усунути кип’ятінням води. Гідрогенкарбонати при цьому розкладаються з утворенням кальцій карбонату і магній гідроксиду, які випадають в осад:
|
|
|
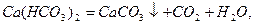
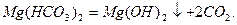
Некарбонатна твердість зумовлена присутністю кальцієвих і магнієвих солей сульфатної, хлоридної, нітратної, фосфатної та силікатної кислот, які при кип'ятінні залишаються в розчині.
Твердість води виражають сумою ммоль-екв. йонів кальцію і магнію, які містяться в 1л води. Один ммоль-екв твердості відповідає вмісту 20,04 мг/л Са2+ або 12,16 мг/л Mg2+.
Існує така класифікація природних вод за твердістю (О.Алєкін):
- дуже м’яка (від 0 до 1,5 ммоль-екв/л);
- м’яка (від 1,5 до 3 ммоль-екв/л);
- середньої твердості (від 3 до 5,4 ммоль-екв/л);
- тверда (від 5,4 до 10,7 ммоль-екв/л);
- дуже тверда (більше за 10,7 ммоль-екв/л).
Найбільш м’які води – це води атмосферних опадів, які мають твердість 70-100 мікро-екв/л. Твердість підземних вод визначається складом контактуючих з ними порід. Так, ґрунтові води Донбасу, які формуються під дією крейдяних та доломітових порід, є дуже твердими: Т = 18-20 ммоль-екв/л.
Твердість річкових вод залежить від кліматичних умов і характеру живлення річок, а також від пори року. Найменша вона під час паводку. Наприклад, твердість води в Дніпрі 5,135 ммоль-екв/л.
Твердість вод морів значно вища. Так, вода Чорного моря має загальну твердість 65,5 ммоль-екв/л. Середнє значення твердості світового океану 130,5 ммоль-екв/л.
Для господарсько-питного водопостачання допустимою вважається твердість не більше 7 ммоль-екв/л (ДСанПіН 383).
Присутність у воді значної кількості солей кальцію і магнію робить воду непридатною для господарсько-побутових потреб.
У твердій воді погано розварюються овочі, збільшуються витрати мила. Така вода є непридатна для використання у парових котлах.
|
|
|
Для усунення твердості води застосовують методи осадження та йонного обміну. Методи осадження поділяються на термічний (нагрівання води до t = 95-980С) та реагентний (застосування вапна або соди як осаджувачів). Термічним методом усувається карбонатна твердість, а реагентним методом переводяться в осад усі солі кальцію і магнію у вигляді CaCO3 і Mg(OH)2.
Для усунення твердості методом йонного обміну воду пропускають через катіоніти. При цьому катіони Са2+, Mg2 +, які знаходяться у воді, обмінюються на катіони Na+ або H+, які містяться в катіоніті:
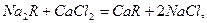
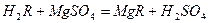
(H2R застосовують, якщо Т<1 ммоль-екв/л).
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 575; Нарушение авторских прав?; Мы поможем в написании вашей работы!