
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методи добування. Фенолами називають сполуки, в яких гідроксильні групи сполучені безпосередньо з атомами Карбону ароматичного кільця
Номенклатура
Феноли
Фенолами називають сполуки, в яких гідроксильні групи сполучені безпосередньо з атомами Карбону ароматичного кільця. Залежно від кількості гідроксильних груп розрізняють одно- та багатоатомні феноли:

Одноатомні феноли, що містять одну гідроксильну групу, утворюють гомологічний ряд, першим представником якого є фенол. Від толуену можна утворити орто -, мета - і пара -гідрокситолуени, які називають крезолами:

За номенклатурою IUPAC феноли розглядають як заміщені бензени. Нумерацію починають від атома Карбону, біля якого знаходиться гідроксигрупа. Поряд з тим феноли, як і інші ароматичні сполуки, зберегли тривіальні назви, які ще широко використовуються в органічній хімії.
Ще й тепер не втратив актуальності метод добування фенолу з кам’яновугільної смоли. Враховуючи велике значення фенолу і продуктів, які добувають на його основі, розроблено ряд синтетичних методів його добування. Найважливіші з них:
1. Гідроліз арилгалогенідів твердими їдкими лугами або перегрітою парою над каталізатором − один із сучасних промислових методів добування фенолів:
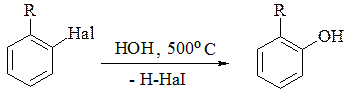
2. Лужний плав сульфокислот ароматичного ряду:
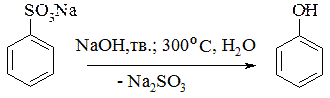
3. Окиснення ізопропілбензену (кумолу). Кумольний метод добування фенолу (метод Сергєєва), за яким одночасно можна добути два цінні продукти – фенол і ацетон, має найбільше промислове значення:


4. Гідроліз солей арилдіазонію:
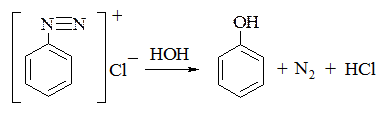
14.3. Фізичні властивості
Фенол – біла кристалічна речовина з характерним запахом, має дезинфікуючі та антисептичні властивості. Фенол – отруйна речовина, при попаданні на шкіру утворює опіки.
14.4. Хімічні властивості.
Фенол – класичний приклад для ілюстрації взаємного впливу атомів та груп атомів в молекулі.
1. Вплив фенілу на гідроксил полягає в тому, що феніл, як сильний акцептор електронів, відтягує електронну густину від атома Оксигену гідроксильної групи. Внаслідок спряження електронна густина на атомі Оксигену в молекулі фенолу зменшується, послаблюється зв’язок О−Н. Тому Гідроген досить легко протонізується (відщеплюється у вигляді протону):
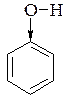
Саме легкість відщеплення протону характеризує міру кислих властивостей сполуки, а тому фенол називають ще карболовою кислотою (використовується як бактерицидний дезинфікуючий засіб).
2. Вплив гідроксилу на феніл полягає в тому, що –ОН група як орієнтант
І роду, що має +М-ефект, зсуває свою електронну густину на ароматичне ядро, а тому полегшує перебіг SЕ-реакцій в ядрі. Найбільше підвищується електронна густина в орто - і пара -положеннях відносно гідроксилу.
Перше положення ілюструється взаємодією фенолу з водним розчином лугу і утворенням солей – фенолятів:
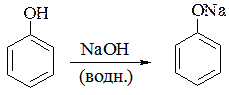
(Спирти з водним розчином лугу не реагують, тому що спирти набагато слабші кислоти ніж феноли).
Друге положення ілюструється реакціями нітрування або галогенування фенолу:

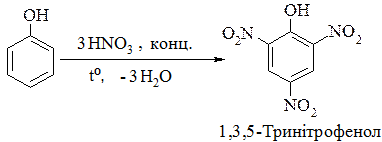
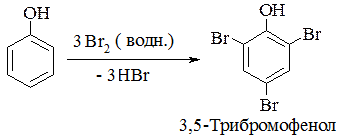
Феноли легко вступають в реакції конденсації за електрофільним механізмом з різними сполуками. Так, фенол з формальдегідом у присутності кислого каталізатора утворює полімери лінійної будови – новолачні смоли:

За наявності надлишку формальдегіду і лужних каталізаторів утворюються резольні смоли (реактопласти, або термоактивні полімери) з розгалуженою лінійною будовою:
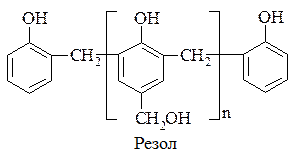
У разі подальшого нагрівання резоли дають нерозчинні резити з тривимірною (зшитою) структурою:

14.5. Окремі представники
Фенол (гідроксибензен, карболова кислота) – безбарвна кристалічна речовина з характерним різким запахом, добре розчинна в більшості органічних розчинників, але обмежено розчинна у воді. Водний розчин застосовується як антисептик. Фенол – отруйна речовина, потрапляючи на шкіру, викликає опіки. Він використовується для добування барвників, пластмас, лікарських препаратів, ароматизуючих речовин тощо.
Крезоли добувають поряд з фенолом з кам’яновугільної смоли. Застосовують для добування штучних смол, а також в якості антисептиків.
14.6. Дво- та триатомні феноли, нафтоли та їх похідні
Гідрохінон використовується як проявник у фотографії, а також як інгібітор полімерізації ненасичених сполук. Пірогалол застосовують як поглинач кисню в газовому аналізі, а також для фарбування волосся та хутра. Похідні нафтолів (їх сульфокислоти) використовують у виробництві синтетичних барвників. [1], c. 256-267; [2], c. 684-710.
Контрольні запитання та завдання
1. Наведіть атомно-молекулярну модель молекули метилового спирту. Охарактеризуйте полярність зв’язків С–О і О–Н. Які йони утворюються при гетеролітичному розриві зв’язку О–Н? Які властивості спиртів зв’язані з цим процесом?
2. Порівняйте будову метану і метилового спирту та дайте відповідь на такі запитання: 1. Чому метан – газ, а метиловий спирт – рідина? 2. Чому метан практично не розчиняється в воді, а метанол змішується з водою у будь-якому відношенні?
3. У чому полягає схожість і відмінність між одно- і багатоатомними спиртами в реакціях дегідратації та окиснення?
4. Чому у дво- і триатомних фенолів ароматичний характер виражений меншою мірою, ніж у фенолу? Для пояснення використовуйте можливі таутомерні структури.
5. Як кислотні властивості фенолів залежать від електронодонорних та електроноакцепторних замісників у ароматичному кільці та від їх розміщення відносно фенольного гідроксилу?
6. Напишіть реакції етиленгліколю (1,2-етандіолу) з такими реагентами: а) Na (мет.); б) HBr; в) CH3COOH [H+]; г) HNO3; е) HIO4.
7. За допомогою яких реакцій можна розрізнити такі сполуки:
а) 1-бутанол і 2-бутанол; б) ізобутиловий і трет- бутиловий спирти; в) пропіловий і аліловий спирти; г) аліловий і пропаргіловий спирти; д) етанол і етандіол; е) 1,2-пропандіол і 1,3-пропандіол?
|
|
Дата добавления: 2015-05-24; Просмотров: 3260; Нарушение авторских прав?; Мы поможем в написании вашей работы!