
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамическое уравнение состояния смеси идеальных газов, влажный воздух
|
|
|
|
Расчет параметров состояния идеального газа, несжимаемой жидкости и двухфазного рабочего тела.
Идальный газ – это воображаемый газ, состоящий из упругих молекул, между которыми отсутствуют силы взаимного притяжения и отталкивания, а объем, занимаемы этими молекулами, бесконечно мал по сравнению с объемом пространства между ними.
Основные свойства ид. газа:
Объем частиц газа равен нулю
Импульс передается только при соударениях
Суммарная энергия частиц постоянна.
Термическим уравнением состояния идеального газа является уравнение Клапейрона –Менделеева PV=RT. Теплоемкостью вещества называется отношение бесконечно малого количества теплоты, подводимого к веществу в каком-либо процессе, к соответствующему бесконечно малому изменению его температуры. Таким образом, согласно молекулярно – кинетической теории теплоемкость идеального газа зависит только от сложности его молекулы (числа степеней свободы) и не зависит от температуры.
6.Модель идеального газа и его уравнения состояния
Идальный газ – это воображаемый газ, состоящий из упругих молекул, между которыми отсутствуют силы взаимного притяжения и отталкивания, а объем, занимаемы этими молекулами, бесконечно мал по сравнению с объемом пространства между ними.
Основные свойства ид. газа:
Объем частиц газа равен нулю
Импульс передается только при соударениях
Суммарная энергия частиц постоянна.
Термическим уравнением состояния идеального газа является уравнение Клапейрона –Менделеева PV=RT. Теплоемкостью вещества называется отношение бесконечно малого количества теплоты, подводимого к веществу в каком-либо процессе, к соответствующему бесконечно малому изменению его температуры. Таким образом, согласно молекулярно – кинетической теории теплоемкость идеального газа зависит только от сложности его молекулы (числа степеней свободы) и не зависит от температуры.
|
|
|
В термодинамике изучают газовые смеси, представляющие собой механическую смесь различных газов, между которыми отсутствуют химические реакции, т.е. газовые смеси не изменящие свои свойста. Каждый газ, входящий в состав смеси занимает весь объём и имеет температуру равную температуре смеси. Будем считать, что каждый газ подчиняется уравнению Клапейрона:
PiV=miRiT, то для газовой смеси массой m можна записать уравнение состояния в виде: pV=mRстT, где Rст=8314,2/µсм.
Давление смеси идеальных газов равно сумме парциальных давлений компонентов смеси (закон Дальтона):
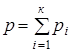
Смесь (раствор) - совокупность химически не взаимодействующих нескольких чистых веществ. Когда они образуют смесь, их называют компонентами, а саму смесь - многокомпонентной системой.
Примеры: воздух, водоаммиачные растворы, водка, сплавы металлов Частным случаем смесей (растворов) является газовая смесь (смесь различных газов) Пример: воздух, Смесь идеальных газов - совокупность материальных точек, отличающихся массой Ее можно рассматривать как идеальный газ с некоторыми средними характеристиками. Законы Дальтона — два физических закона, определяющих суммарное давление и растворимость смеси газов.

|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 1413; Нарушение авторских прав?; Мы поможем в написании вашей работы!