
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Определение параметров для основных точек цикла. Расчет производится с помощью таблиц термодинамических свойств газов
|
|
|
|
РАСЧЕТ ГАЗОВОГО ЦИКЛА С УЧЕТОМ ПЕРЕМЕННОЙ ТЕПЛОЕМКОСТИ
с = f(t),
Расчет производится с помощью таблиц термодинамических свойств газов.
Параметры P, V, t определяют также по уравнению состояния (4) и соотношении параметров в процессах, приведенных ранее. Исключение составляет адиабатный процесс. Поскольку с = f(t), то показатель адиабаты зависит от температуры.
 (33)
(33)
Поэтому соотношения формулы (34)

заменяют выражениями (35) и (36)


Безразмерные величины относительный объем q0 и относительное давление p0 взять из таблицы в зависимости от температуры.
Параметры U, i, S находят по таблицам, в которых отсчет внутренних удельных энергий, энтальпий и энтропий начинается с 0 К.
Для точки 1:
T 1=273+800C=353 К,
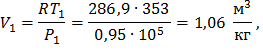
Рассмотрим адиабатный процесс 1-2:
При t 1=800C (T 1=353 K) относительный объем q 01=4210, тогда из формулы (35):
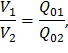
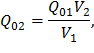

По таблице находим t 2»332,40C (T 2 »605,4 K).
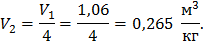
По таблице находим
p01 = 2,4553,
p02 » 16,8497, тогда из формулы (36):

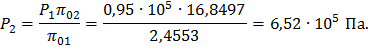
Из графика видно:


Рассмотрим изохору 2-3:
P 3= P 2×2,4=6,52×105×2,4=15,65×105 Па,

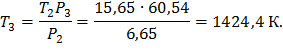
Рассмотрим политропный процесс 3-4:
P 3 V 3n= P 4 V 4n , (37)
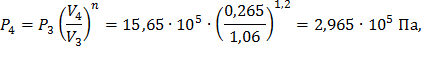
В формулу (7) предыдущего раздела подставляем соотношение параметров для политропы, получаем формулу (12) и выражаем T4:
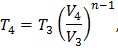
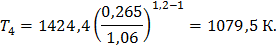
Параметры U, i, S найдем из таблицы (приблизительно). Все результаты параметров в таблице 4.
Таблица 4 – Результаты определения параметров в точках
| № точки | P, 105 Па | V, м3/кг | t, 0C | Т, К | U, кДж/кг | i, кДж/кг | S, кДж/(кг·К) |
| 0,95 | 1,06 | 252,80 | 353,60 | 6,8662 | |||
| 6,52 | 0,26 | 438,64 | 612,20 | 7,4182 | |||
| 15,6 | 0,26 | 1135,5 | 1544,2 | 8,3825 | |||
| 2,96 | 1,06 | 827,06 | 1136,8 | 8,0552 |
3.2 Определение 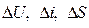 для каждого процесса
для каждого процесса
|
|
|
Изменение удельной внутренней энергии по формуле (38):
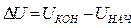 ; (38)
; (38)
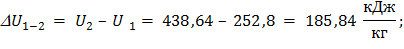
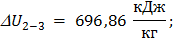

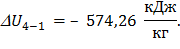
Изменение удельной энтальпии по формуле (39):
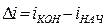 ; (39)
; (39)
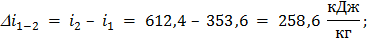
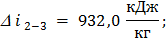
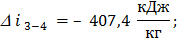
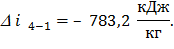
Изменение удельной энтропии по формуле (40):
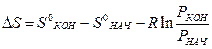 ; (40)
; (40)
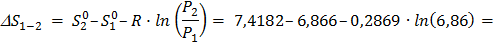
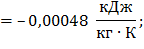
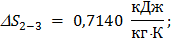


Результаты расчетов в таблице 5.
Таблица 5 – Результаты расчетов
| № процессов | 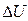 , кДж/кг , кДж/кг
|  , кДж/кг , кДж/кг
| 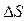 , кДж/(кг·К) , кДж/(кг·К)
| Примечания |
| 1-2 | 185,84 | 258,6 | –0,00048 | |
| 2-3 | 696,86 | 932,0 | 0,7140 | |
| 3-4 | –308,44 | –407,4 | 0,1495 | |
| 4-1 | –574,26 | –783,2 | –0,8629 | |
| Всего: | 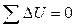
| 
| 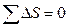
| – |
3.3 Определение q, l, l¢, j, y в каждом процессе
Удельное количество теплоты:
Для адиабатного:
q1-2=0 (n=k).
Для изохорного:
q 2-3 = D U = U 3 – U 2 = 696,86 кДж/кг (l=0);
q 4-1 = D U = –574,26 кДж/кг (l=0).
Для политропного формулы (41) и (42):

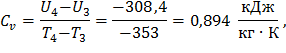

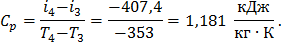
Показатель адиабаты формула (43):

k = 1,32.
Удельное количество теплоты формула (44):

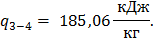
Удельная работа изменения объема газа в процессах:
Для адиабатного:

Для изохорного:
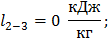
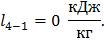
Для политропного:
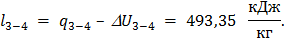
Удельная располагаемая работа (полезная) в процессах:
Для адиабатного:
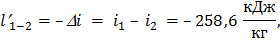
Для изохорного:
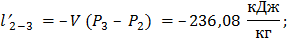

Для политропного:
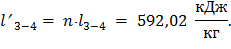
Коэффициенты распределения энергии в процессе по формулам (23) и (24) предыдущего раздела:
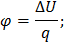
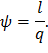
Все результаты сводятся в таблицу 6.
Таблица 6 – Результаты определения параметров в каждом процессе
| № процессов | q, кДж/кг | l, кДж/кг | l¢, кДж/кг | 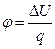
| 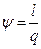
| |
| 1-2 | –185,84 | –258,60 | ||||
| 2-3 | 696,86 | –236,08 | ||||
| 3-4 | 185,06 | 493,35 | 592,02 | – 1,7 | 2,7 | |
| 4-1 | –574,26 | 213,06 | ||||
| Всего: | 
| 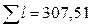
| 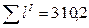
| – | – |
3.4 Определение lц, ht, pi
Полезная работа газа за цикл определяется:
как разность работ расширения и сжатия по формуле (45):
l ц= l расш – l сж ; (45)
как разность теплоты, подведенной и отведенной по формуле (46):
|
|
|
l ц = q 1 – q 2 = q подв – q отв. (46)
С учетом знаков плюс и минус полезная работа за цикл определяется как алгебраическая сумма, формулы (47) и (48):
l ц = l 1-2 + l 2-3 + l 3-4 + l 4-1 (47)
или
l ц = q 1-2 + q 2-3 + q 3-4 + q 4-1 (48)
или,
l¢ ц = l¢ 1-2 + l¢ 2-3 + l¢ 3-4 + l¢ 4-1 = 310,2 кДж/кг,
l ц= l 1-2 + l 2-3 + l 3-4 + l 4-1 = 307,51 кДж/кг,
Термический к.п.д., по формуле (30) как при постоянной теплоемкости:

Термический к.п.д. цикла по формуле (31):
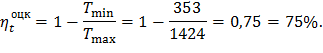
Среднецикловое давление (индикаторное) по формуле (32):
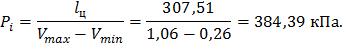
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 422; Нарушение авторских прав?; Мы поможем в написании вашей работы!