
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные теоретические положения. Цель проведения лабораторной работы
 |
Цель проведения лабораторной работы
ЛАБОРАТОРНАЯ РАБОТА № 3
Контрольные вопросы
1. В каких средах наблюдается химическая коррозия?
2. Является ли газовая коррозия локальной?
3. Какова основная причина химической коррозии металлов?
4. Дайте определение жаростойкости металлов и сплавов.
5. Дайте определение жаропрочности металлов и сплавов.
6. Какие факторы влияют на жаростойкость стали?
7. Приведите условие сплошности пленок?
8. Для каких металлов выполняется условие сплошности?
9. Как можно повысить жаростойкость металлов и сплавов?
10. Чем определяется скорость химической коррозии в установившемся режиме?
11. Чем определяется скорость химической коррозии при кинетическом контроле процесса?
12. Какие металлы повышают жаростойкость сталей?
13. Как влияет углерод на жаростойкость сталей?
14. Как влияет структура сталей на их жаростойкость?
15. Поясните суть трех теорий жаростойкого легирования.
16. Каким образом подготавливают образцы к выполнению лабораторной работы?
17. Какие приборы используют при выполнении лабораторной работы?
18. Какие показатели используют при оценке газовой коррозии?
19. Как рассчитываются массовые показатели коррозии?
20. Как перейти от массовых показателей коррозии к глубинному?
ВЛИЯНИЕ ВЕЛИЧИНЫ ПОВЕРХНОСТИ АНОДА И КАТОДА НА СИЛУ ТОКА ГАЛЬВАНИЧЕСКОГО ЭЛЕМЕНТА, РАБОТАЮЩЕГО
С КИСЛОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ
Определить влияние величины поверхности анода и катода на силу тока гальванического элемента Zn-Cu, работающего с кислородной деполяризацией.
Задачи проведения лабораторной работы состоят в том, чтобы
знать: принцип работы гальванического элемента, особенности протекания электрохимического коррозионного процесса и непосредственно катодного процесса с кислородной деполяризацией, влияние величины поверхности катода и анода на силу тока гальванического элемента, работающего с кислородной деполяризацией;
|
|
|
уметь: собрать электрическую схему, определить силу тока гальванического элемента.
3.2.1 Электрохимический механизм растворения металла в электролитах
Первопричиной коррозии металлов, в том числе и электрохимической коррозии является их термодинамическая неустойчивость. При взаимодействии с электролитами металлы растворяются, переходя в более стабильное окисленное (ионное) состояние. Электрохимический механизм коррозии описан электрохимической реакцией, которая протекает с участием свободных электронов. Ионизация атомов металла и восстановление окислительного компонента коррозийной среды протекает не в одном акте, а скорости этих процессов зависят от величины электродного потенциала металлов в электролитах.
Электрохимическое растворение металла - сложный процесс, который состоит из трех основных одновременно протекающих процессов (рисунок 3.1):
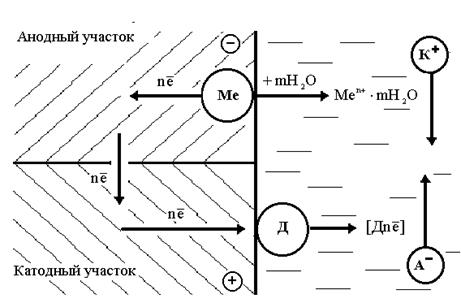 |
Рисунок 3.1 – Общая схема электрохимической коррозии
1) анодного - образование гидратированных ионов металла в электролите и некомпенсированных электронов на анодных участках по реакции:
ne neMen+ ® Men+×mН2O (3.1)
2) перетекание электронов в металле от анодных участков к катодным и соответствующие перемещения катионов и анионов в растворе;
3) катодного - ассимиляция электронов ионами или молекулами раствора (деполяризаторами Д), способными к восстановлению на катодных участках по реакции:
Д + ne ® [Дne] (3.2)
Таким образом, электрохимическая коррозия на неоднородной (гетерогенной) поверхности металла аналогична работе короткозамкнутого гальванического элемента. При замыкании в электролите двух обратимых электродов с разными потенциалами происходит перетекание электронов от более отрицательного электрода (анода) к менее отрицательному (более положительному) электроду (катоду). Перетекание электронов выравнивает значения потенциалов замкнутых электродов. Если бы при этом электродные процессы (анодный на аноде и катодный на катоде) не протекали, потенциалы электродов уравнялись бы и наступила бы полная поляризация. В действительности анодные и катодный электродные процессы продолжаются, препятствуя наступлению полной поляризации вследствие перетекания электронов от анода к катоду.
|
|
|
Ионы и молекулы раствора, которые обеспечивают протекание катодного процесса называют деполяризаторами.
3.2.2 Электрохимическая коррозия металла с кислородной
деполяризацией
Процессы коррозии металлов, при протекании которых катодная деполяризация осуществляется растворенным в электролите кислородом, называют коррозией с кислородной деполяризацией. Самопроизвольное протекание процесса коррозии металла с кислородной деполяризацией возможно, если (jМе)об.<  .:
.:
(jО2)об.= jоО2+  (3.3)
(3.3)
где (jО2)об. - обратимый потенциал кислородного электрода в данных условиях, В; jоО2 - стандартный потенциал кислородного электрода В; (jМе)об. - обратимый электродный потенциал металла, В; Р(О2) - парциальное давление кислорода, атм; а`ОН- - активность гидроксильных ионов; F - число Фарадея (96500 г×экв); R = 8,31 Дж/(К×моль) - газовая постоянная; T - абсолютная температура, К.
Коррозия металлов с кислородной деполяризацией в большинстве случаев происходит в электролитах, которые контактируют с атмосферой, парциальное давление кислорода в которой Р = 0,21 атм. Таким образом, при определении термодинамической возможности протекания коррозионных процессов с кислородной деполяризацией расчет обратимого потенциала кислородного электрода в этих электролитах следует делать, учитывая реальное парциальное давление кислорода в воздухе.
С кислородной деполяризацией корродируют металлы в атмосфере (например, ржавление оборудования металлургических заводов), в воде и нейтральных водных растворах солей (например, охладительные системы доменных и мартеновских печей, конвертеров, металлическое обшивка речных и морских судов), и в грунте (например, различные трубопроводы).
|
|
|
Для защиты металлических конструкций от коррозии с кислородной деполяризацией в нейтральных электролитах (пресной и морской воде, водных растворах солей, грунтах) существуют следующие методы:
1) применение достаточно стойких металлов и сплавов: термодинамически стойких в данных условиях (никель, медь и медных сплавы (бронзы)) – в морской воде; предрасположенных к пасивации (алюминий, хромистые и хромоникелевые стали) – в воде; тех, которые покрываются защитными пленками труднорастворимых продуктов коррозии (цинк, свинец) - в растворах сульфатов;
2) удаление из электролита деполяризатора – кислорода. Например, деаэрация или обескислороживание питающей воды паровых котлов или воды охлаждающих систем;
3) введение в воду или разбавленные растворы солей разных добавок, которые замедляют коррозию за счет сильного торможения анодного процесса, - пассиваторов или пленкообразователей (например фосфатов, полифосфатов, аминов);
4) нанесение на металлы разных защитных покрытий: металлических (например, на сталь - цинка, кадмия, никеля, олова, свинца и др.), неметаллических неорганических (оксидных, фосфатных для защиты от атмосферной коррозии) и органических (например, лакокрасочных, асфальто-битумных, полимерных и др.);
5) электрохимическая защита металлических конструкций катодной поляризацией от внешнего источника постоянного тока или с помощью протекторов, или анодной поляризацией при возможности пассивации металла.
3.2.3 Особенности катодного процесса кислородной деполяризации
Катодный процесс кислородной деполяризации включает следующие стадии:
· Растворение кислорода воздуха в электролите.
· Перенесение растворенного кислорода в объеме электролита и части слоя Прандтля в результате движения электролита, обусловленного конвекцией или дополнительным перемешиванием.
· Диффузионный перенос кислорода в слое электролита толщиной δ (в диффузном слое) или в пленке продуктов коррозии на металле к катодным участкам поверхности корродирующего металла.
|
|
|
· Ионизация кислорода по реакциям:
- в нейтральных растворах
О2 + 4е + 2Н2О = 4ОН-;
- в кислых растворах
О2 + 4е + 4Н+ = 2Н2О.
· Диффузия и конвективный перенос ионов ОН_ от катодных участков корродирующего металла вглубь раствора.
При коррозии металлов с кислородной деполяризацией наиболее затрудненными стадиями катодного процесса являются: при очень больших скоростях подведения кислорода к корродирующему металлу - ионизация кислорода, а в спокойных электролитах - диффузия кислорода. В последнем случае наблюдается непосредственная зависимость между количеством кислорода, который поступает в единицу времени к поверхности катода, и током, выработанным элементом (чем больше доступ кислорода, тем больше ток).
Величина доступа кислорода к поверхности анода, если это не вызовет пассивации анода, существенным образом не влияет на силу тока, так как наиболее медленным процессом является процесс диффузии кислорода к поверхности катода.
Сила тока гальванического элемента, который работает с кислородной деполяризацией, зависит от величины поверхности катода. Увеличение поверхности катода (при прочих равных условиях) вызовет увеличение количества кислорода, который притекает к его поверхности в единицу времени, и повышение силы тока элемента, если условия доступа кислорода к поверхности катода остаются прежними.
Увеличение поверхности анода в этих случаях не влияет на силу тока элемента, так как не ускоряет процессов деполяризации.
Для процессов коррозии металлов с кислородной деполяризацией характерна замедленность переноса кислорода к катодным участкам поверхности корродирующего металла. Это обусловлено малой концентрацией кислорода в электролитах (вследствие плохой его растворимости в воде и в водных растворах); медленной диффузией кислорода через слой электролита, прилегающий к поверхности металла; дополнительным затруднением диффузии кислорода через пленку вторичных труднорастворимых продуктов коррозии, часто образующихся на поверхности корродирующего металла.
Замедленность катодного процесса заметно влияет на скорость коррозии металлов с кислородной деполяризацией, а в многих случаях это влияние является преобладающим. Наиболее затрудненными стадиями катодного процесса кислородной деполяризации, а часто и всего коррозионного процесса, в зависимости от условий протекания, являются:
1) ионизация кислорода (кинетический контроль);
2) диффузия кислорода (диффузионный контроль);
3) ионизация и диффузия кислорода одновременно (смешанный диффузионно-кинетический контроль).
Кинетический контроль протекания катодного процесса (контроль перенапряжением ионизации кислорода) наблюдается при сравнительно небольших катодных плотностях тока и очень высоких скоростях подвода кислорода к металлу:
а) при сильном перемешивании электролита;
б) при очень тонкой пленке электролита на поверхности металла (при влажной атмосферной коррозии металлов).
Если электролитом является вода, то быстрый подвод кислорода к металлу может замедлить протекание анодного процесса вследствие наступления пассивности металла, что приведет к значительной анодной поляризации и повышению коррозийной стойкости металла при преобладающем влиянии анодного процесса.
Скорость коррозии металлов не склонных к пассивации в условиях сильной аэрации определяется в основном перенапряжением ионизации кислорода. В этом случае скорость коррозии зависит от природы металлов и содержания катодных примесей или структурных составляющих: чем ниже перенапряжение ионизации кислорода на микрокатодах, и, чем больше количество этих микрокатодов, тем выше скорость катодной реакции, а, следовательно, и коррозионного процесса.
Диффузионный контроль протекания катодного процесса (затрудненный доступ кислорода к катодным участкам) наблюдается при катодных плотностях тока, близких к предельной диффузионной плотности тока и очень малых скоростях подвода кислорода к металлу, обусловленных медленностью протекания диффузного процесса:
а) в спокойных (неперемешивающихся) электролитах;
б) при наличии на поверхности металла пленки труднорастворимых продуктов коррозии;
в) при подземной коррозии металлов.
Во многих случаях коррозии металлов с кислородной деполяризацией диффузия кислорода определяет скорость всего процесса. В этих условиях коррозионный ток (скорость коррозии металла) определяется только площадью катода.
Смешанный диффузионно-кинетический контроль протекания катодного процесса (сравнимое влияние на скорость катодного процесса перенапряжения ионизации и медленной диффузии кислорода), очевидно, наиболее распространенный случай коррозии металлов с кислородной деполяризацией. Довольно часто скорость коррозии металлов определяется скоростью протекания обеих стадий катодного процесса. Как и в предыдущем случае, процесс чувствителен к изменению условий диффузии кислорода. Вместе с тем скорость коррозии зависит от природы и количества катодных примесей, но в меньшей степени, чем при чисто кинетическом контроле процесса.
|
|
|
|
|
Дата добавления: 2015-05-07; Просмотров: 454; Нарушение авторских прав?; Мы поможем в написании вашей работы!