
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Свойства оксидов и гидроксидов марганца
|
|
|
|
| Оксиды | MnO | Mn2O3 | MnO2 | (MnO3) | Mn2O7 |
| Свойства | ярко выраженные основные | основные | амфотерные | кислотные | сильно кислотные |
| Гидроксиды | Mn(OH)2 | Mn(OH)3 | Mn(OH)4 H2MnO3 | H2MnO4 | HMnO4 |
| Свойства | ярко выраженные основные | основные | амфотерные | кислотные | сильно кислотные |
| Названия | гидроксид марганца (II); соли Mn(II) | гидроксид марганца (III); соли Mn(III) | гидроксид марганца (IV); манганаты(IV) | Марганцевая (VI) кислота; манганаты(VI) | марганцевая (VII) кислота; перманганаты |
| Усиление кислотных свойств |

| ||||
| Усиление основных свойств |

|
Соединения марганца (II). Оксид и гидроксид марганца (II) проявляют только основные свойства. Они нерастворимы в воде, но легко растворяются в кислотах с образованием солей двухвалентного марганца.
Большинство солей двухвалентного марганца хорошо растворимы в воде и подвергаются гидролизу по катиону. К труднорастворимым солям относятся средние соли – сульфид, фосфат и карбонат.
В кристаллическом состоянии соли марганца (II) имеют слабо розовую окраску, в водных растворах – практически бесцветны.
Гидроксид двухвалентного марганца образуется косвенным путём – действием щёлочи на растворы солей. В момент образования образуется белый осадок (чаще наблюдаемый как телесный), который на воздухе постепенно буреет под действием кислорода воздуха:
2Mn(OH)2(т) + 2Н2О(ж) + О2(г) → 2Mn(OH)4(т)
Марганец (II) образует комплексные соединения с координационным числом, равным шести. В водных растворах известны катионные комплексы в виде аквакомплекса [ Mn (Н2О)6]2+ и аммиаката [ Mn (NН3)6]2+ и анионные – тиоцианатные [ Mn (NSC)6]4– и цианидные [ Mn (CN)6]4-. Но комплексные соединения двухвалентного марганца неустойчивы и быстро разрушаются в водных растворах.
|
|
|
Соединения марганца (II) проявляют восстановительные свойства, окисляясь в нейтральной среде до марганца (IV), в сильнощелочной – до марганца (VI), а в кислой до марганца (VII):
3MnSO4(в) +2KClO3(в) +12KOH(в)→3K2MnO4(в) +2KCl(в) + 3K2SO4(в) + 6H2O(ж)
2MnSO4(в)+5PbO2(т)+6HNO3(в)→2HMnO4(в)+3Pb(NO3)2(в)+2PbSO4(в)+2H2O(ж)
Если in vitro Mn2+ проявляет восстановительные свойства, то in vivo Mn2+ восстановительные свойства выражены слабо за счёт стабилизирующего влияния биолигандов.
Соединения марганца (III). Соли трёхвалентного марганца окрашены в тёмный цвет и склонны к образованию комплексных солей (ацидокомплексов). Все соли марганца (III) малоустойчивы. В кислом растворе они легко восстанавливаются до солей марганца (II). В нейтральном растворе простые соли легко гидролизуются с образованием гидроксида Mn(III), который быстро переходит на воздухе в гидроксид марганца (IV). Гидроксид марганца (III) – Mn2O3 ּ Н2О или MnО(OH) встречается в природе в виде минерала манганита (бурая марганцевая руда). Искусственно полученный гидроксид марганца (III) применяют в качестве чёрно-бурой краски. Оксид марганца (III) при нагревании до температуры более 940 оС на воздухе или выше 1090 оС в токе кислорода переходит с смешанный оксид Mn3O4 устойчивого состава, что используется в весовом анализе.
Соединения марганца (IV). Оксид Mn(IV) наиболее устойчивое при обычных условиях кислородное соединение марганца. MnO2 и соответствующий ему гидроксид практически нерастворимы в воде.
MnO2 проявляет окислительно-восстановительную двойственность. В кислой среде он действует как сильный окислитель (+ 1,23 В), восстанавливаясь до Mn(II). На этом свойстве основан один из способов получения хлора:
MnO2(т) + 4HCl(в) → MnCl2(в) + Cl2(г) + 2H2O(ж)
В щелочной среде под действием окислителей Mn(IV) окисляется до Mn(VI).
Гидроксид марганца (IV) проявляет амфотерный характер – кислотный и основной в равной степени.
Соли марганца (IV) неустойчивы и разлагаются в водных растворах с образованием солей Mn(II).
|
|
|
Соединения марганца (VI). Оксид шестивалентного марганца в свободном виде не выделен. Гидроксид марганца (VI) проявляет кислотный характер. свободная марганцевая (VI) кислота неустойчива и диспропорционирует в водном растворе по схеме:
3H2MnO4(в) → 2HMnO4(в) + MnO2(т) + 2H2O(ж).
Манганаты (VI) образуются при сплавлении диоксида марганца со щёлочью в присутствии окислителей и имеют изумрудно-зелёную окраску. В сильно щелочной среде манганаты (VI) довольно устойчивы. При разбавлении щелочных растворов происходит гидролиз, сопровождающийся диспропорционированием:
3К2MnO4(в) + 2H2O(ж) → 2КMnO4(в) + MnO2(т) + 4КOH(в).
Манганаты (VI) – сильные окислители, восстанавливающиеся в кислой среде до Mn(II), а в нейтральной и щелочной средах – до MnO2. Под действием сильных окислителей манганаты (VI) могут быть окислены до Mn(VII):
2К2MnO4(в) + Cl2(г) → 2КMnO4(в) + 2КCl(в).
При нагревании выше 500 оС манганат (VI) распадается на продукты:
манганат (IV) и кислород:
2К2MnO4(т) → К2MnO3(т) + О2(г).
Соединения марганца (VII). Оксид марганца (VII) – Mn2O7 выделяется в виде темно-зеленой маслянистой жидкости при действии концентрированной серной кислоты на перманганат калия:
2KMnO4(т) + H2SO4(к) = K2SO4(в) + Mn2O7(ж) + H2O(ж).
Оксид марганца (VII) устойчив до 10 оС и разлагается со взрывом по схеме:
Mn2O7(ж) →2MnO2(т) + О3(г).
При взаимодействии Mn2O7 с водой образуется марганцовая кислота HMnO4, которая имеет фиолетово-красную окраску:
Mn2O7(ж) + H2O(ж) = 2HMnO4(в) (только в виде ионов MnO4– и Н+).
Безводную марганцовую кислоту получить не удалось, в растворе она устойчива до концентрации 20 %. Это очень сильная кислота, кажущаяся степень диссоциации в растворе концентрации 0,1 моль/дм3 равна 93 %.
Марганцовая кислота – сильный окислитель. Еще энергичнее взаимодействует Mn2O7, горючие вещества при соприкосновении с ним воспламеняются.
Соли марганцовой кислоты называются перманганаты. Наиболее важным из них является перманганат калия, он является очень сильным окислителем. С его окислительными свойствами по отношению к органическим и неорганическим веществам часто приходится встречаться в химической практике.
Степень восстановления перманганат-иона зависит от характера среды:
|
|
|
кислая среда Mn (II) (соли Mn2+)
 MnO4-+8H++5ē = Mn2++4H2O, Е0 = +1.51 B
MnO4-+8H++5ē = Mn2++4H2O, Е0 = +1.51 B
Перманганат нейтральная среда Mn (IV) (оксид марганца (IV))
MnO4-+2H2O+3ē=MnO2 +4OH-,Е0 = +1.23 B
щелочная среда Mn (VI) (манганаты M2MnO4)
MnO4-+ē = MnO42-, Е0 = +0.56 B
Как видно, наиболее сильные окислительные свойства перманганаты проявляют в кислой среде.
Образование манганатов происходит в сильнощелочном растворе, обеспечивающем подавление гидролиза K2MnO4. Так как реакция обычно проходит в достаточно разбавленных растворах, конечным продуктом восстановления перманганата в щелочной среде, как и в нейтральной, является MnO2 (см. диспропорционирование).
При температуре около 250 оС перманганат калия разлагается по схеме:
2KMnO4(т) 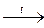 K2MnO4(т) + MnO2(т) + O2(г)
K2MnO4(т) + MnO2(т) + O2(г)
Перманганат калия применяется как антисептическое средство. Водные растворы его различной концентрации от 0,01 до 0,5% применяются для дезинфекции ран, полоскания горла и других антивоспалительных процедурах. Успешно 2 – 5% растворы перманганата калия употребляются при ожогах кожи (кожа подсушивается, и пузырь не образуется). Для живых организмов перманганаты являются ядами (вызывают коагуляцию белков). Их обезвреживание производят 3 %-ным раствором Н2О2, подкисленным уксусной кислотой:
2KMnO4+5Н2О2+6СН3СООН →2Mn(СН3СОО)2+2СН3СООК +8Н2О+ 5O2
Марганец – биологически активный микроэлемент, содержащийся в живых организмах. В организме человека содержится около 12 мг марганца, причём 43% этого количества находится в костях, а остальное – в мягких тканях. Он входит в состав ряда ферментов. Двухвалентный марганец усиливает каталитическую активность большого числа ферментов различных классов – трансфераз, гидролаз, изомераз. Фермент глутаминсинтетаза, содержащий марганец, катализирует биосинтез глутамина из глутаминовой кислоты и аммиака с участием АТФ. Ионы Mn2+ стабилизируют конформацию нуклеиновых кислот, участвуют в процессах репликации ДНК, синтезе РНК и белка. Ионы Mn3+ совместно с Fe3+ входит в состав трансферина, супероксиддисмутазы и кислотной фосфатазы – в состав типичных металлопротеинов.
Марганец влияет на кроветворение, рост, размножение, минеральный, липидный и углеводный обмен, развитие скелета.
|
|
|
В токсикологии перманганат калия используется для качественного обнаружения метанола, новокаина, кокаина.
Раствор перманганата калия применяется качестве титранта при количественном определении восстановителей: Fe2+, C2O42-, поли- и оксикарбоновых кислот, альдегидов, муравьиной, мочевой, аскорбиновой кислот методом прямого титрования и ряда окислителей (например, нитратов и нитритов)– методом обратного титрования.
Соединения марганца являются сильными ядами, действующими на центральную нервную систему, поражающими почки, лёгкие, сердце.
|
|
|
|
|
Дата добавления: 2015-05-09; Просмотров: 29384; Нарушение авторских прав?; Мы поможем в написании вашей работы!