
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные теоретические сведения
|
|
|
|
Параллельное соединение резисторов.
Лабораторная работа №5.
Обесцвечивание раствора
Фосфат серебра
Анионы 1 группы
АНИОНЫ
КАТИОНЫ IV ГРУППЫ
Pb2+, Cu2+, Hg2+, Ag+
Реакции катиона Ag+
1) 2AgNO3 + 2NaOH → 2AgOH ↓ + 2NaNO3
Ag2O↓ + H2O
оксид серебра (бурый)
2) 2AgNO3 + K2CrO4 → Ag2CrO4↓ + 2KNO3
хромат серебра (кирпично-красный)
3) AgNO3 + KBr → AgBr↓ + KNO3
бромид серебра (бледно-желтый)
4) AgNO3 + KI → AgI↓ + KNO3
йодид серебра (ярко-желтый)
Реакции катиона Pb2+
1) Pb(NO3)2 + 2NaOH → Pb(OH)2↓ + 2NaNO3
гидроксид свинца (белый)
2) Pb(NO3)2 + K2CrO4 → PbCrO4 ↓ + 2KNO3
хромат свинца (желтый)
3) Pb(NO3)2 + H2SO4 → PbSO4 ↓ + 2HNO3
Сульфат свинца (белый)
4) Pb(NO3)2 +2KI → PbI2 ↓ + 2KNO3
Йодид свинца (желтый)
Реакции катиона Cu2+
1) Cu(NO3)2 + 2NaOH → Cu(OH)2 ↓ + 2NaNO3
Гидроксид меди (голубой)
2) CuSO4 + Na2S2O3 + H2O → CuS ↓ + Na2SO4 + H2SO4
тиосульфат натрия сульфид меди (черный)
3) 2Cu(NO3)2 + K4[Fe(CN)6] → Cu2 [Fe(CN)6] ↓ + 4KNO3
Гекса-циано-феррат меди (красно-бурый)
Реакции катиона Hg2+
1) Hg(NO3)2 + 2NaOH → HgO ↓ + 2NaNO3 + H2O
оксид ртути (желтый)
2) Hg(NO3)2 + 2KI → HgI2 ↓ + 2KNO3
йодид ртути (оранжево-красный)
3) Hg(NO3)2 + Na2S2O3 + H2O → HgS ↓+ H2SO4 + 2NaNO3
Сульфид ртути (черный)
| Реактивы | Ag+ | Pb2+ | Cu2+ | Hg2+ |
| NaOH гидроксид натрия | Ag2O ↓ оксид серебра (бурый) | Pb(OH)2↓ гидроксид свинца (белый) | Cu(OH)2↓ гидроксид меди (голубой) | HgO↓ оксид ртути (желтый) |
| K2CrO4 хромат калия | Ag2CrO4↓ хромат серебра (кирпично-красный) | PbCrO4 ↓ хромат свинца (желтый) | _ | _ |
| KBr Бромид калия | AgBr ↓ бромид серебра (св.-желт.) | _ | _ | _ |
| KI йодид калия | AgI ↓ йодид серебра (яр.-желт.) | PbI2 ↓ йодид свинца (желт.) | _ | HgI2 ↓ йодид ртути (оранж.-красн.) |
| H2SO4 серная кислота | _ | PbSO4↓ Сульфат свинца (белый) | _ | _ |
| Na2S2O3 тиосульфат натрия | _ | _ | CuS ↓ сульфид меди (черн.) | HgS ↓ сульфид ртути (черн.) |
| K4[Fe(CN)6] гексациано-феррат калия | _ | _ | Cu2[Fe(CN)6] гексациано-феррат меди (красно-бур.) | _ |
Классифицируются по способности взаимодействовать AgNO3 и BaCl2
|
|
|
| № группы | Характеристика группы | Анионы |
| Взаимодействие с AgNO3 и BaCl2 с образованием осадков – растворимы с HNO3 | CO32- - карбонаты SO42- - сульфаты SO32- - сульфиты S2O32- - тиосульфаты PO43- - фосфаты | |
| Взаимодействие с AgNO3 с образованием осадков – растворимы с HNO3; Взаимодействие с BaCl2 без образования осадка. | Cl- - хлорид I- - йодид Br- - бромид S2- - сульфид | |
| Взаимодействие с AgNO3 и BaCl2 без образования осадков | NO3- - нитрат NO2- - нитрит СH3COO- - ацетат |
1) Катион – сульфит:
Na2SO3 + 2HCl → 2NaCl + SO2 ↑+ H20
Оксид серы (резкий запах)
2) Катион – сульфат:
H2SO4 + BaCl2 → BaSO4↓ + 2HCl
Сульфат бария (белый)
3) Катион – фосфат:
Na2HPO4+ 3AgNO3→Ag3PO4↓+ 2NaOH+HNO3
4) Катион – сульфит:
Na2SO3 + I2 + H2O → Na2SO4 + 2HI
Цель лабораторной работы: Экспериментально проверить расчет эквивалентного сопротивления при параллельном соединении резисторов.
В лабораторной работе исследуется параллельное соединение трех резисторов (Рис 1).
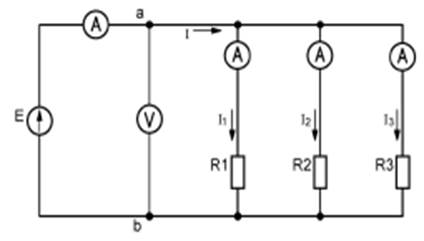
Рисунок 1. Схема параллельного соединения трех резисторов.
При параллельном соединении ко всем резисторам цепи приложено одинаковое напряжение. Поэтому согласно закону Ома:
I1= 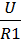 ; I2 =
; I2 =  ; I3 =
; I3 = 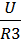
Согласно закону токов Кирхгофа, общий ток цепи:
I= I1+ I2 + I3
или

Соответственно, эквивалентное сопротивление рассматриваемой цепи при параллельном соединении трех резисторов определяется формулой
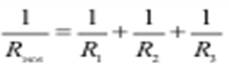
Если в формуле (4) вместо значений 1/R использовать соответствующие значения проводимости:
G = 1/R
то получим альтернативное написание:
Gэкв = G1 + G2 +G3
Эквивалентная проводимость параллельной цепи равна сумме проводимостей параллельно соединенных резисторов. Следовательно, при увеличении числа параллельно включаемых резисторов эквивалентная проводимость электрической цепи увеличивается (а эквивалентное сопротивление – уменьшается). Из приведенных выше формул также следует, что токи между параллельно соединенными резисторами распределяются обратно пропорционально их сопротивлениям, т.е. чем больше сопротивление ветви в параллельной цепи, тем меньше ток в этой ветви. В случае параллельного соединения нескольких (n) резисторов с одинаковым сопротивлением R эквивалентное сопротивление цепи Rэкв будет в n раз меньше сопротивления R.
|
|
|
Rэкв = R/n
|
|
|
|
|
Дата добавления: 2015-05-10; Просмотров: 373; Нарушение авторских прав?; Мы поможем в написании вашей работы!