
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Характеристика білків, жирів, вуглеводів та нуклеїнових кислот
|
|
|
|
Молекулярний рівень організації живої природи
Розділ 5. Сучасні рівні організації живої природи
До складу клітини входять високомолекулярні органічні сполуки – білки, нуклеїнові кислоти, складні вуглеводи (полісахариди), молекули яких складаються з великої кількості однакових чи різних за хімічною будовою ланок, що повторюються, називають біополімерами (від грец. біос та поліс – численний). Прості молекули, із залишків яких складаються біополімери, називають мономерами (від грец. монос – один, поодинокий). Особлива група органічних сполук – це біологічно активні речовини – ферменти.
Білки, їх будова та функція. Білки – це високомолекулярні біополімери, мономерами яких є залишки амінокислот. Нескінченна різноманітність білкових молекул забезпечується різними комбінаціями залишків лише 20 амінокислот. Кожен білок характеризується постійним складом амінокислотних залишків та їхньою певною послідовністю.
Усі амінокислоти мають спільну групу атомів. Вона складається з аміногрупи (-NH2), якій притаманні лужні властивості, та карбоксильної групи (—СООН) із кислотними властивостями. Ці групи, як і атом гідрогену, зв’язані з одним і тим самим атомом карбону. Групи атомів, за якими амінокислоти розрізняються між собою, називають радикалами, або R–групами.
Амінокислоти поділяють на замінні та незамінні. Замінні амінокислоти можуть синтезуватись в організмі людини і тварин із продуктів обміну речовин, незамінні амінокислоти в організмі людини і тварин не синтезуються. Вони надходять разом із їжею. Їх синтезують рослини, гриби, бактерії.
Залежно від конфігурації розрізняють білки фібрилярні та глобулярні. Молекули фібрилярних білків складаються з поліпептидних ланцюгів. Ці білки нерозчинні у воді й виконують в організмі структурну функцію (наприклад, кератин входить до складу волосся людини або шерсті тварин).
|
|
|
Молекули глобулярних білків складаються зі щільно скручених поліпептидних ланцюгів і за формою нагадують кульку. Ці білки здебільшого розчинні у воді та сольових розчинах. Вони виконують в організмі різноманітні функції (наприклад, гемоглобін забезпечує транспортування газів).
Залежно від особливостей будови білки поділяють на прості та складні. Прості, або протеїни (від грец. протос — перший), складаються лише з амінокислотних залишків, а складні, або протеїди (від грец. протос та ейдос – вигляд), у своєму складі мають також залишки фосфатної та нуклеїнових кислот, вуглеводів, ліпідів, атоми Феруму, Цинку, Купруму та ін.
Для білків характерні чотири рівні структурної організації (рис.1):
Первинна структура білків визначається якісним і кількісним складом амінокислотних залишків, з’єднаних пептидними зв’язками, а також їхньою послідовністю. Часто молекула білка у вигляді ланцюга, складеного з амінокислотних залишків, нездатна виконувати специфічні функції.
Вторинна структура характеризує просторову організацію білкової молекули, яка закручується у спіраль. Радикали амінокислот (R–групи) при цьому залишаються ззовні спіралі. У підтриманні вторинної структури важлива роль належить водневим зв’язкам, які виникають між атомами гідрогену NH2–груп одного витка спіралі та оксигену СО–групи іншого.

Рис.1. Просторові моделі структурної організації білків
Третинна структура зумовлена здатністю поліпептидної спіралі закручуватись у грудку – глобулу (від лат. глобулюс – кулька). Підтримання третинної структури відбувається за рахунок дисульфідних зв’язків, які виникають між залишками амінокислоти цистеїну.
|
|
|
Четвертинна структура білків виникає внаслідок об’єднання окремих глобул, які разом утворюють функціональну одиницю – агрегати. Стабілізація четвертинної структури досягається гідрофобними, електростатичними та іншими взаємодіями, а також водневими зв’язками.
Функції білків:
1. Будівельна (структурна). Білки є складовою частиною біологічних мембран (колаген, осеїн).
2. Захисна.Полягає у запобіганні пошкодженням клітин, органів, проникненню в організм мікроорганізмів (імуноглобуліни або антитіла).
3. Сигнальна. Окремі складні білки клітинних мембран, змінюючи свою структуру, передають сигнали із зовнішнього середовища на інші ділянки мембрани або всередину клітини.
4. Скоротлива (рухова). Завдяки цій функції клітини, тканини, органи або весь організм можуть змінювати форму, рухатися. Скоротливі білки актин та міозин входять до складу м’язових клітин.
5. Запасна. Деякі білки можуть відкладатися у клітинах “про запас”.
6. Живильна. В ендоспермі насіння багатьох видів рослин (пшениці, кукурудзи, рису ін.) відкладаються білки, які споживають зародки.
7. Транспортна. Це одна з головних функцій білків, що забезпечує газообмін у клітинах і тканинах. Гемоглобін – пігмент крові людини – переносить кисень та деяку частку вуглекислого газу (10%).
8. Енергетична. За повного розщеплення 1 г білків у середньому звільняється 17,2 кДж енергії.
9. Регуляторна. Деякі білки (гормони, ферменти) регулюють активність обміну речовин, процеси росту і розвитку організмів.
10. Каталітична. Каталіз (припинення) – зміна швидкості перебігу хімічних реакцій під дією певних хімічних сполук. Каталітичну функцію – біокаталіз – у живих організмів виконують ферменти.
Ферменти – це прості (однокомпонентні) або складні (двокомпонентні) білки. Їх зараз відомо понад 6000. Ферменти прискорюють перебіг біохімічних процесів у 100 – 1000 разів порівняно з тими, які відбуваються у середовищі без ферментів. Завдяки ферментам енергія, необхідна для перебігу реакції, менша, ніж без їхньої участі. Активність ферментів виявляється лише за відповідних умов: певної температури, тиску, кислотності середовища тощо. Ферментативні реакції відбуваються у кілька етапів. Ферменти утворюють нестійкий комплекс із речовинами, які вступають у реакцію. Цей комплекс згодом швидко розпадається з утворенням продуктів реакції. Сам фермент при цьому свою структуру не втрачає і здатний каталізувати наступну подібну реакцію.
|
|
|
Ліпіди, їх будова та функція. Ліпіди – органічні сполуки, нерозчинні у воді (тобто гідрофобні), їх можна виділити з клітин за допомогою неполярних розчинників (ефіру, хлороформу, ацетону тощо). Ліпіди здатні утворювати складні сполуки з білками, вуглеводами, залишками фосфатної кислоти тощо. Найпоширеніші серед ліпідів – жири. Вміст жирів у клітинах становить від 5 до 15% сухої речовини, а у клітинах жирової тканини (наприклад, у жировому тілі комах) – до 90%. Підвищений вміст жирів характерний для нервової тканини, підшкірної клітковини, сальника, молока ссавців тощо. Багато жирів міститься у клітинах плодів та насінні певних видів рослин (соняшника, волоського горіха, маслини та ін.). До ліпідів також належать воски, що здійснюють переважно захисну функцію. У ссавців воски, які виділяють сальні залози, змащують поверхню шкіри, надаючи їй еластичності та зменшуючи зношення волосяного покриву. У птахів воски секретує куприкова залоза. Восковий шар вкриває листки наземних рослин і поверхню зовнішнього скелета членистоногих – мешканців суходолу, запобігаючи надлишковому випаровуванню води організмами. Інша група ліпідів – стероїди. Вони є важливими компонентами вітаміну D, деяких статевих гормонів, гормонів кори надниркових залоз.
Одна з найважливіших функцій ліпідів у живих організмах – енергетична. У разі повного окиснення 1 г жирів до вуглекислого газу і води виділяється 38,9 кДж енергії, тобто майже удвічі більше, ніж при повному розщепленні такої самої кількості вуглеводів. До того ж при окисненні 1 г жирів утворюється 1,1 г води. Саме завдяки запасам жиру деякі тварини можуть відносно тривалий час обходитися без води. Наприклад, верблюди в пустелі можуть не пити по 10 – 12 діб, а ведмеді, бабаки та інші тварини під час зимової сплячки не споживають води понад два місяці. Необхідну для їхніх процесів життєдіяльності воду ці тварини одержують унаслідок окиснення жирів, відкладених про запас. Іншою важливою функцією ліпідів є будівельна: фосфоліпіди (тобто ліпіди, які містять фосфатні групи) є основою клітинних мембран, входять до складу нервових волокон тощо. Захисна функція ліпідів полягає у захисті внутрішніх органів від механічних пошкоджень (наприклад, нирки людини вкриті м’яким жировим шаром). Накопичуючись у підшкірній клітковині деяких тварин (китів, тюленів та ін.), жири виконують теплоізоляційну функцію, запобігаючи переохолодженню. Так, у синього кита шар жиру у підшкірній клітковині може становити 50 см. У жировому тілі комах можуть накопичуватися кінцеві продукти обміну речовин. Жирова тканина у цих тварин здійснює видільну функцію. Ліпіди входять до складу деяких біологічно активних речовин, наприклад певних гормонів. Вони беруть участь у регуляції життєвих функцій організмів, зокрема в обміні речовин у хребетних тварин і людини.
|
|
|
Будова та функції вуглеводів. Хімічний склад вуглеводів відповідає формулі (СН2O)n, де n дорівнює трьом та більше. У клітинах тварин і людини вміст вуглеводів незначний. Натомість у клітинах рослин їх значно більше (наприклад, у листках, насінні, плодах – майже 70%, у бульбах картоплі – до 90%).
Залежно від кількості мономерів, що входять до складу молекул, вуглеводи поділяють на три основні класи:
Моносахариди, або прості цукри, залежно від кількості атомів Карбону, поділяють на тріози (3 атоми), тетрози (4), пентози (5), гексози (6) і так далі до декоз (10). У природі найпоширеніші гексози, а саме глюкоза і фруктоза. Солодкий присмак ягід, фруктів, меду залежить від вмісту в них цих сполук. Серед пентоз важливе значення мають рибоза і дезоксирибоза, які входять до складу нуклеїнових кислот та аденозинтрифосфорної кислоти (АТФ).
Олігосахариди – сполуки, в яких кілька залишків молекул моносахаридів з’єднані між собою ковалентними зв’язками. Серед них найпоширеніші дисахариди, які утворюються внаслідок сполучення залишків двох молекул моносахаридів. Наприклад, буряковий (або тростинний) цукор – сахароза – складається із залишків глюкози і фруктози, а солодовий – мальтоза – лише із залишків глюкози тощо. Дисахариди мають солодкий присмак. Вони, як і моносахариди, добре розчинні у воді.
Полісахариди – молекули, молекулярна маса яких може сягати кількох мільйонів. Полісахариди розрізняються між собою складом мономерів, довжиною та розгалуженістю ланцюгів. Полісахариди майже не розчиняються у воді й не мають солодкого присмаку. Один із найпоширеніших полісахаридів – крохмаль. Він синтезується у процесі фотосинтезу у клітинах рослин і складається із залишків глюкози. Крохмаль у значній кількості відкладається у клітинах рослин, насамперед листків, насіння, бульб тощо. У клітинних стінках рослин міститься полісахарид целюлоза – міцний, волокнистий, нерозчинний у воді. Деревина, кора, бавовна складаються переважно з целюлози.
У грибів, тварин і людини запасним полісахаридом є глікоген. Він відкладається здебільшого у м’язах і клітинах печінки. До складу клітинних стінок деяких грибів і зелених водоростей, кутикули членистоногих входить полісахарид хітин.
Основні функції вуглеводів у живих організмах – енергетична та будівельна. Енергетична функція вуглеводів полягає у здатності розщеплюватися з виділенням енергії. За повного розщеплення 1 г цих сполук вивільняється 17,2 кДж енергії. Кінцеві продукти окиснення вуглеводів – С02 і Н20. Будівельна, або структурна, функція вуглеводів полягає в тому, що ці сполуки входять до складу опорних елементів клітин організмів: хітин є компонентом зовнішнього скелета членистоногих, грибів і водоростей. Клітинні стінки рослин містять целюлозу, захищають їх і підтримують їхню форму.
Будова і функції нуклеїнових кислот. Нуклеїнові кислоти — це складні високомолекулярні біополімери, мономерами яких е нуклеотиди. Молекула нуклеотиду складається із залишків нітратної основи, п’ятивуглецевого моносахариду (пентози) і фосфатної кислоти.
Залежно від виду пентози, що входить до складу нуклеотиду, розрізняють два типи нуклеїнових кислот: дезоксирибонуклеїнову (ДНК) та рибонуклеїнову (РНК). До складу ДНК входить залишок дезоксирибози, а РНК – рибози. У молекулах ДНК і РНК містяться залишки таких нітратних основ: аденіну (скорочено позначається літерою А), гуаніну (Г), цитозину (Ц), тиміну (Т), а у РНК – замість тиміну урацил (У).
1953 року Джеймс Уотсон і Френсіс Крик запропонували модель просторової структури ДНК, правильність якої згодом було підтверджено експериментально. Молекула ДНК складається з двох ланцюгів нуклеотидів, які з’єднуються між собою за допомогою водневих зв’язків (рис. 2).
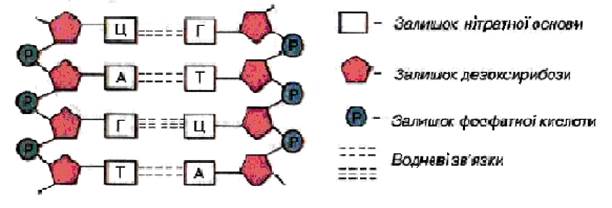
Рис. 2. Ділянка подвійної спіралі ДНК
|
 Ці зв’язки виникають між двома нуклеотидами, які ніби доповнюють один одного за розмірами. Залишок аденіну (А) завжди сполучається із залишком тиміну (Т) (між ними виникає два водневі зв’язки), а гуаніну (Г) – із залишком цитозину (Ц) (між ними виникає три водневі зв’язки) (рис. 3). Відповідно до запропонованої моделі будови ДНК два ланцюги нуклеотидів обвивають один одного, створюючи закручену праворуч спіраль (вторинна структура ДНК). При цьому діаметр спіралі становить приблизно 2 нм (нанометр дорівнює 1*10-6 міліметра). За певних умов (дія кислот, лугів, високої температури тощо) відбувається процес денатурації ДНК – розривання водневих зв’язків між комплементарними нітратними основами різних
Ці зв’язки виникають між двома нуклеотидами, які ніби доповнюють один одного за розмірами. Залишок аденіну (А) завжди сполучається із залишком тиміну (Т) (між ними виникає два водневі зв’язки), а гуаніну (Г) – із залишком цитозину (Ц) (між ними виникає три водневі зв’язки) (рис. 3). Відповідно до запропонованої моделі будови ДНК два ланцюги нуклеотидів обвивають один одного, створюючи закручену праворуч спіраль (вторинна структура ДНК). При цьому діаметр спіралі становить приблизно 2 нм (нанометр дорівнює 1*10-6 міліметра). За певних умов (дія кислот, лугів, високої температури тощо) відбувається процес денатурації ДНК – розривання водневих зв’язків між комплементарними нітратними основами різнихполінуклеотидних ланцюгів. Денатурована ДНК
після припинення дії факторів, які її спричиняють, може поновити свою структуру завдяки відновленню водневих зв’язків між комплементарними нуклеотидами (процес ренатурації ДНК).
Інформаційна РНК є копією певної ділянки молекули ДНК (одного чи кількох генів). Вона переносить спадкову інформацію від ДНК до місця синтезу молекули білка, а також бере безпосередню участь у її збиранні. Частка і-РНК становить приблизно 2% загальної кількості РНК клітини.
Транспортна РНК порівняно з інформаційною має менші розміри. Її частка становить до 20% загальної кількості РНК у клітині. Вона приєднує до себе амінокислоти і переносить їх до місця синтезу білкової молекули. Кожну амінокислоту транспортує специфічна т-РНК. Транспортна РНК має постійну вторинну структуру, яка за формою нагадує листок конюшини. Така просторова структура зумовлена водневими зв’язками між комплементарними нуклеотидами. Біля верхівки такого «листка конюшини» розташовані три нуклеотиди, що визначають, яку саме амінокислоту слід транспортувати. Сама амінокислота приєднується за допомогою ковалентного зв’язку до ділянки біля основи молекули т-РНК.
Рибосомна РНК становить приблизно 80% загальної кількості РНК у клітині. Вона входить до складу особливих органел клітин усіх типів — рибосом. Взаємодіючи з білками, р-РНК виконує структурну функцію і бере певну участь у процесах синтезу білків). Але в передачі спадкової інформації вона участі не бере.
Молекула АТФ складається із залишків нітратної основи (аденіну), вуглеводу (рибози) та трьох залишків фосфатної кислоти. АТФ – універсальна сполука. У її високоенергетичних хімічних зв’язках запасається значна кількість енергії. Якщо за участю відповідного ферменту від молекули АТФ відщепляється один залишок фосфатної кислоти, АТФ перетворюється на аденозиндифосфатну кислоту (АДФ). При цьому звільняється приблизно 42 кДж енергії. Коли ж від молекули АТФ відщепляються два залишки фосфатної кислоти, вона перетворюється на аденозинмонофосфатну кислоту (АМФ). При цьому енергії звільняється вже до 84 кДж. Енергія використовується для синтезу необхідних організму сполук, на підтримання певної температури тіла, забезпечення різних процесів життєдіяльності.
|
|
|
|
|
Дата добавления: 2015-05-26; Просмотров: 14854; Нарушение авторских прав?; Мы поможем в написании вашей работы!